Лекция для врачей "Боль в кистевом суставе после травмы (перелом)" (отрывок из книги "Детская ортопедия" - Виссер Я. Д.)
Боль в кистевом суставе после травмы
- Обследование: может определяться боль при пальпации в зоне анатомической табакерки или по всей поверхности кистевого сустава.
- Дифференциальная диагностика:
- Недиагностированный перелом ладьевидной кости
- Недиагностированный перелом по типу «пряжки» (веретенообразный перелом)
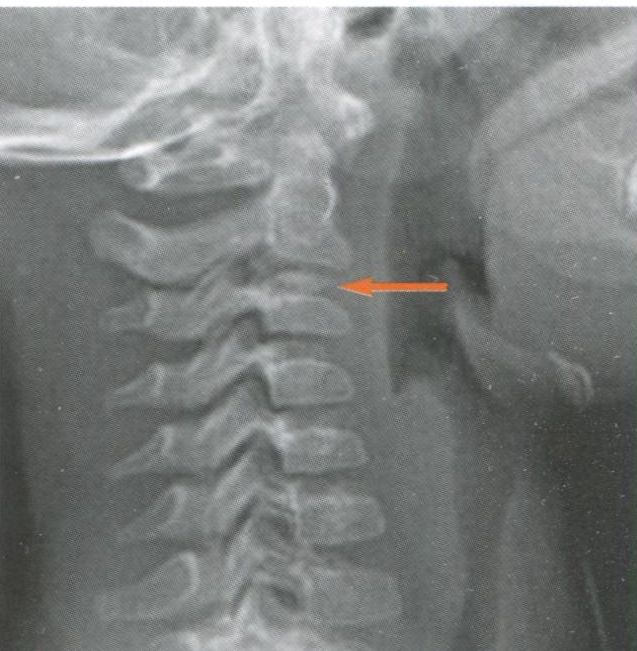
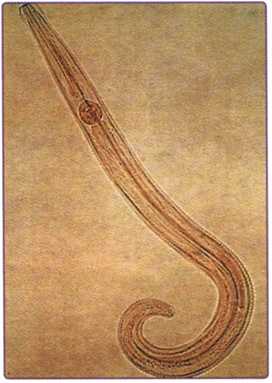
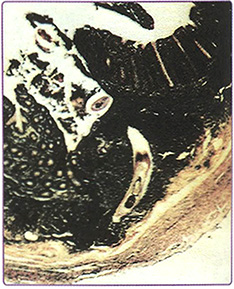
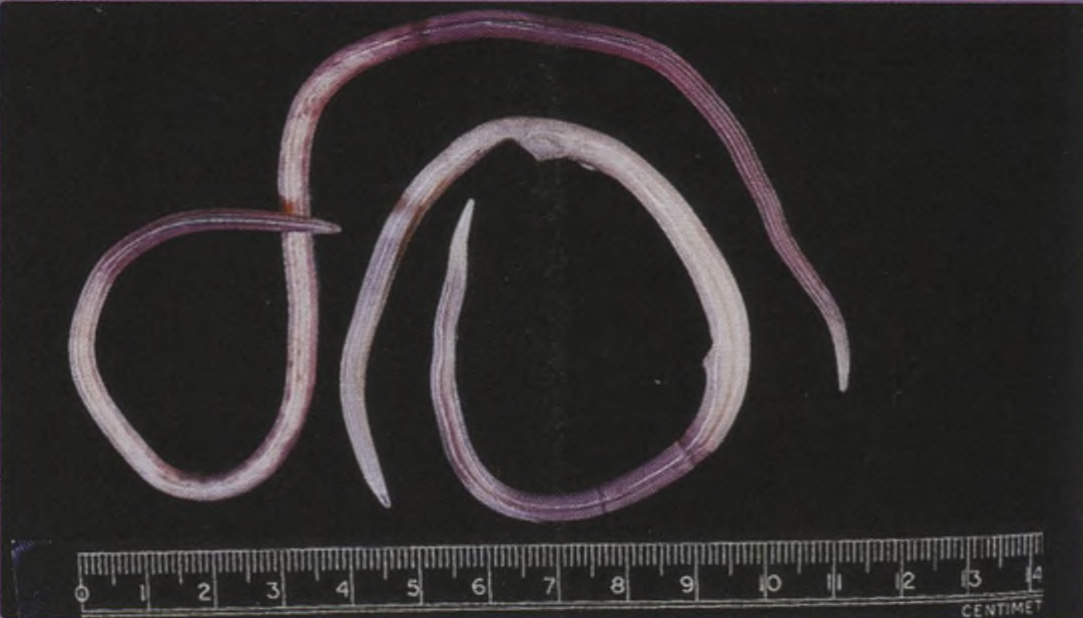
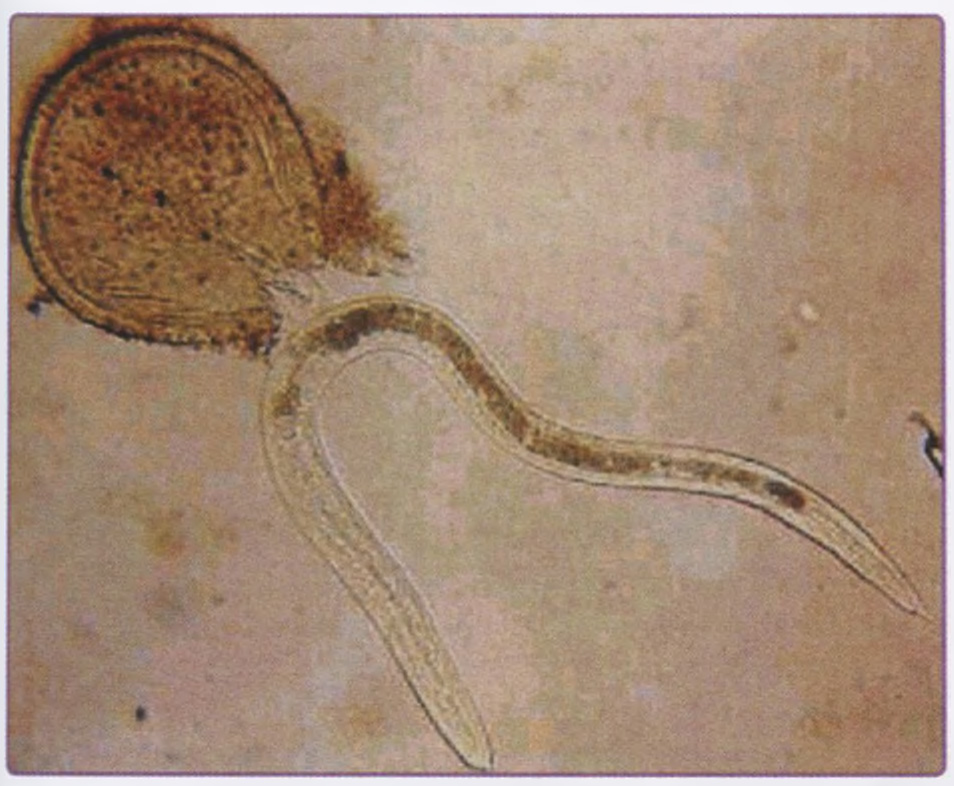
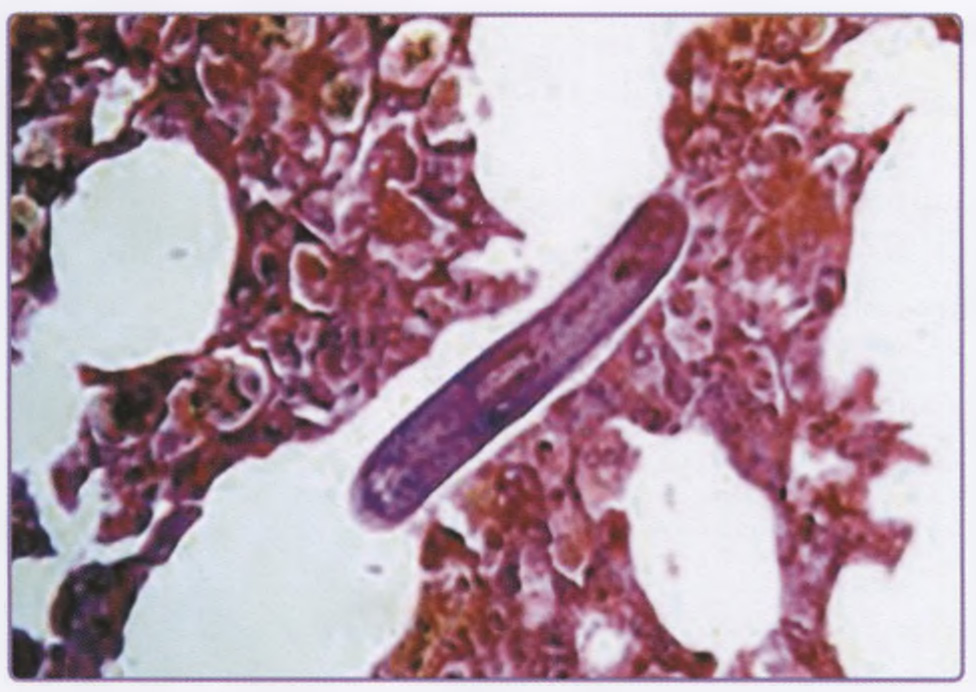
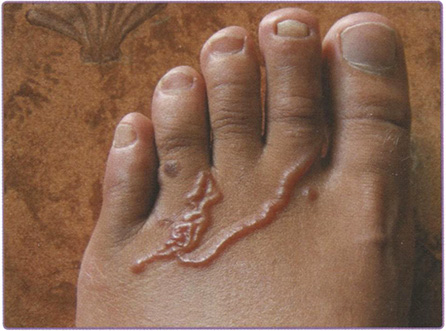
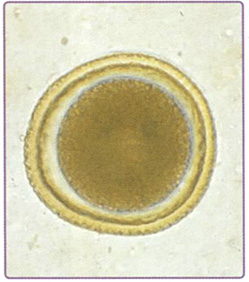
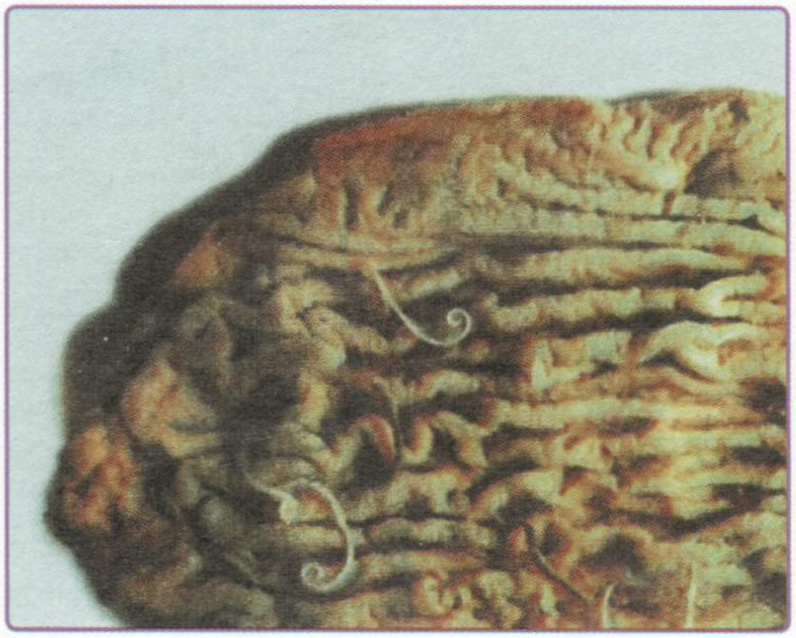
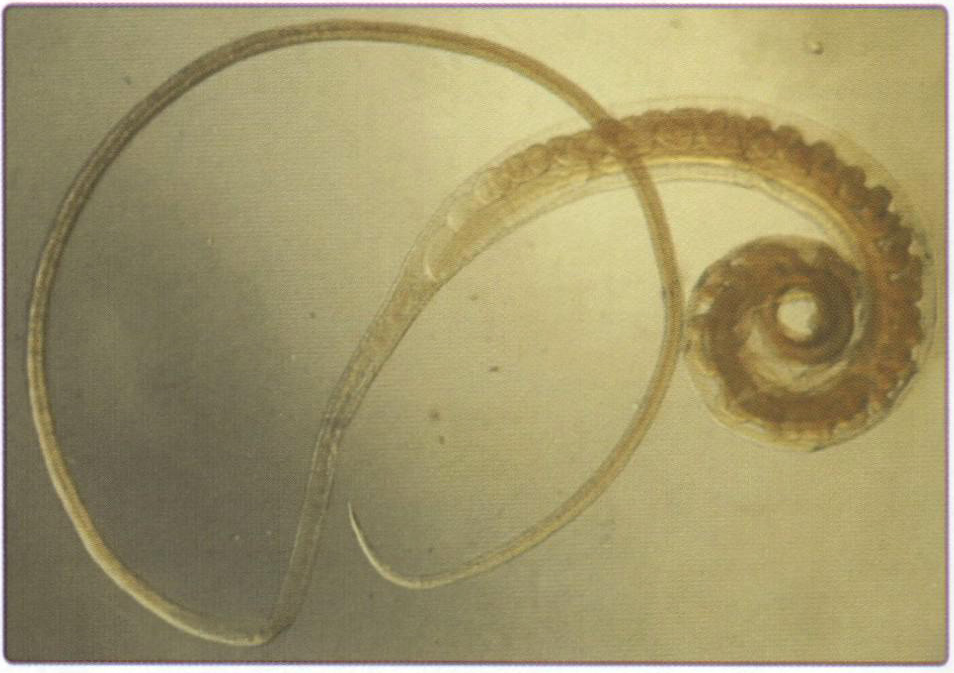
Пояснение: недиагностированный перелом ладьевидной кости. Перелом ладьевидной кости является наиболее частым переломом в области запястья. Он обычно встречается у подростков и молодых людей в возрасте от 14 до 30 лет, но может случаться и в период полового созревания. У детей младшего возраста подобное повреждение встречается крайне редко. Примерно в 40 % случаев перелом не диагностируется, поскольку пациенты уделяют недостаточно внимания повреждению или перелом не распознаётся при рентгенографии в отделении оказания экстренной медицинской помощи, выполненной после травмы (рис. 7.6). При обследовании пальпаторно определяется болезненность в области анатомической табакерки (рис. 7.7).
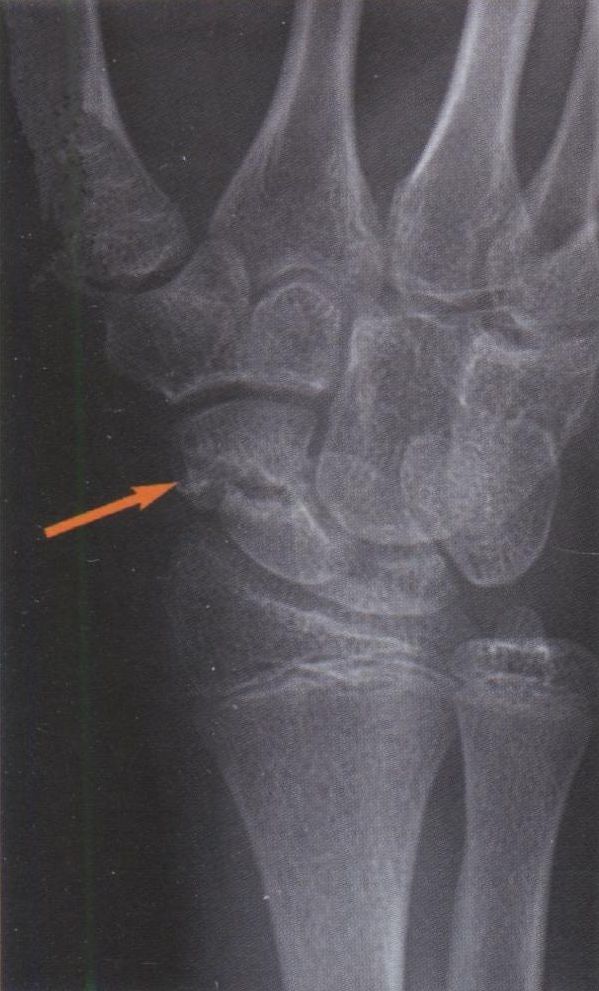
Рис. 7.6. Ладьевидная кость может быть подвержена перелому в период полового созревания.
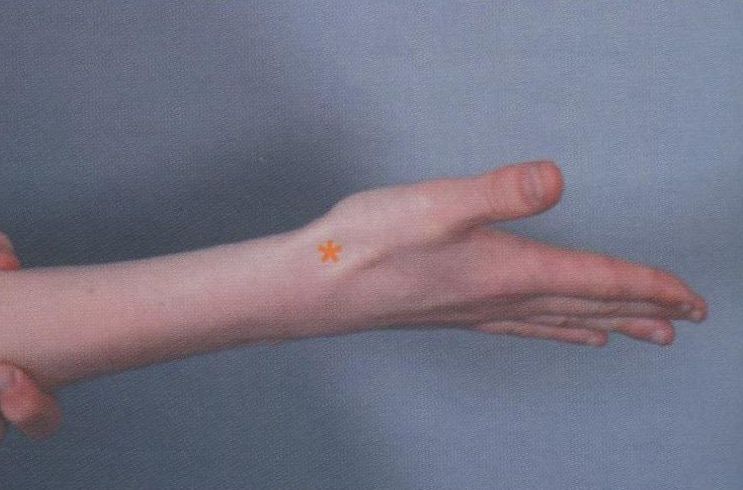
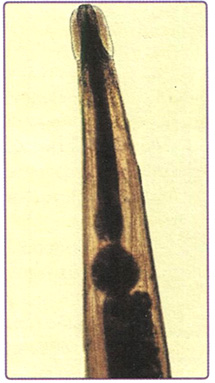
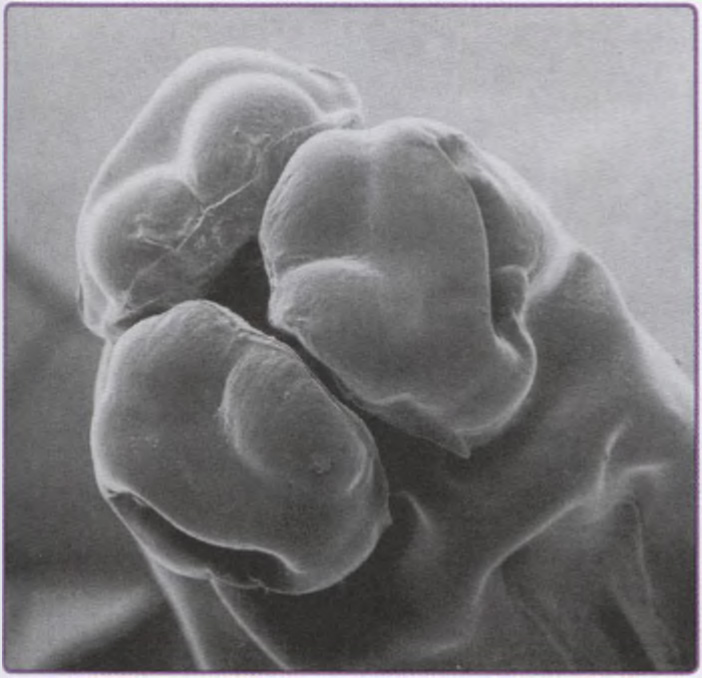
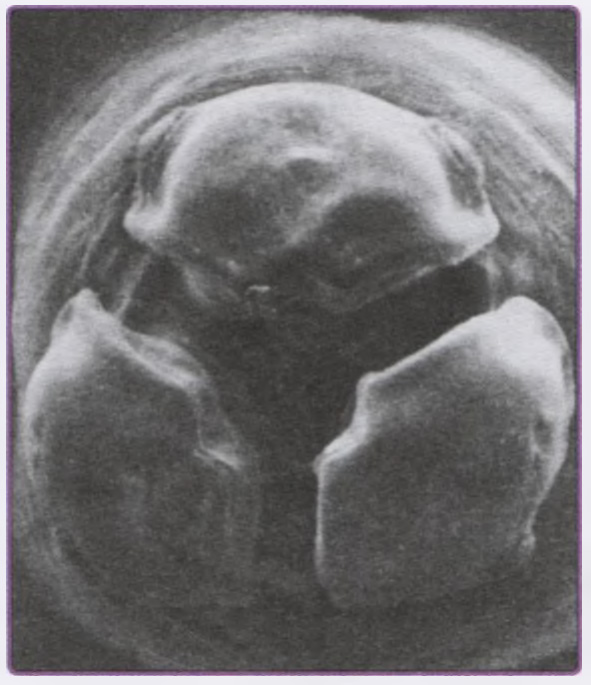
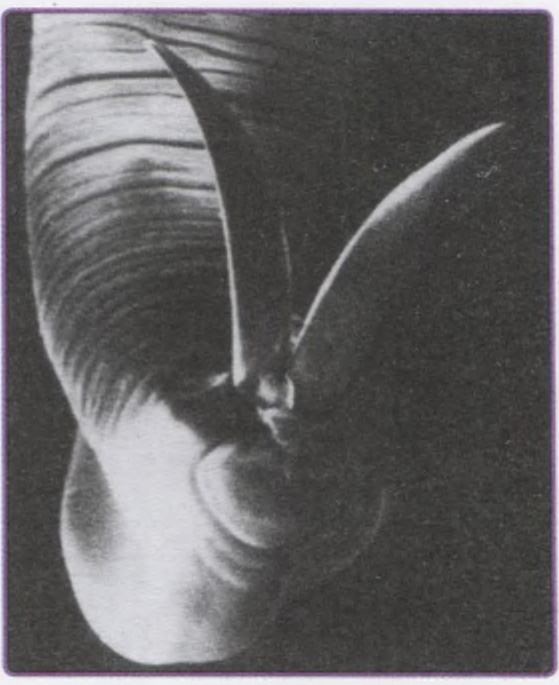
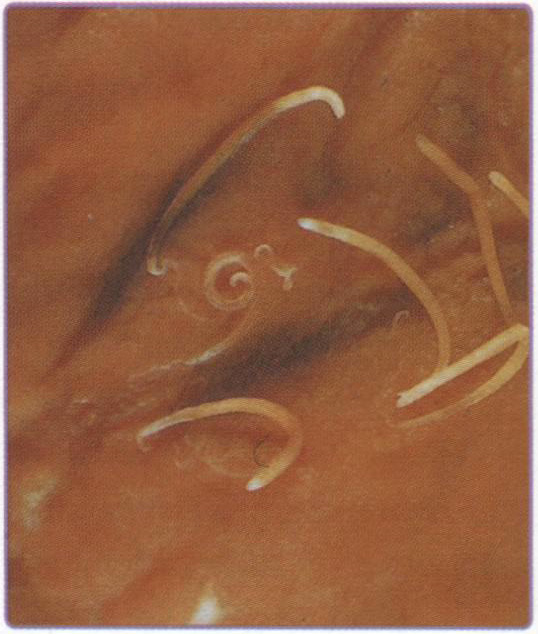
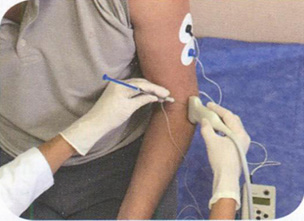
Рис. 7.7. Анатомическая табакерка представляет собой углубление на лучевой поверхности кистевого сустава между сухожилиями мышц длинного и короткого разгибателей большого пальца. Углубление отчётливо заметно при разогнутом суставе и отведении большого пальца (отмечено звёздочкой)
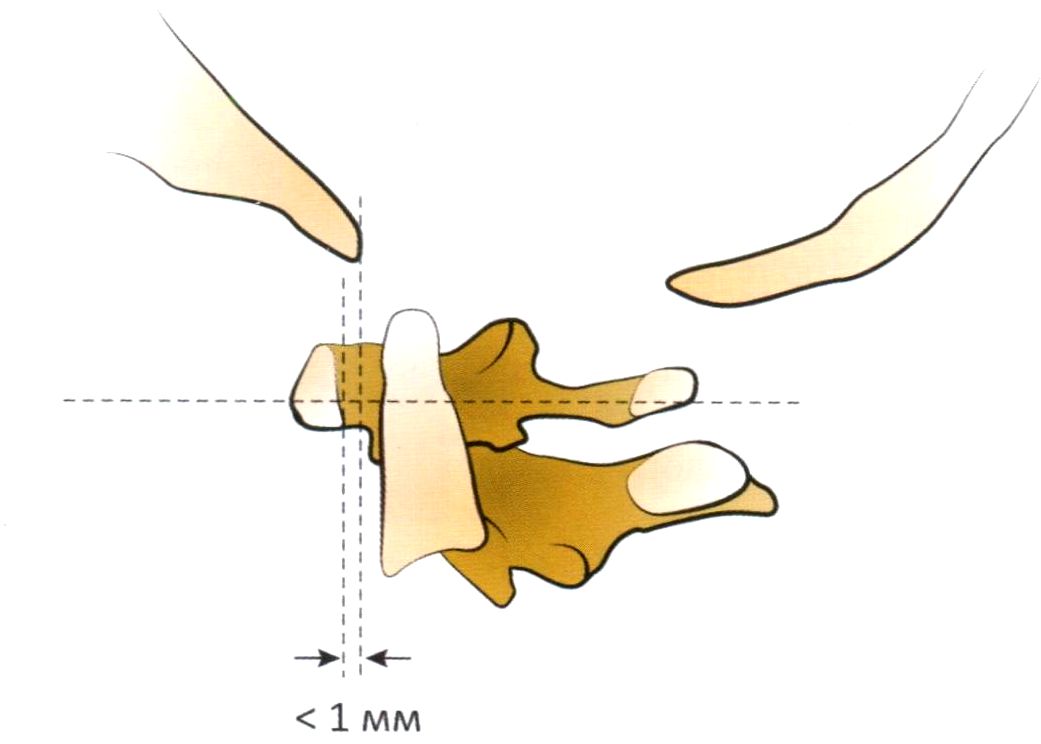
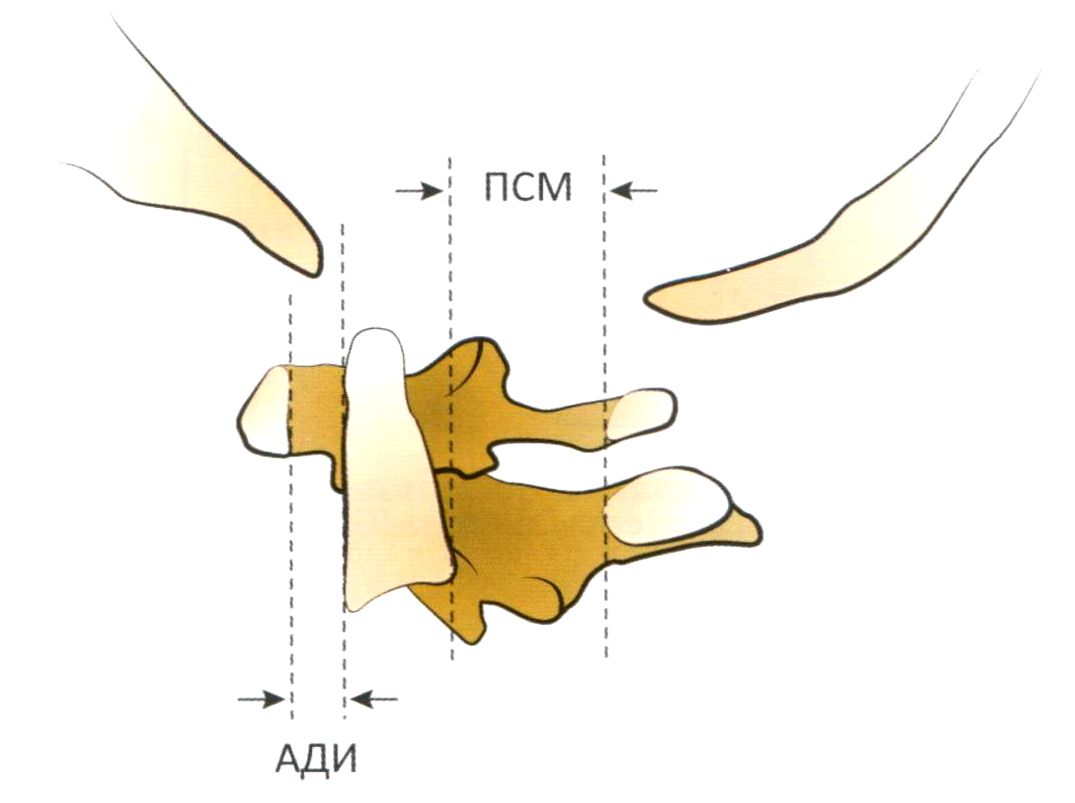
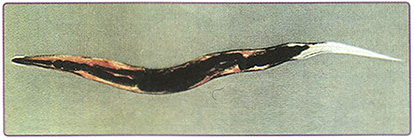
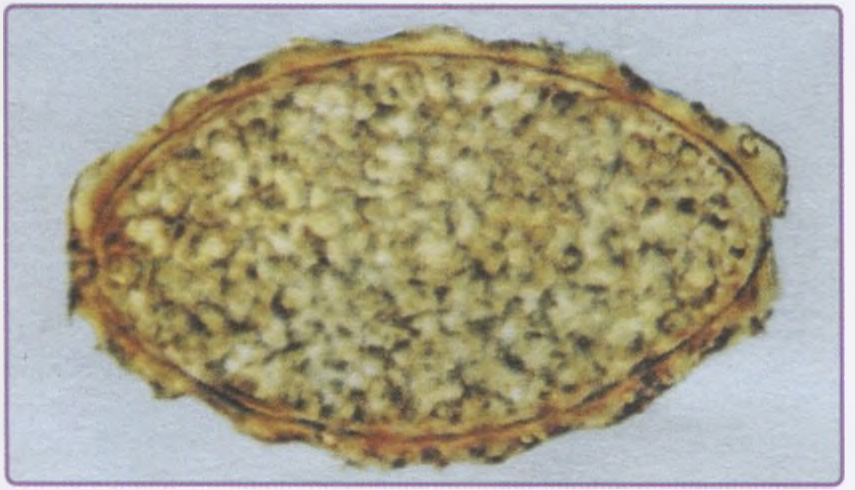
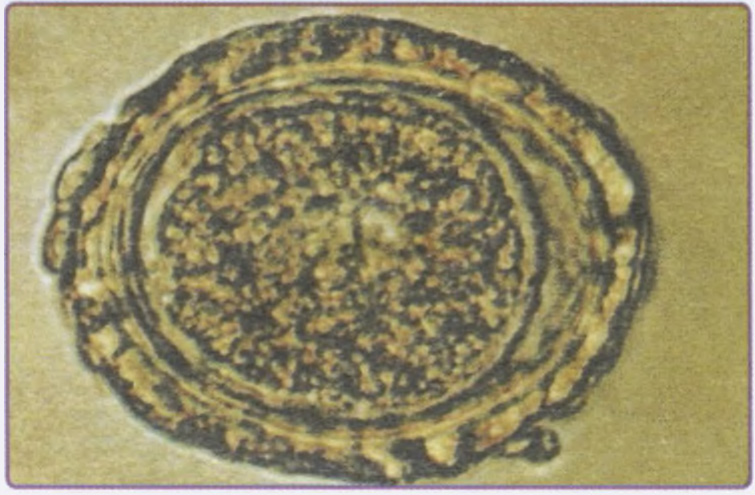
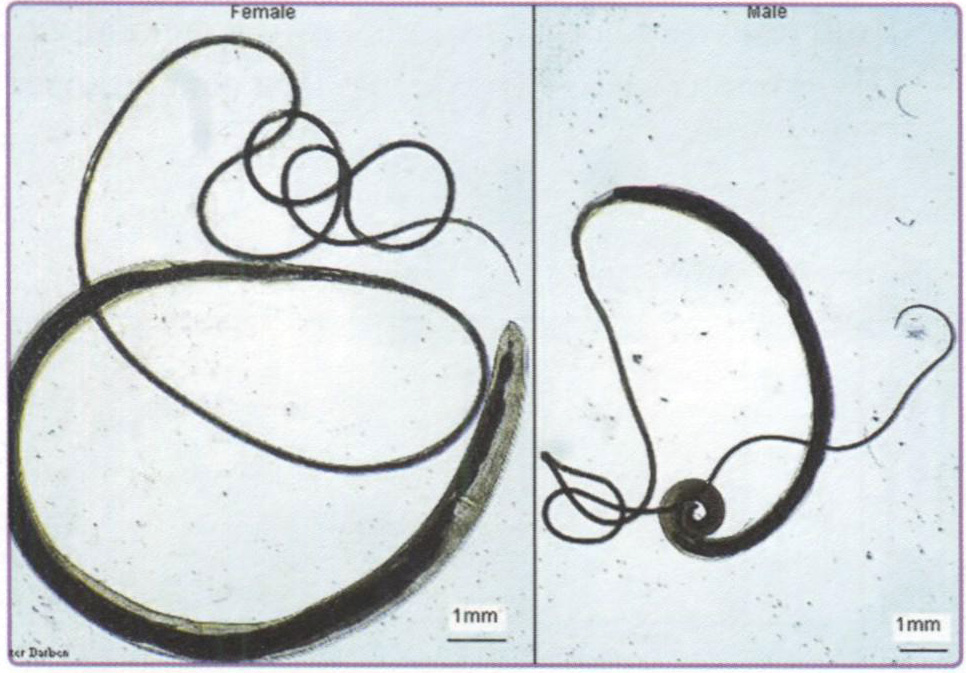
Недиагностированный перелом по типу «пряжки». Перелом по типу «пряжки» локализуется в дистальной части лучевой кости, непосредственно проксимальнее дистальной ростковой зоны. Такие переломы часто остаются незамеченными, поскольку в результате повреждения, для которого характерно вспучивание кортикального слоя, соосность не нарушается (рис. 7.8). Такой тип переломов также называют веретенообразным.
- Дополнительное обследование: рентгенография кистевого сустава в переднезадней и боковой проекциях. При подозрении на перелом ладьевидной кости необходимо выполнить рентгенографию кистевого сустава в соответствующей проекции (косая проекция в 3/4).
- Первичная медицинская помощь: не требуется.
- Когда направлять: при подозрении на перелом.
- Специализированное лечение: недиагностированный перелом ладьевидной кости. У детей переломы ладьевидной кости обычно заживают хорошо. Выбор метода лечения может склоняться в сторону гипсовой иммобилизации на срок от 6 до 12 недель, даже если перелом произошёл уже несколько месяцев назад.
Недиагностированный перелом по типу «пряжки». Консолидация перелома старше 3 недель уже завершена. При сохранении патологических проявлений можно применить гипсовую иммобилизацию на срок до 3 недель.
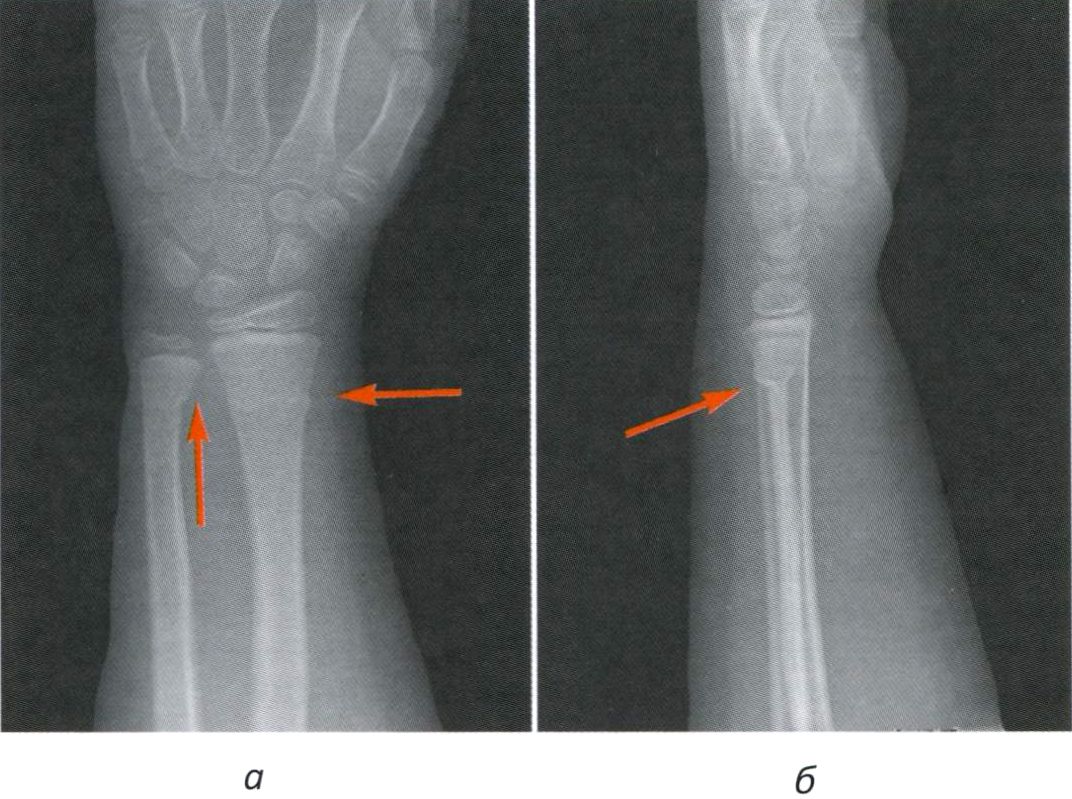
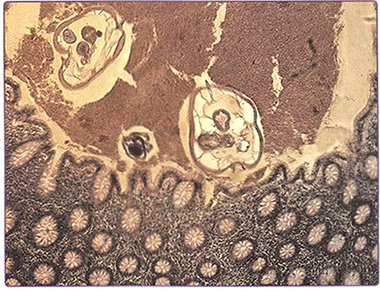
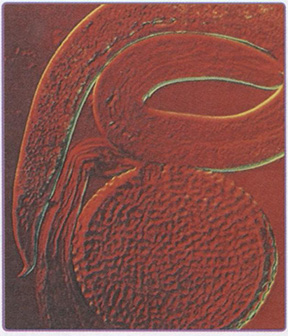
Рис. 7.8. Рентгенография кистевого сустава в переднезадней (а) и боковой (б) проекции: визуализируется перелом по типу «пряжки» в дистальном отделе лучевой кости (стрелки)
Выраженная болезненность в кистевом суставе с резким ограничением движений
- Жалобы: движения в кистевом суставе отсутствуют, состояние сопровождается выраженной болезненностью.
- Обследование: высокоинтенсивная боль в кистевом суставе.
- Дифференциальная диагностика:
- Острый остеомиелит
- Септический артрит
Пояснение, дополнительное обследование, принципы оказания первичной медицинской помощи, показания к направлению и особенности специализированного лечения смотрите в главе 18.
Дифференциальная диагностика: нарушение соосности кистевого сустава

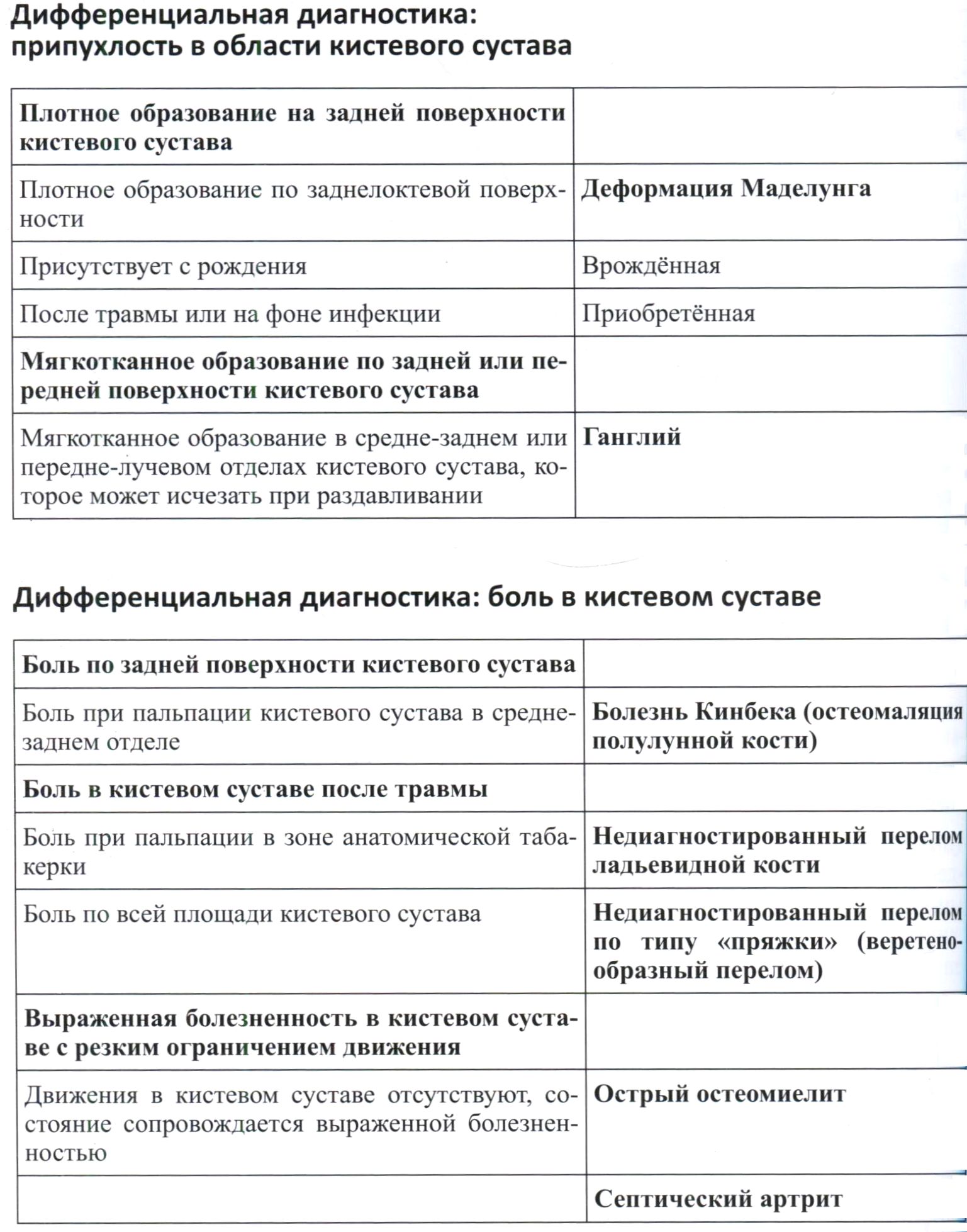
Дифференциальная диагностика: припухлость в области кистевого сустава.
Дифференциальная диагностика: боль в кистевом суставе
Вы читали отрывок из книги "Детская ортопедия" - Виссер Я. Д.
Дополнительный материал к лекции
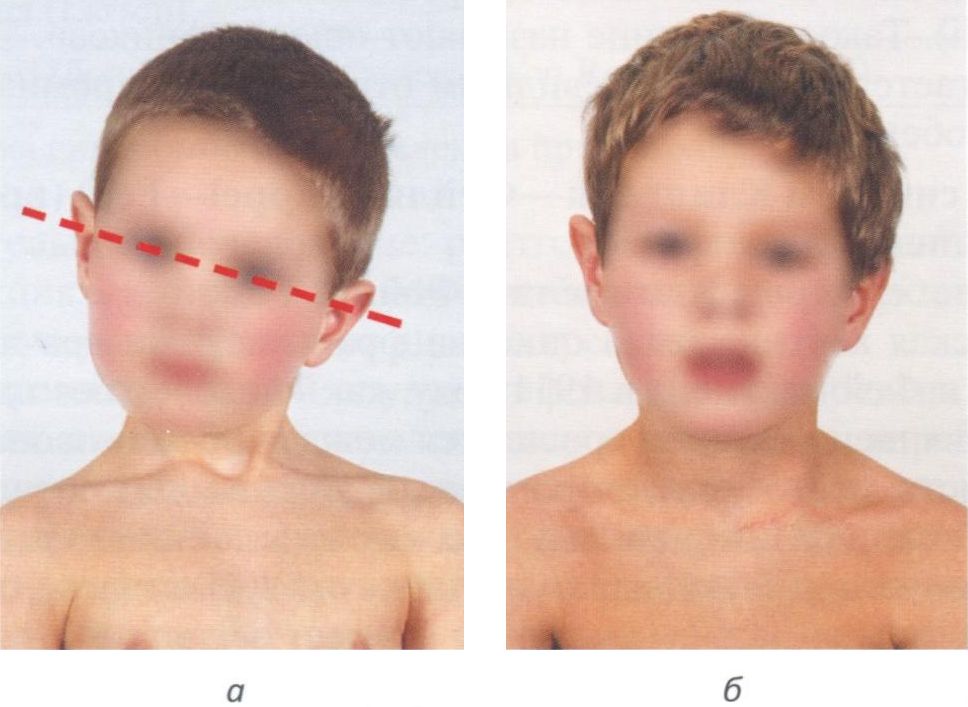
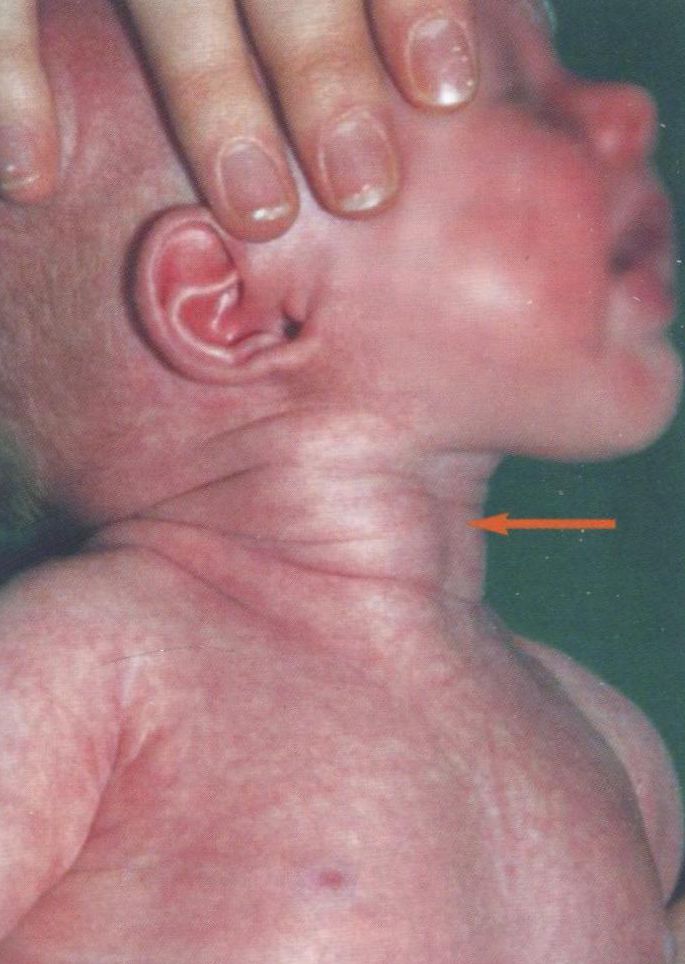
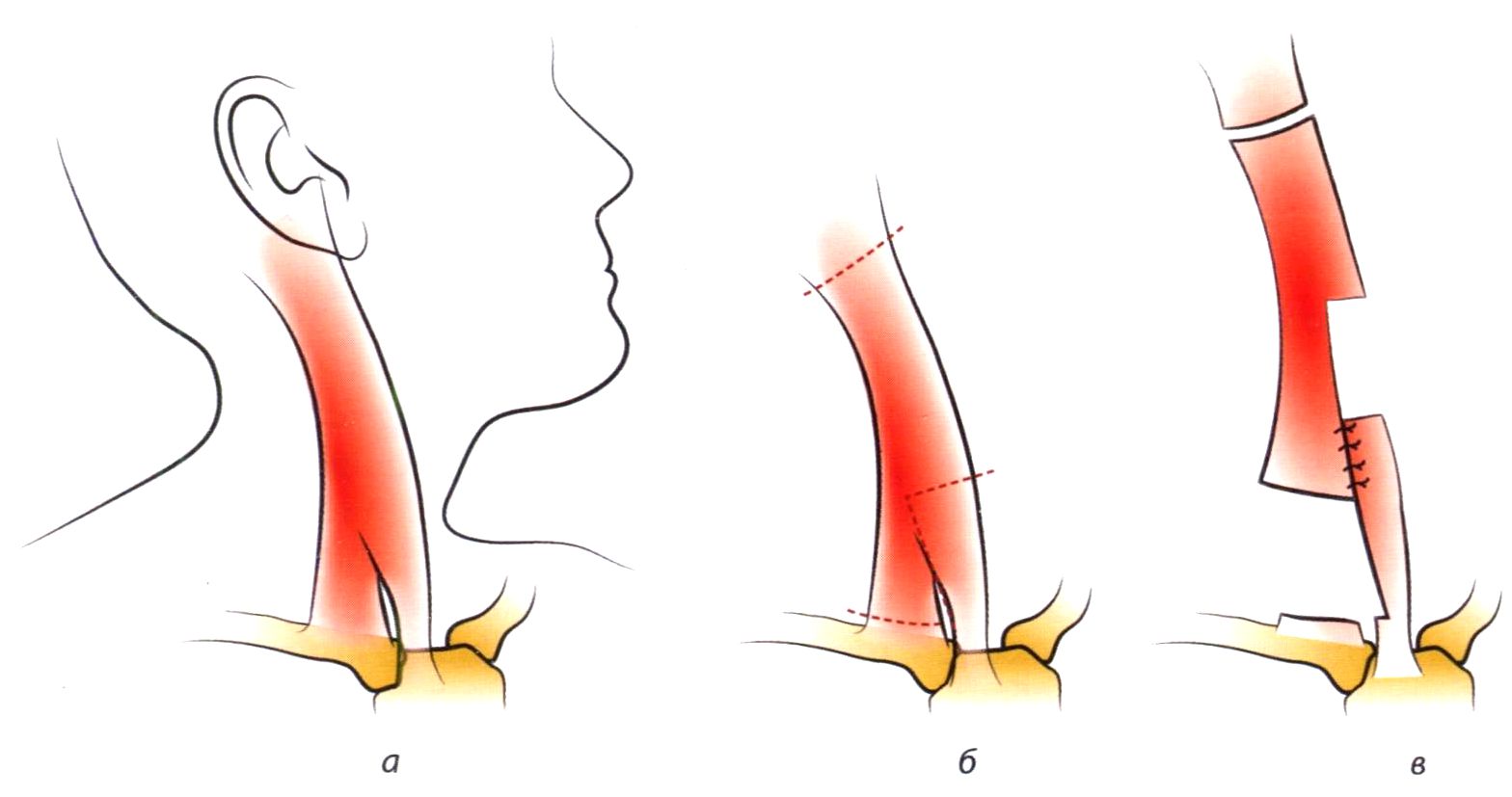
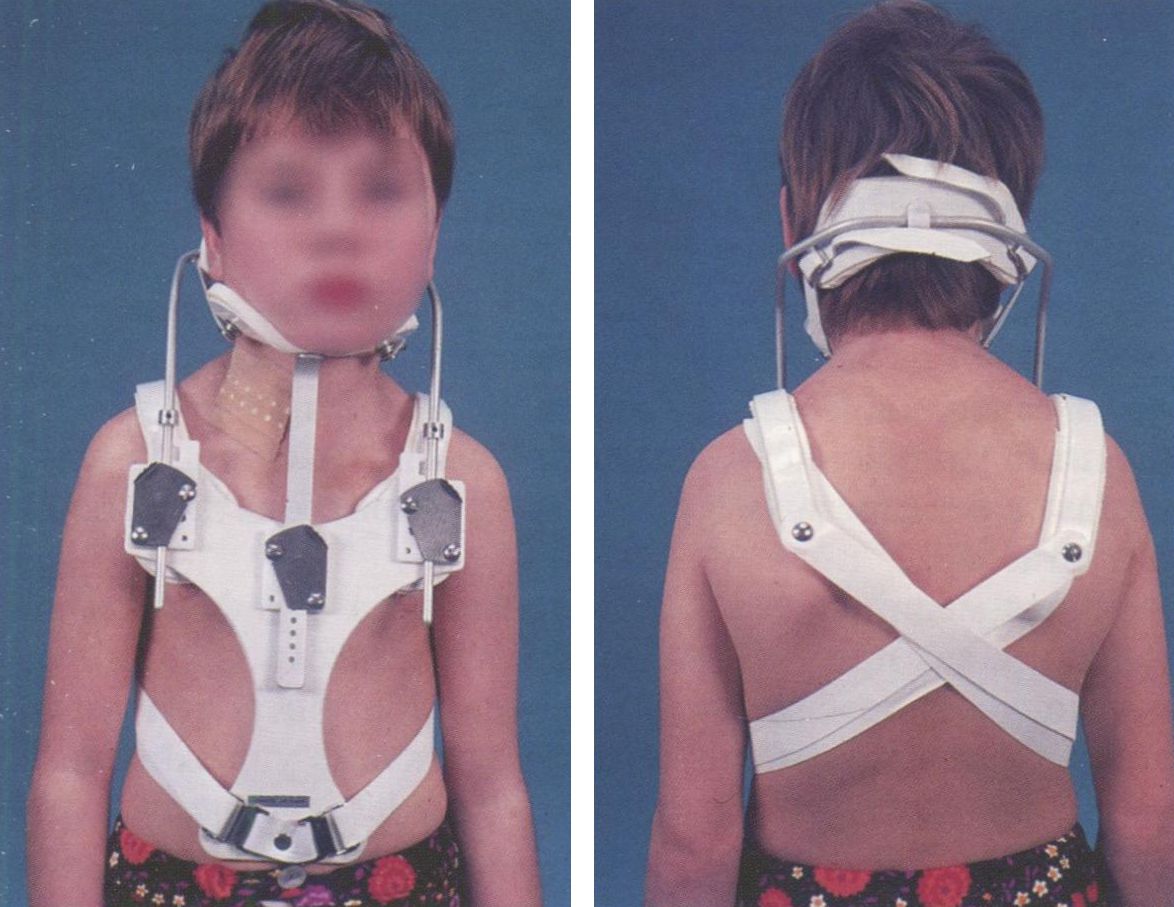
Кривошея у новорожденных: симптомы, диагностика, лечение
Боль в шее у ребёнка: синдром Гризеля, дисцит, подвывих
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru

Книга "Детская ортопедия"
Автор: Виссер Я. Д.
В книге представлены наиболее часто встречающиеся в практике врача ортопедические заболевания детского возраста. Подробно обсуждаются заболевания плечевого и локтевого суставов, а также предплечья, лучезапястного сустава и кисти. Отдельно рассматриваются инфекции костей и суставов, врождённые аномалии развития, деформации грудной клетки, заболевания тазобедренного и коленного суставов, а также патологические изменения голеностопного сустава и стопы. Кроме того, здесь уделено внимание заболеваниям спины и шеи, а также проблемам разновеликости и нарушений походки. В издании рассматриваются вопросы хирургических вмешательств, особенности ведения пациента и принципы консервативного лечения.
Таким образом, книга представляет собой диагностический инструмент при работе с любыми ортопедическими заболеваниями у детей, включая врождённые аномалии развития, и предназначена для детских ортопедов, педиатров, детских физиотерапевтов, реабилитологов, врачей общей практики, а также всех медицинских специалистов, интересующихся проблемами детской ортопедии.
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru
Содержание книги "Детская ортопедия" - Виссер Я. Д.
Глава 1. Стенка грудной клетки
Деформация стенки грудной клетки
Боль в области передней стенки грудной клетки
Глава 2. Шея
Деформация шеи
Сгибательная деформация шеи
Короткая шея
Кривошея
Боль в шее
Острая болезненная скованность с возможной кривошеей
Медленное развитие болезненной скованности с возможной кривошеей
Болезненная скованность и возможная кривошея с неврологическими проявлениями
Глава 3. Спина
Нарушение соосности позвоночника
Боковое искривление позвоночника
Патологическая круглая спина
Патологическая вогнутая спина
Комбинированные деформации
Боль в спине
Боль в спине, сопровождающаяся ночным потоотделением
Боль в спине с неврологическими проявлениями
Глава 4. Таз
Боль в области таза
Глава 5. Плечо
Аномалии плечевого пояса
Отсутствие ключицы
Высокое стояние лопатки
Повторяющиеся нетравматические подвывихи/вывихи плеча
Рецидивирующий посттравматический подвывих/вывих плеча
Припухлость в области плечевого сустава
Припухлость в области ключицы у новорождённых
Припухлость в области лопатки, ключицы или верхней части области плеча
Ограничение движений в плечевом суставе у новорождённых
Родовой паралич плеча
Боль в плече
Боль в плече неопределённого характера
Боль в плече после незначительной травмы
Боль в плече у спортсменов-метателей
Боль при движениях в плечевом суставе
Полное отсутствие движений в плечевом суставе на фоне значительно выраженной болезненности
Глава 6. Локтевой сустав и предплечье
Нарушение соосности локтевого сустава
Деформация локтевого сустава после перелома
Повторяющийся подвывих/вывих предплечья
Припухлость в области локтевого сустава
Припухлость по задней, передней или наружной поверхности локтевого сустава
Ограничение подвижности предплечья и локтевого сустава
Ограничение разгибания и/или сгибания в локтевом суставе после перелома
Ограничение подвижности предплечья
Боль в локтевом суставе
Боль по наружной стороне локтевого сустава после тяги за руку
Боль в наружном отделе локтевого сустава
Боль во внутреннем отделе локтевого сустава
Выраженная болезненность в локтевом суставе с резким ограничением движений
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru
Глава 7. Кистевой сустав
Нарушение соосности кистевого сустава
Крючковидная деформация кистевого сустава
Припухлость в области кистевого сустава
Плотное образование на тыльной поверхности кистевого сустава
Мягкотканное образование по задней или передней поверхности кистевого сустава
Боль в области кистевого сустава
Боль по тыльной поверхности кистевого сустава
Боль в кистевом суставе после травмы
Выраженная болезненность в кистевом суставе с резким ограничением движений
Глава 8. Кисть
Аномалии большого и трёхфаланговых пальцев
Добавочный большой или трёхфаланговые пальцы
Гигантизм большого и/или трёхфаланговых пальцев
Нарушение соосности трёхфаланговых пальцев
Укорочение трёхфаланговых пальцев
Сросшиеся трёхфаланговые пальцы и/или большой палец
Нарушение соосности большого пальца
Удлинение большого пальца
Укорочение большого пальца
Припухлость в области кисти
Глава 9. Тазобедренный сустав
Ограничение движений в тазобедренном суставе у новорождённых и младенцев
Ограничение движений в тазобедренном суставе кнаружи от средней линии тела
Ноги не сводятся вместе либо сводятся с перекосом таза
Переваливающаяся походка
Щёлкающее бедро
Боль в тазобедренном суставе
Боль в паховой области, в области таза или бедра
Боль в тазобедренном суставе и ограничение внутренней ротации
Боль в тазобедренном суставе и ограничение движений во всех плоскостях
Боль в тазобедренном суставе после незначительной травмы
Полное отсутствие движений в тазобедренном суставе на фоне значительно выраженной болезненности
Глава 10. Коленный сустав
Нарушение соосности коленного сустава
О-образное искривление ног
Х-образная деформация коленных суставов
Разгибательная деформация коленных суставов
Сгибательная деформация коленных суставов
Повторяющийся подвывих/вывих надколенника
Припухлость в области коленного сустава
Припухлость непосредственно выше и/или ниже коленного сустава
Припухлость в заднем отделе коленного сустава
Ограничение движений в коленном суставе
Ограничение разгибания в коленном суставе
Ограничение сгибания в коленном суставе
Выпот в коленном суставе
Выпот в коленном суставе через несколько часов после травмы
Выпот в коленном суставе в течение 24 часов после травмы
Выпот в коленном суставе без предшествующей травмы
Выпот в коленном суставе и поражение других суставов
Выпот в коленном суставе с ночным потоотделением
Боль в коленном суставе
Боль неопределённого характера непосредственно выше или ниже коленного сустава
Боль по внутренней или наружной стороне коленного сустава
Боль в переднем отделе коленного сустава
Боль в области бедра и коленного сустава
Полное отсутствие движений в коленном суставе на фоне значительно выраженной болезненности
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru
Глава 11. Голень
Нарушение соосности голени
Передненаружное искривление голени
Вальгусное искривление голени с антекурвацией
Боль в области голени
Боль высокой интенсивности в области голени
Боль по наружной стороне голени
Боль по внутренней стороне голени
Глава 12. Голеностопный сустав
Нарушение соосности голеностопного сустава
Прогрессирующее отклонение пятки кнаружи (вальгусная деформация)
Прогрессирующее внутреннее отклонение пятки (варусная деформация)
Боль в голеностопном суставе
Боль в переднем отделе голеностопного сустава
Боль в заднем отделе голеностопного сустава
Полное отсутствие движений в голеностопном суставе на фоне значительно выраженной болезненности
Растяжение связок голеностопного сустава
Глава 13. Стопа
Деформации стопы
Врождённые деформации стопы
Ходьба на носках
Уплощение продольного медиального свода стопы
Патологически высокий продольный медиальный свод стопы
Боль в стопе
Боль по наружной стороне заднего отдела стопы
Боль в пятке
Боль по внутренней стороне в проекции среднего отдела стопы
Болезненная припухлость в верхненаружном отделе пяточной области
Болезненная припухлость по внутренней стороне среднего отдела стопы
Безболезненная двусторонняя припухлость в медиальном отделе подошвенной поверхности стоп
Глава 14. Пальцы стоп
Аномалии пальцев
Добавочный палец
Гигантизм пальцев стопы
Сгибательная деформация пальцев
Перекрещивающиеся пальцы
Укорочение пальцев
Сращение пальцев
Медиальное отклонение большого пальца
Латеральное отклонение большого пальца
Медиальное отклонение мизинца
Боль в пальцах стопы
Боль и ограничение движений в большом пальце
Боль на уровне головки второй плюсневой кости (или третьей, или четвёртой, или пятой)
Боль в области ногтевой пластины
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru
Глава 15. Разновеликость ног
Укорочение или удлинение одной ноги
Укорочение одной ноги
Удлинение одной ноги
Глава 16. Нарушение походки
Введение
Нарушения походки
Хромота
Переваливающаяся походка
Ходьба на носках
Наружная установка стоп
Внутренняя установка стоп
Анталгическая походка с разгрузкой тазобедренного сустава
Походка с укорочением фазы опоры
Глава 17. Врождённые пороки развития конечностей и позвоночника
Общие положения
Классификация
Частота
Верхняя конечность
Полное или частичное отсутствие верхней конечности
Полное отсутствие верхней конечности либо отсутствие плеча или предплечья между туловищем и кистью наряду с локтевым суставом
Аномалии предплечья и/или кисти
Нижняя конечность
Полное или частичное отсутствие нижней конечности
Полное отсутствие нижней конечности либо отсутствие бедра или голени между туловищем и стопой наряду с коленным суставом
Укорочение бедра, коленный сустав всегда сохранён
Аномалии голени и/или стопы
Спина
Поза Будды
Глава 18. Инфекции костей и суставов
Полное отсутствие движений в конечности на фоне значительно выраженной болезненности
Частота
Патогенез острого остеомиелита
Патогенез септического артрита
Локализация
Другие локализации
Патогены
Поздние осложнения
Купить книги по ортопедии в интернет-магазине медицинской книги shopdon.ru