Водно-электролитный обмен и его нарушения в организме человека. Лекция для врачей
Отрывок из книги "Водно-электролитный обмен и его нарушения: руководство для врачей"
Водно-электролитный обмен
Водно-электролитный обмен в организме человека включает в себя сопряженные процессы потребления, всасывания, распределения во внутренней среде, обмена между внутренней средой и клетками, выделения из нее воды и электролитов. Физиологически оптимальная активность водно-электролитного обмена обеспечивает постоянство осмотической концентрации частиц (осмотический гомеостаз), ионного состава (ионный гомеостаз), кислотно-основного равновесия, объема жидкостей (объемный гомеостаз) в обособленных, но взаимосвязанных компартментах внутренней среды организма. Водно-электролитный баланс обеспечивается различными молекулярными структурами клеток, которые посредством регуляторных механизмов интегрируются в единую систему с другими видами обмена и физиологическими процессами в самих клетках, различных органах, организме в целом. При неотложных состояниях расстройства водно-электролитного обмена, как правило, не первичны, но, возникнув на фоне других нарушений, они требуют первостепенного лечения. Варианты хронических расстройств водно-электролитного обмена не всегда очевидны без проведения лабораторной диагностики. Например, в ряде случаев гипертонической болезни первичны нарушения водно-натриевого баланса, приводящие к увеличению массы циркулирующей крови и, как следствие, — к увеличению минутного объема сердца и повышению артериального давления. Снижение артериального давления может быть достигнуто лишь фармакологическими средствами, устраняющими первичную причину болезни — нарушения баланса воды (см. «Нарушения регуляции обмена воды»). Иными словами, состояние водно-электролитного обмена является базисом, негативные изменения которого способны сами по себе привести организм к фатальным последствиям. Адекватное лечение водно-электролитных нарушений содействует успешному проведению этиопатогенетической терапии основного заболевания.
Современная система показателей лабораторной диагностики нарушений водно-электролитного обмена позволяет разобраться в характере и степени этих нарушений и провести их рациональную терапию. Ниже приведены современные представления о молекулярных основах водно-электролитного обмена и принципах его лабораторного контроля в клинической практике.
Купить книгу "Водно-электролитный обмен и его нарушения: руководство для врачей"
Вода и электролиты (вводные понятия)
Вода — незаменимый, обязательный компонент функционирования любой биологической системы, составляющие которой в той или иной степени зависимы от химических и физических свойств как отдельных молекул воды, так и образуемых ими надмолекулярных структур. Содержание базовых биохимических и физиологических процессов, их количественный аспект (например, освобождение энергии в реакциях биологического окисления) требуют точных знаний химического состава молекулы воды, закономерностей ее образования.
Впервые разложение воды на водород и кислород электрическим током выполнили в 1800 г. английские ученые У. Николсон и А. Корлайль. Однако более определенные данные по химическому составу воды были получены несколько позже, в 1805 г., Ж. Л. Гей-Люсаком и А. Гумбольтом, показавшими, что для ее образования необходимы два объема водорода и один объем кислорода. Позднее Ж. Б. Дюма (1843) нашел точные весовые отношения между водородом и кислородом в молекуле воды. Химический символ воды 1-120 был принят на конгрессе химиков в Карлсруэ в 1860 г. В 1931 г. Г. Юри сделал сообщение об открытии тяжелого изотопа водорода — дейтерия (D). В 1933 г. два американских ученых Г. Льюис и Р. Макдональд впервые выделили з природной воды практически чистую дейтериевую воду — D20.
Воду, состоящую из дейтерия и кислорода, стали называть тяжелой водой. После открытия сверхтяжелого изотопа водорода трития (Т) была обнаружена сверхтяжелая вода. В 1980-е годы искусственно были получены изотопы водорода терций (4H) и квинтий (5 Н). С учетом существования различных изотопов кислорода возможно образование 8 разновидностей воды, из которых 39 радиоактивны и всего лишь стабильны. Разновидности воды с изотопами водорода терцием (4Н) квинтием (5 Н) в природе не встречаются. В физиологических процессах используется только одна ее разновидность — протиевая вода (Н2O).
Многообразие свойств воды и необычность их проявления в значительной степени определяются физическими свойствами молекулы воды. В отдельной молекуле воды ядра водорода и кислорода расположены относительно друг друга так, что образуют равнобедренный треугольник со сравнительно крупным ядром кислорода на вершине и двумя мелкими ядрами водорода у основания. В молекуле воды имеются четыре полюса зарядов: два отрицательных за счет избытка электронной плотности у кислородных пар электронов и два положительных — вследствие недостатка электронной плотности у ядер водорода — протонов. Такие особенности сочетания группировки атомов в молекуле воды с распределением заряда позволили говорить о ней как о биполярной частице, или диполе воды (рис. 1).
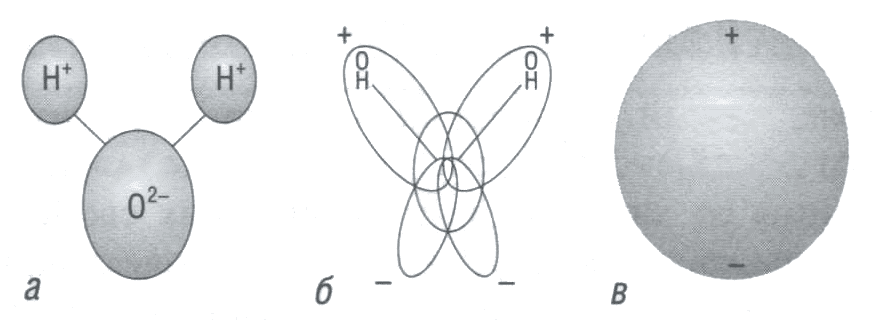
Рис. 1. Молекула воды: а — схема взаимного расположения водорода (Н 2-) и кислорода (0 2-) в молекуле воды; б — характер распределения зарядов в молекуле воды; в — молекула воды как физическая частица — диполь воды
Благодаря упорядоченным по месту избыточным зарядам молекулы воды способны связываться между собой в относительно устойчивую надмолекулярную структуру (рис. 2). На основании результатов изучения структур, образуемых взаимодействующими молекулами воды в различных условиях, сделаны выводы об их способности формировать микрокристаллы. Микрокристалл из молекул воды похож на фигуру, которая возникает при растяжении куба за два противоположных угла. Куб принимает форму ромбовидного многоугольника. Микрокристалл из молекул воды имеет размеры 2х2х3 нм. В обычном, жидком состоянии при температуре от 0 до 100о С вода состоит из таких или подобных структурных элементов, в каждом из которых содержится 912 молекул. Микрокристаллы воды, в свою очередь, объединены в более крупные образования - ячейки размером 0,5 мкм (микрометр тысячная доля миллиметра), которые можно видеть в контрастно-фазовом микроскопе.
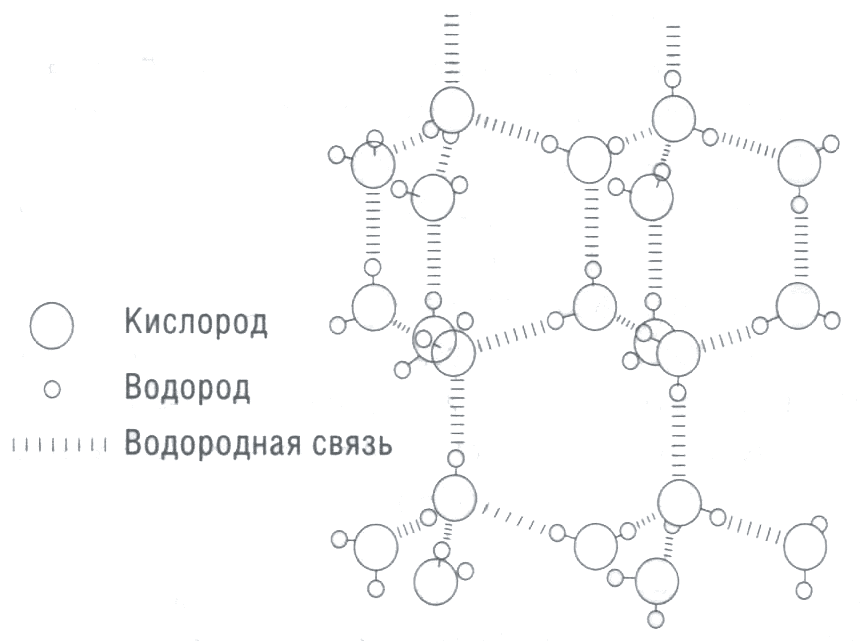
Рис. 2. Надмолекулярная структура воды, формируемая молекулами за счет водородных связей: молекула воды посредством водородных связей способна одновременно в равной степени взаимодействовать с четырьмя другими молекулами воды
Микрокристаллическая структура воды претерпевает определенные трансформации в растворе, то есть при внесении в воду различных веществ, вступающих с ее молекулами в физико-химические взаимодействия. Структурные элементы из молекул воды в цитоплазме клеток (внутриклеточный раствор), исследованные в определенных условиях, напоминают снежинку и получили название кластеров. Вопрос о том, являются ли кластеры универсальной структурной единицей организации воды в клетках и внутренней среде организма, остается открытым.
Трансформации микрокристаллической структуры воды в растворе возникают при физических и физико-химических воздействиях — инфракрасном, рентгеновском облучении, воздействии ультра- и инфразвуком, изменении редокс-потенциала, концентрации ионов водорода, электролитов, различных органических соединений.
В биологических растворах (цитоплазма, интерстициальная жидкость, лимфа, плазма крови и др.) редокс-потенциал, рН, концентрации электролитов и ряда органических соединений являются постоянными контролируемыми величинами, что указывает на свойственную биологическим растворам определенную структурную организацию молекул воды. Если учесть, что микрокристаллическая структура воды предопределяет четкий порядок перемещения ее молекул между клеточными структурами, клеточными структурами и внеклеточной средой, внеклеточной средой и внешней средой, постоянные контролируемые параметры биологических растворов поддерживают, в свою очередь, устойчивый характер этого обмена. Перемещение молекул в растворе позволяет им реализовать в биологических системах целый ряд свойств, определяющих функции воды в организме.
В частности, молекулы воды, точнее, ее диполи, способны взаимодействовать не только между собой, но и с молекулами и атомами других веществ и соединений. Под воздействием диполей воды на поверхности погруженных в нее веществ межатомные и межмолекулярные силы ослабевают в 80 раз. Столь сильное влияние на межмолекулярные и межатомные взаимодействия других веществ, присущее только воде, объясняет ее способность быть универсальным растворителем, «помогая» контактирующим с ней молекулам распадаться на ионы (например, различным солям — NaCl Na+ + СI-), сама вода проявляет большую устойчивость. Из 1 млрд молекул воды диссоциированными при комнатной температуре оказываются лишь две. Вода сама химически не изменяется под действием большинства тех соединений, которые она растворяет, а также не изменяет их. Это характеризует ее как инертный растворитель, что важно для живых организмов на нашей планете, поскольку необходимые их клеткам питательные вещества поступают в водных растворах в сравнительно устойчивом виде.
Определенные свойства как отдельных молекул воды, так и надмолекулярных образований лежат в основе физиологических функций воды в организме.
Вода выполняет в организме следующие физиологические функции:
- является структурной основой оптимального физиологически активного объема клетки и внутренней среды организма;
- определяет структурную упорядоченность биомолекул;
- обеспечивает субстратную специфичность действия ферментов;
- выступает в качестве субстрата в ряде ферментативных реакций;
- формирует направленный поток веществ внутри клетки;
- является транспортной средой при обмене веществ между клетками, между внешней средой и внутренней средой, между внутренней средой и клетками;
- участвует в процессах терморегуляции;
- играет роль гемодинамического фактора в работе сердечно-сосудистой системы.
Поступая в организм человека извне, в основном через желудочно-кишечный тракт, молекулы воды пребывают в постоянном движении. Они перемещаются в составе растворов в обособленные мембранами пространства, в итоге покидая организм через канальцевую систему почек, различные железы внешней секреции, легкие, кишечник (рис. 3).
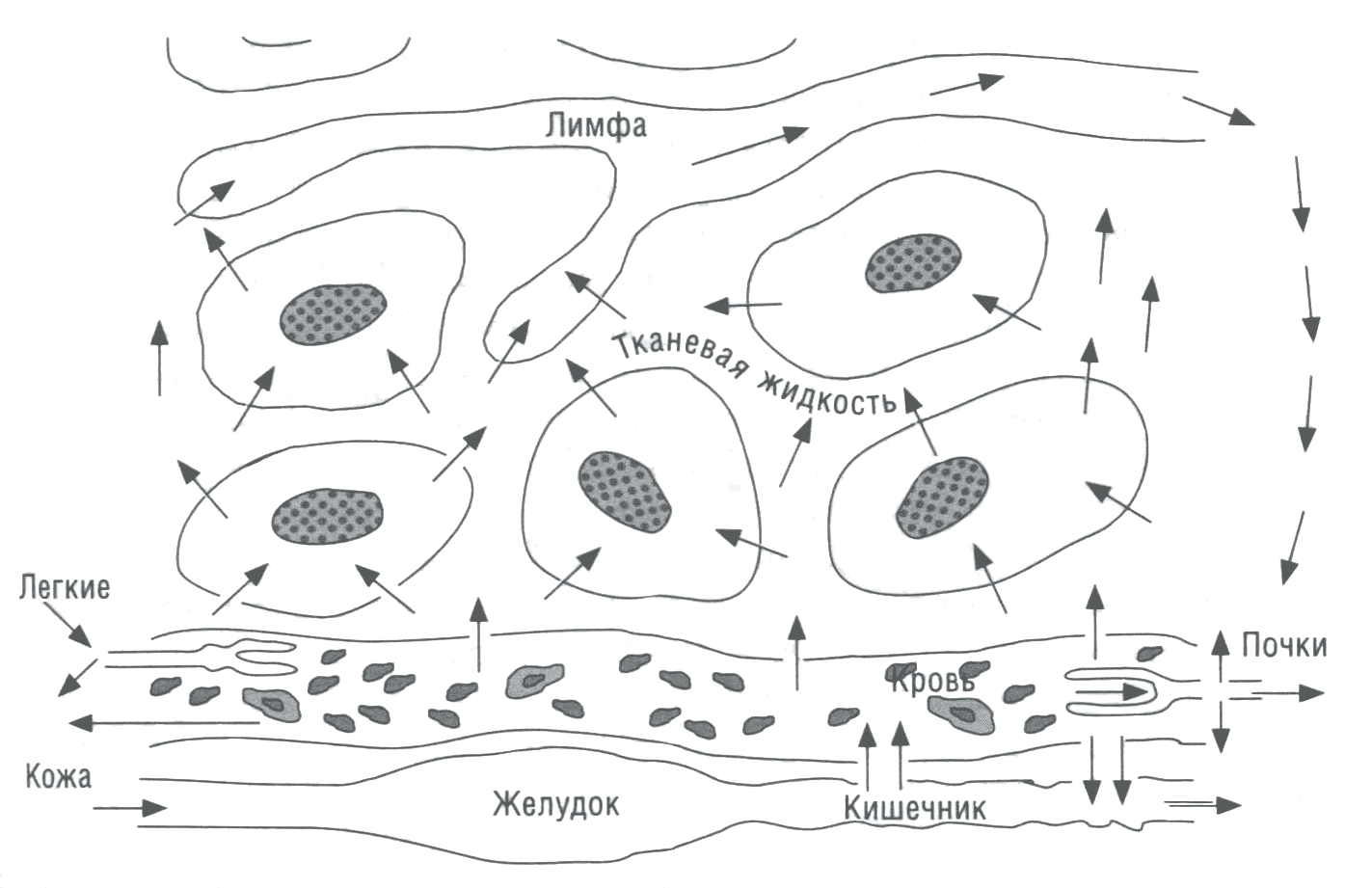
Рис, 3. Перемещение воды по обособленным мембранами пространствам организма, ее обмен между ними и внешней средой
Перемещение молекул воды из одного пространства в другое, включая и поступление извне через желудочно-кишечный тракт, и удаление через канальцевую систему почек, различные железы внешней секреции, межклеточные контакты, тесно сопряжено с перемещением электролитов, являющихся неотъемлемыми компонентами водных растворов организма. К электролитам относят молекулы солей, кислот, оснований, органических соединений, которые в водном растворе в той или иной степени ионизированы. В зависимости от характера ионизации электролиты делят на катионы и анионы.
Важнейшие тестируемые индикаторные катионы внутренней среды организма — ионы натрия (Na+), калия (К+), кальция (Са2+) и магния (Mg2+). Тестируемым катионом является и ион водорода Н+ , биохимические и патобиохимические аспекты обмена которого рассматриваются отдельно вследствие его особого, относительно самостоятельного положения в биологических системах. Нарушения обмена ионов водорода предопределяют острые расстройства обмена других электролитов, тогда как обратные влияния имеют менее существенный характер.
Важнейшими тестируемыми индикаторными анионами внутренней среды организма являются ионы хлора хлора (СI -), гидрокарбоната (НСОз-),
фосфатов (НРО42- , Н2РО4-), сульфата (S042- ). К анионам также относят радикалы органических кислот — ацетат, пируват, лактат, бета-гидроксибутират, ацетоацетат. Совокупность электролитов и других частиц в жидкостях внутренней среды, как и в любых других растворах, придает им свойства, не зависящие от химической природы частиц или их способности участвовать в тех или иных биохимических и физиологических процессах. Поскольку такие свойства обусловлены коллективным влиянием растворенных частиц, их принято называть коллигативными — от латинского colligams, что означает «собирать». К числу коллигативных свойств относятся понижение давления паров над раствором, понижение температуры замерзания растворов по сравнению с растворителем, осмотическое давление. Для количественной характеристики всей суммы частиц пользуются показателем осмолярности, отражающей суммарную концентрацию частиц в 1 л воды. Осмотическое давление раствора проявляется при разделении раствора и растворителя или растворов разной концентрации мембраной, проницаемой лишь для молекул растворителя. Осмотические силы, создаваемые разностью осмотических давлений раствора и растворителя или двух растворов, предопределяют движение молекул растворителя в сторону раствора с большей концентрацией осмотически активных частиц. Осмотическое равновесие будет достигнуто при выравнивании концентрации соли в растворах, разделенных полупроницаемой мембраной, и сопровождается увеличением объема раствора, в котором концентрация соли исходно была выше.
Структуры, разделяющие компартменты биологических растворов, обладают свойствами полупроницаемых мембран, пропускающих не только молекулы воды, но и вещества с большей молекулярной массой, за исключением белков. В этой связи для биологических растворов важной характеристикой является давление, обусловленное белками, — коллоидно-осмотическое (онкотическое). Ограниченная способность белков к перемещению в пределах компартментов внутренней среды, их различная концентрация в этих компартментах, а значит, и связанное с ними коллоидно-осмотическое давление важны для направленного движения воды в организме (подробнее см. в разделе «Осмос, тоничность, осмолярность»). Связанный с белками заряд (в биологических средах отрицательный) предопределяет характерный электролитный состав взаимосвязанных биологических растворов. Разность концентраций электролитов в жидкостных пространствах обусловлена характером взаимодействия биологических пространств организма, разделенных ограниченно проницаемыми мембранами для молекул пептидной природы — высокомолекулярных электролитов.
Концентрация белков в интерстициальной жидкости составляет 4 г/л, в лимфе — 39 г/л, в плазме — 66—80 г/л, во внутриклеточном пространстве — 150 г/л. Разность концентраций белков соответственно определяет и разность ассоциированных с ними избыточных отрицательных зарядов. А это значит, что сохранение электронейтральности растворов в жидкостных пространствах достигается перераспределением низкомолекулярных отрицательно заряженных электролитов, главным образом ионов хлора и бикарбоната (эффект Гиббса—Доннана).
Распределение и нормальное содержание электролитов в индикаторных жидкостях внутренней среды и цитоплазме клеток приведено на рис. 4.
Значительные различия в количественном распределении отдельных электролитов между внутри- и внеклеточной жидкостями обусловлены не только отличиями в способности разных ионов перемещаться между ними через биологические мембраны. Так, преобладающие во внеклеточной жидкости ионы натрия, хлора и гидрокарбоната, а во внутриклеточной — калия, магния, фосфатов и сульфата сопоставимы по способности проникать через цитоплазматическую мембрану клеток. Однако регулируемая проницаемость ионных каналов в цитоплазматической мембране в сочетании с функционирующими в ней АТФ-зависимыми транспортными механизмами противостоят стремлению различных ионов к равномерному распределению во взаимосвязанных через цитоплазматическую мембрану растворах.
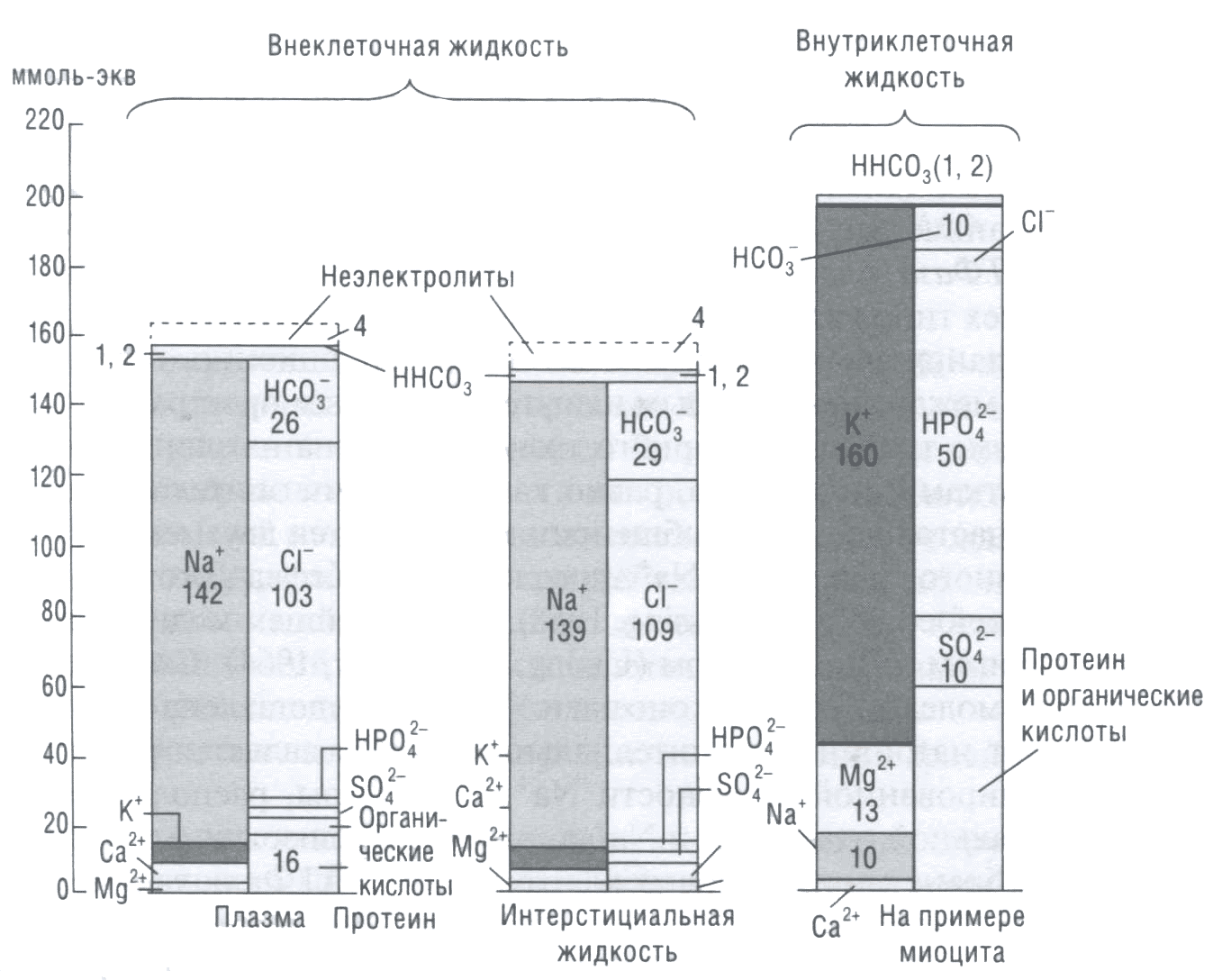
Рис. 4. Распределение и нормальное содержание электролитов в индикаторных жидкостях внутренней среды и цитоплазме клеток
Парацеллюлярный перенос электролитов всегда является пассивным процессом — это их диффузия (конвекция) через межклеточные промежутки в направлении электрохимического или концентрационного градиента. Парацеллюлярное движение электролитов посредством диффузии сочетается с их переносом межклеточным током воды (следование за растворителем) под действием осмотических или гидростатических сил. Всасывание воды и минеральных солей парацеллюлярным путем весьма существенно в проксимальных отделах кишечника, канальцевой системе почек. Движущие силы парацеллюлярного перемещения электролитов формируются в результате их трансцеллюлярного транспорта.
Трансцеллюлярный перенос электролитов возможен благодаря работе Na+ К+-АТФазы, функциональная активность которой тесно связана с работой ионных каналов и системой активного транспорта органических и неорганических ионов.
Na+, К+-АТФаза является ключевым белком цитоплазматической мембраны всех типов клеток, осуществляющим освобождение энергии АТФ для создания электрохимического и концентрационного градиентов Na+и К+ между внеклеточным и внутриклеточным пространствами.
В механизме трансцеллюлярного транспорта иона натрия эпителиальными клетками кишечника, равно как и другими эпителиальными клетками, в настоящее время общепринятой является двухмембранная модель активного транспорта Na+, предложенная Кефед-Джонсеном и Уссингом (koefoed-Johnsen, Ussing, 1958) и в дальнейшем модифицированная Уссингом и Виндхагером (Ussing, Wmdhager, 1964). Схема двухмембранной модели Кефед-Джонсена и Уссинга представлена на рис. 5.
Транспорт натрия через эпителиальные клетки является результатом координированной активности Na+, К+-АТФаза, расположенной на базолатеральной мембране, и Na+-каналов, локализованных на апикальной мембране эпителиальных клеток. Na+, К+-АТФаза, удаляющая натрий из клеток за счет освобождения энергии АТФ, поддерживает его низкую внутриклеточную концентрацию, что создает возможность его перемещения через натриевые каналы и систему активного транспорта апикальной мембраны в цитозоль по концентрационному градиенту.
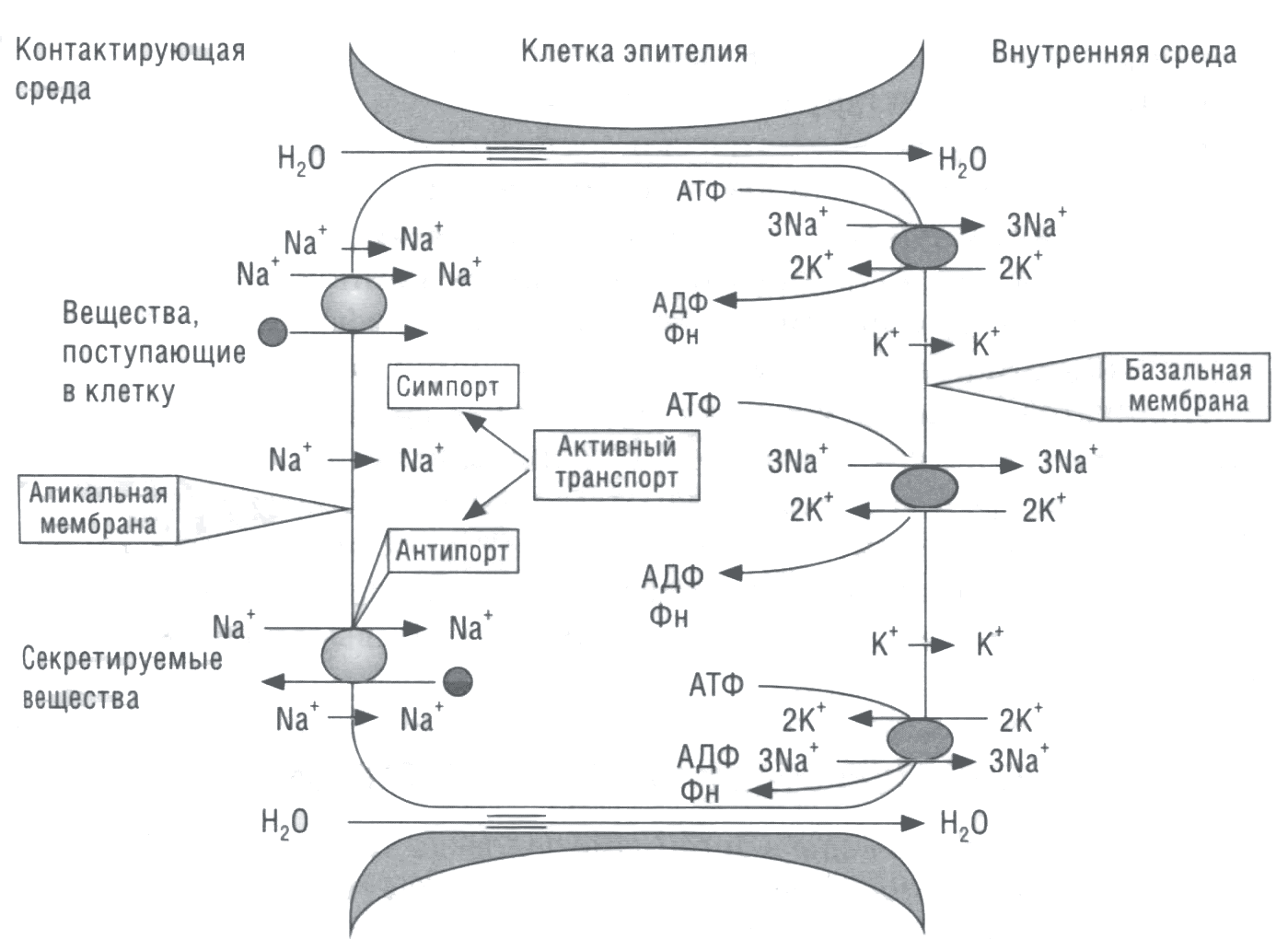
Рис. 5. Двухмембранная модель транспорта натрия в эпителии: АДФ — аденозиндифосфат; ФН — неорганический фосфат
Калий, поступающий в клетку благодаря работе Na+ К+-АТФазы, удаляется по калийселективным каналам базолатеральной мембраны за счет электрохимического градиента. Вследствие процессов направленного транспорта натрия и калия в микроокружение клетки со стороны базолатеральной мембраны их количество возрастает, создавая осмотический и электрохимический градиенты относительно внеклеточного микроокружения со стороны апикальной мембраны. Осмотический и электрохимический градиенты являются движущей силой парацеллюлярного перемещения воды и различных ионов.
Электролиты выполняют в организме следующие физиологические функции:
- предопределяют надмолекулярную организацию структуры воды, упорядоченный характер перемещения молекул воды между клетками и внутренней средой, внутренней и внешней средами;
- отвечают за осмолярность жидкостей тела;
- образуют биоэлектрический потенциал;
- катализируют процессы обмена веществ;
- определяют реальный РН жидкостей тела;
- упрочняют структуру костной ткани; формируют депо биологически доступной формы энергии;
- участвуют в процессах свертывания крови;
- обладают иммуномодулирующей активностью;
- являются структурно-функциональным компонентом системы регуляции активности пролиферативных, дифференцировочных и апоптотических процессов в клетках организма.
Индикаторными жидкостями внутренней среды, по содержанию электролитов в которых судят о сбалансированности их обмена, являются цельная кровь, плазма (сыворотка) крови, цитозоль эритроцитов. Полнота оценки обмена воды и электролитов достигается при дополнительном изучении их содержания в моче. Концентрацию электролитов в Международной системе единиц (СИ) выражают в мэкв/л и ммоль/л.
Характеристика жидкостей организма
Общее количество воды в организме человека зависит от количества жировой ткани, в которой ее содержание составляет около 3070. В «обезжиренном теле» (с учетом 1070 липидов, участвующих в построении морфологических структур клеток) количество воды достигает 72—73%. Наибольшее количество воды содержится в организме новорожденных, что объясняется большим внеклеточным пространством. К первому году жизни ребенка количество воды в его теле заметно снижается, прежде всего, за счет внеклеточного пространства. Количество воды на 1 кг массы тела у детей все же больше, чем у взрослых, однако на 1 м2 поверхности тела содержание жидкости у детей значительно меньше. Водный обмен у детей протекает более интенсивно, чем у взрослых, у которых вся вода в организме обновляется примерно каждый месяц, а внеклеточное водное пространство — каждую неделю. У грудного ребенка время пребывания молекулы воды в организме составляет 3—5 дней. В отличие от взрослых у детей раннего возраста отмечается большая проницаемость клеточных мембран, а фиксация жидкости в клетке и межклеточных структурах более слабая. Особенно это касается межуточной ткани, так как кислые мукополисахариды основного вещества определяют прочность этой связи. К периоду полового созревания содержание воды составляет у мужчин 55—60%, у женщин — 46—55% (рис. 6). Причиной различий в содержании воды в организме мужчин и женщин является количество у них жировой ткани, на которую у мужчин приходится 12—25% массы тела, а у женщин 25—35%; содержание воды в жировой ткани составляет 30% ее массы, что и предопределяет различия в количестве воды в организмах мужчин и женщин.
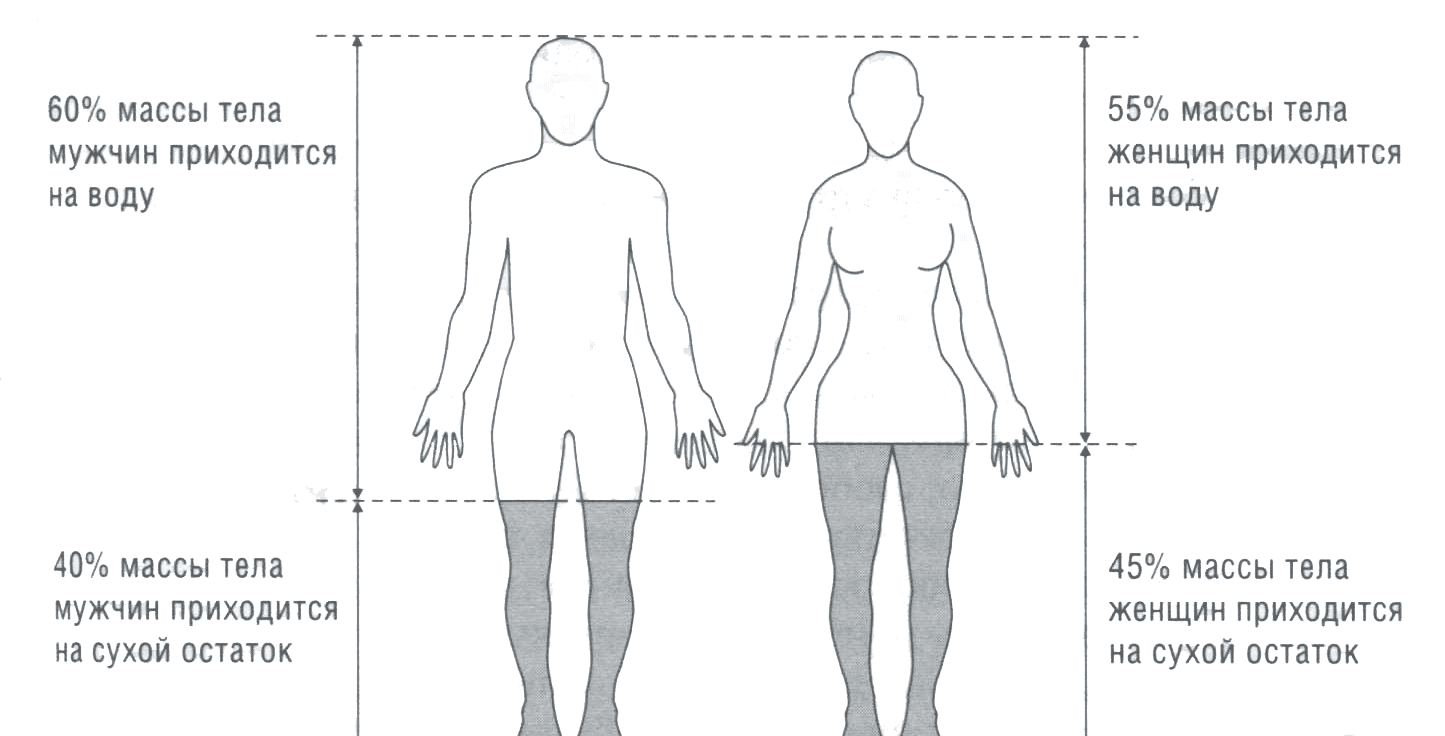
Рис. 6. Содержание воды в общей массе тела в организме мужчин (слева) и женщин (справа)
Определение общего количества воды в организме в эксперименте проводят, используя методики с оксидами дейтерия (D2O) и трития (Т2O). Однако этот подход неприменим в клинической практике. Величину отдельных пространств, занимаемых жидкостью, можно определять с помощью методов разведения с применением веществ, равномерно распределяющихся или во всех жидкостях организма, или только во внеклеточной жидкости (хлоридное пространство), или только в плазме крови, либо можно определить лабильную, не связанную с кислыми мукополисахаридами воду (инулиновое пространство). У ребенка объемы хлоридного и инулинового пространств почти одинаковы — 41,2 и 40% массы тела, у взрослого же они соответственно равны 26,4 и 1670, что свидетельствует о большей лабильности водного обмена у детей.
Физиологически детерминированное содержание воды в организме независимо от возраста, вида деятельности и в какой-то степени от характера заболевания позволяет в большинстве случаев использовать способ упрощенного расчета ее общего количества в организме с помощью следующего выражения:
масса тела, кг х 0,6 (мужчины)
масса тела, кг х 0,5 (женщины).
Половина всей воды организма находится в мышечной ткани, выполняющей функцию депо.
В целом общая масса воды в организме распределена таким образом, что 2/3 ее содержится во внутриклеточном пространстве, а 1/3 находится вне клеток (рис. 7).
В организме человека присутствует еще один компартмент, содержащий воду, но его вклад в общую структуру водного обмена организма, как правило, не рассматривается. Связан он, собственно, с биологическими мембранами. Воду, входящую в состав биологических мембран, разделяют на связанную, свободную и захваченную.Связанная вода присутствует в мембранах клеток в виде одиночных молекул и гидратных оболочек. Одиночные молекулы располагаются в углеводородной зоне мембраны. Гидратные оболочки образуются вокруг полярных частей молекул белков и липидов. Гидратные оболочки основных структурных липидов состоят обычно из 10—12 молекул воды. Эта вода осмотически неактивна и не способна растворять какие-либо вещества.
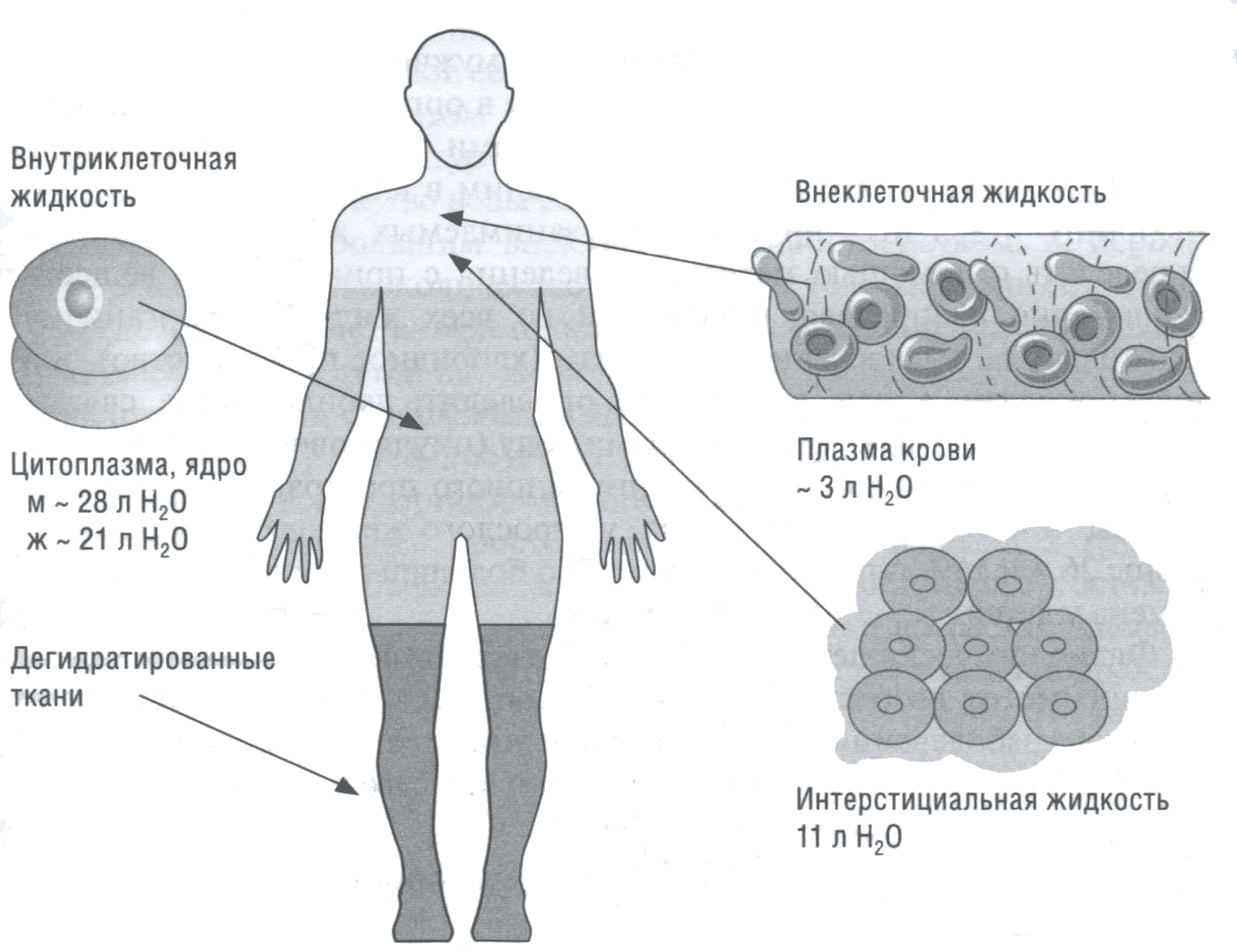
Рис. 7. Содержание воды в различных жидкостях тела: м — у мужчины; ж — у женщины
Свободная вода характеризуется способностью совершать изотропное движение в пределах мембраны, характерное для жидкой воды. Этой фракции присуща осмотическая активность. Она может покидать пределы биологической мембраны, обмениваясь с молекулами воды вне- или внутриклеточного пространства.
Вода, которая определяется в центральной части мембран между липидными бислоями, составляет фракцию захваченной воды. Захваченной воде присущи свойства свободной воды, однако она медленно обменивается с внемембранными фракциями из-за физической разобщенности.
Все фракции воды являются структурными компонентами мембран, определяя их стабильность и функциональные свойства. Вода биологических мембран не остается интактной при тех или иных видах расстройств водного обмена, однако закономерности изменений водных компонентов мембраны, их роль в нарушении функций мембран остаются практически не изученными.
Вы читали отрывок из книги "Водно-электролитный обмен и его нарушения: руководство для врачей"

В руководстве рассмотрены вопросы обмена воды и электролитов в организме человека и его нарушений. Дан краткий обзор гомеостаза воды и электролитов в норме. Описаны варианты нарушений водно-электролитного обмена, механизмы возникновения различных нарушений, методы их диагностики. Приведены значения показателей водно-электролитного обмена в норме и при патологических процессах.
Издание предназначено врачам широкого профиля, анестезиологам, реаниматологам, специалистам клинической лабораторной диагностики, студентам медицинских вузов. Книга может использоваться в системе последипломного образования врачей.
Купить книгу "Водно-электролитный обмен и его нарушения: руководство для врачей"





























































































0 комментариев