Методические рекомендации. «Особенности течения LONG-COVID инфекции. Терапевтические и реабилитационные мероприятия». Часть 7. "Неврологические заболевания. Long-COVID инфекции"
Лонг-ковид: что такое лонг-ковид и как с ним бороться? Часть 1
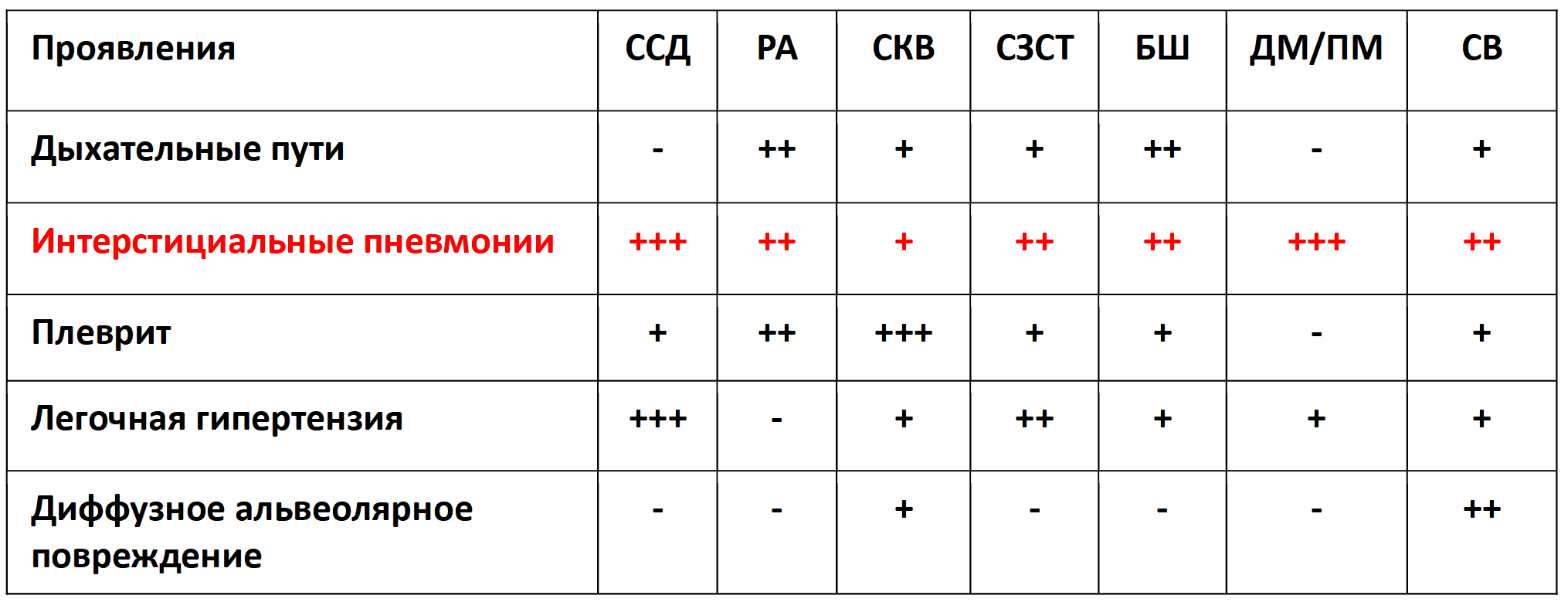
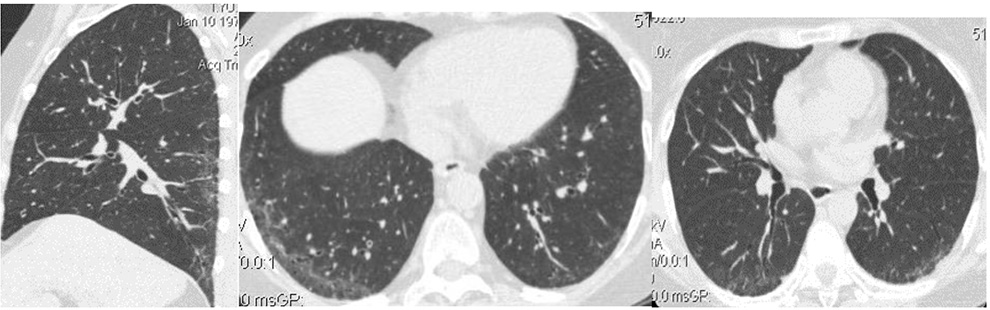
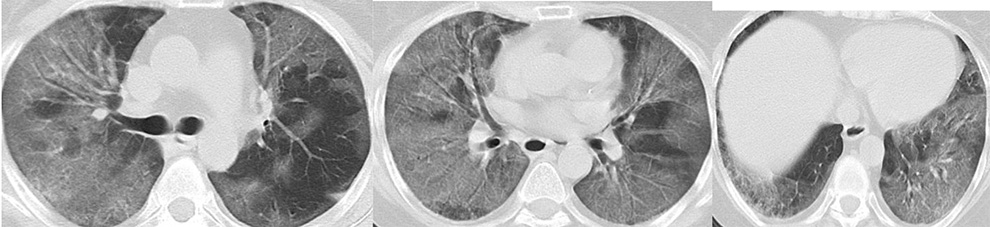
Поражение дыхательной системы при LONG-COVID инфекции. Часть 2
Поражение сердечно-сосудистой системы при Long-COVID инфекции. Часть 3
Поражение эндокринной системы при Long-COVID инфекции. Часть 4
Поражение почек при Long-COVID. Часть 5
Ревматизм. Long-COVID инфекции. Часть 6
Психиатрия. Long-COVID инфекции. Часть 8
Детский мультисистемный воспалительный синдром, ассоциированный с COVID-19. Часть 9
Мультисистемный воспалительный синдром у взрослых, ассоциированный с COVID-19. Часть 10
Медицинская реабилитация при Long-COVID инфекции Часть 11
Неврологические заболевания. Long-COVID инфекции.
Постковидный синдром можно определить как последствия новой коронавирусной инфекции, на фоне которой до 20% пациентов страдают от долгосрочных симптомов, в большинстве случаев длящихся до 12-ти недель, в 2,3% случаев – более 12-ти недель.
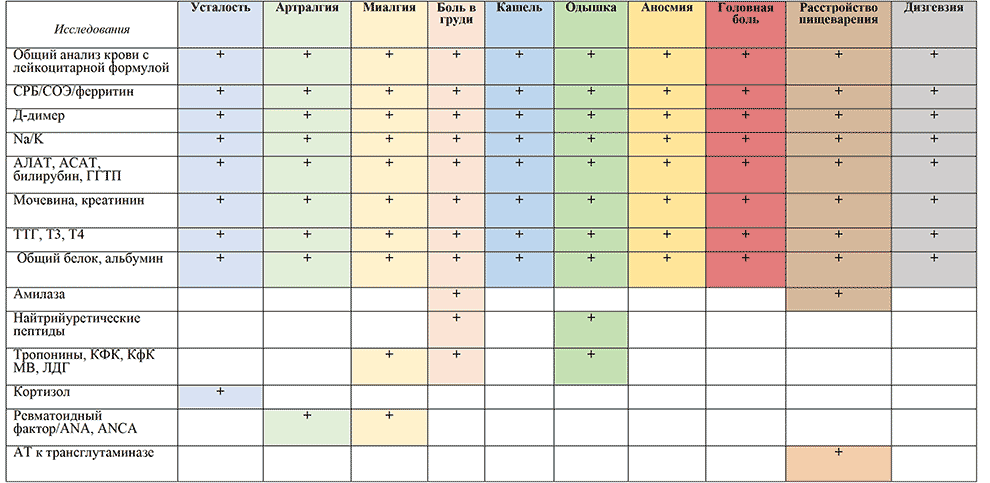
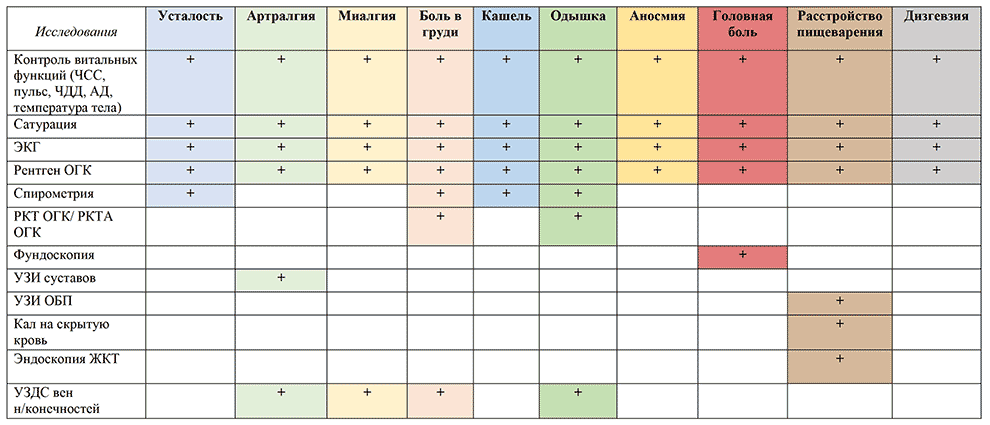
Диагностики острой коронавирусной инфекции в большинстве случаев не вызывает затруднений, напротив, длительный COVID-19 имеет широкий спектр разнообразных проявлений, именно поэтому диагноз постковидного синдрома не всегда является очевидным в клинической практике. В частности, по данным ВОЗ, пациенты, выздоравливающие от инфекции COVID-19, могут иметь такие стойкие симптомы, как: усталость, выраженную утомляемость, сложность концентрировать внимание и снижение умственной работоспособности, забывчивость, потеря или изменение вкуса, запаха или слуха, одышка, сухой кашель, тошнота, боль в животе и грудной клетке.
Метаанализ 30 обсервационных исследований, проведенный в 18 странах мира, позволил выделить два основных симптомокомплекса: острый постковидный синдром, характеризующийся симптомами, сохраняющимися в течение месяца после первоначальной инфекции, что соответствует продолжающемуся симптоматическому COVID-19; и хронический постковидный синдром, отличающийся сохраняющимися более 3 месяцев симптомами после первоначальной инфекции, что соответствует постковидному синдрому, согласно классификации NICE.
При продолжающемся симптоматическом COVID-19 выделено 13 преобладающих симптомов, среди которых наиболее частыми являются: быстрая утомляемость (0,37; 95% ДИ 0,20–0,56, I2=98%); одышка (0,35; 95% ДИ 0,16–0,562, I2=97%); тревожные нарушения (0,29; 95% ДИ 0,19–0,40, I2=88%).
Среди других проявлений отмечаются кашель, озноб, лихорадка, депрессия, нарушение памяти, нарушение концентрации внимания, головная боль, артралгия, аносмия, агевзия, торакалгия и чувство стеснения в груди. При хроническом постковидном синдроме наиболее часто наблюдаются: утомляемость (0,48; 95% ДИ 0,23–0,73, I2=100%); нарушение сна (0,44; 95% ДИ 0,08–0,85, I 2=99%) и одышка (0,39; 95% ДИ 0,16–0,64, I2=99%), а также головная боль, аносмия, агевзия, торакалгия или чувство стеснения в груди. Согласно данным мультипараметрического анализа с учётом пола, возраста, этнической принадлежности, индекса массы тела и факта госпитализации, наличие только быстрой утомляемости объясняет долгосрочное нарушение физической активности у пациентов, перенесших COVID-19 (OR 6,0; 95% ДИ 1,0–34,9; р=0,04), что в свою очередь влияет на течение сопутствующих заболеваний.
Обобщая основные проявления постковидного синдрома, возникающие постоянно или волнообразно, можно выделить следующие:
- нарушения дыхания (одышка, неполный вдох, апноэ)
- болевые синдромы различной локализации (цефалгии, миалгии, артралгии, дорсалгии)
- нарушения обоняния и вкусовые нарушения
- нарушения пищевого поведения (булимия или анорексия)
- потеря волос, выпадение зубов, кистозные образования в полости челюстей
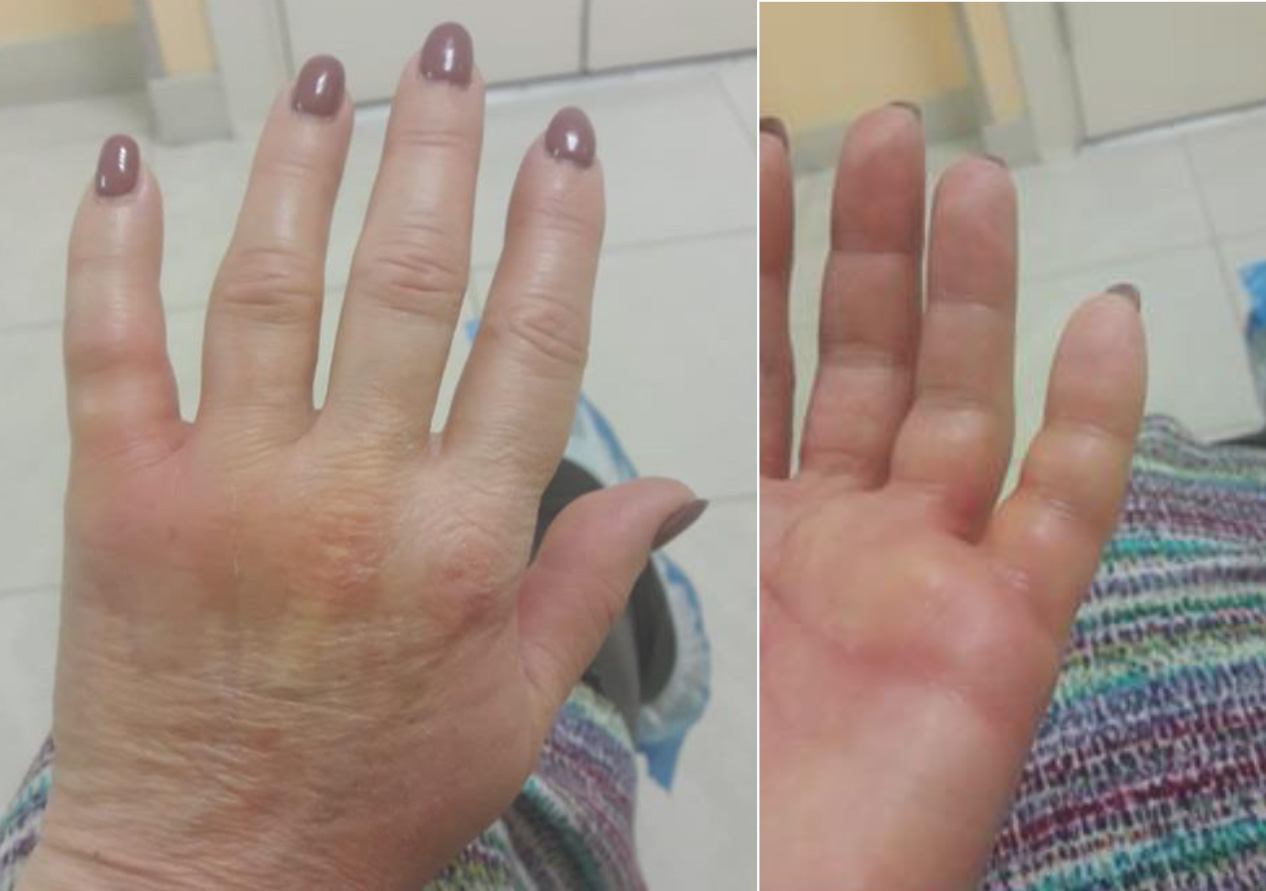
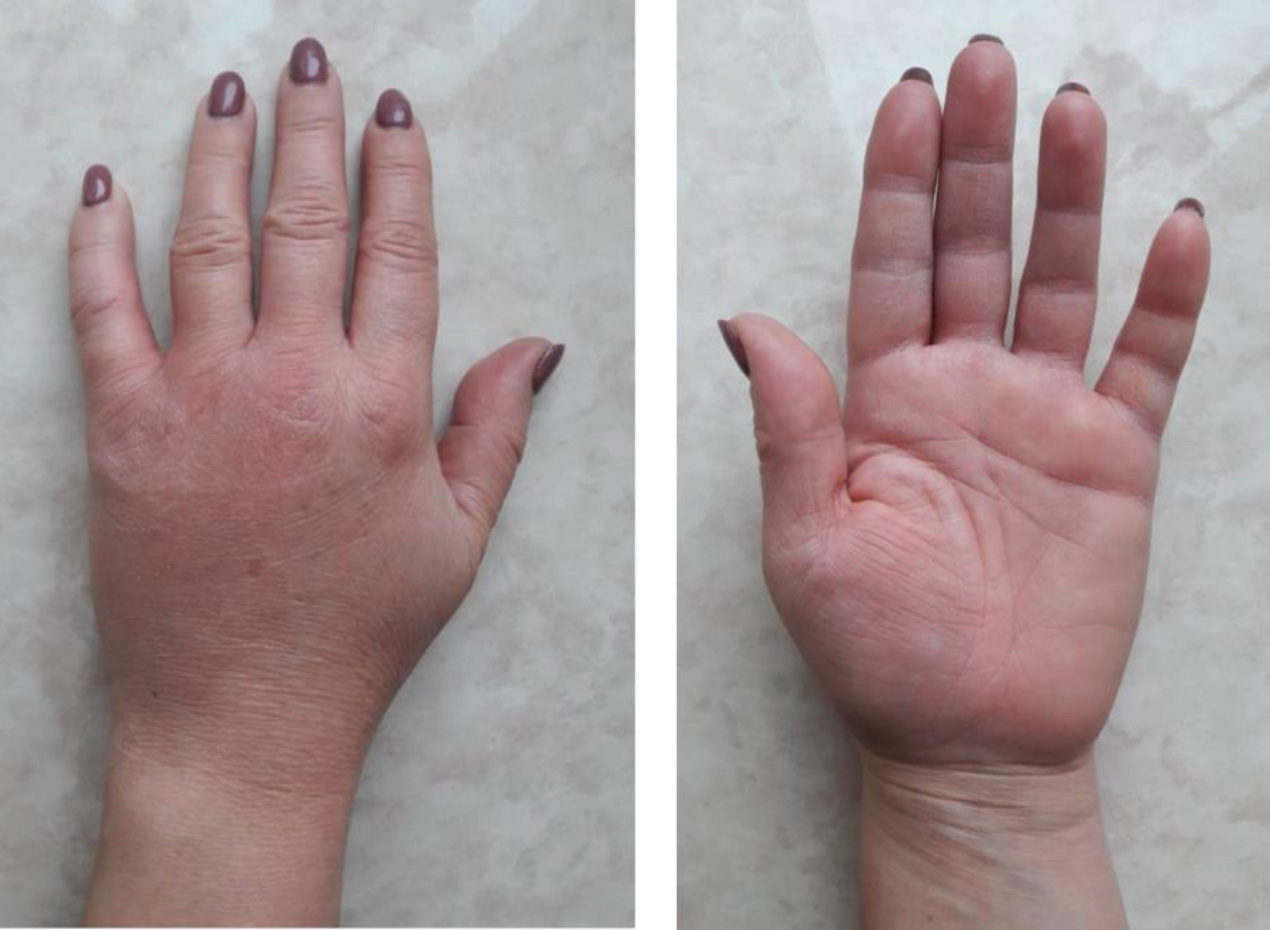
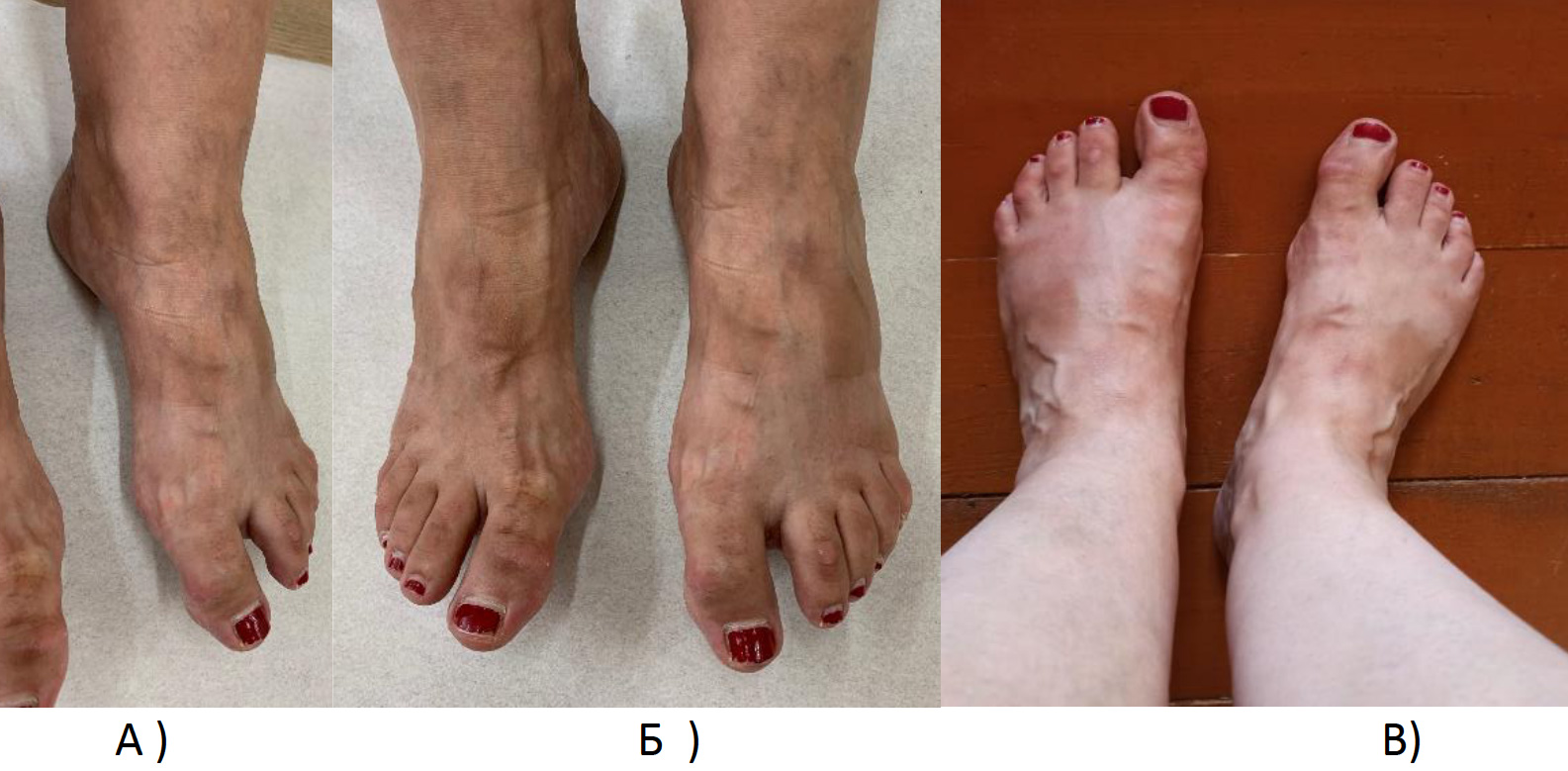
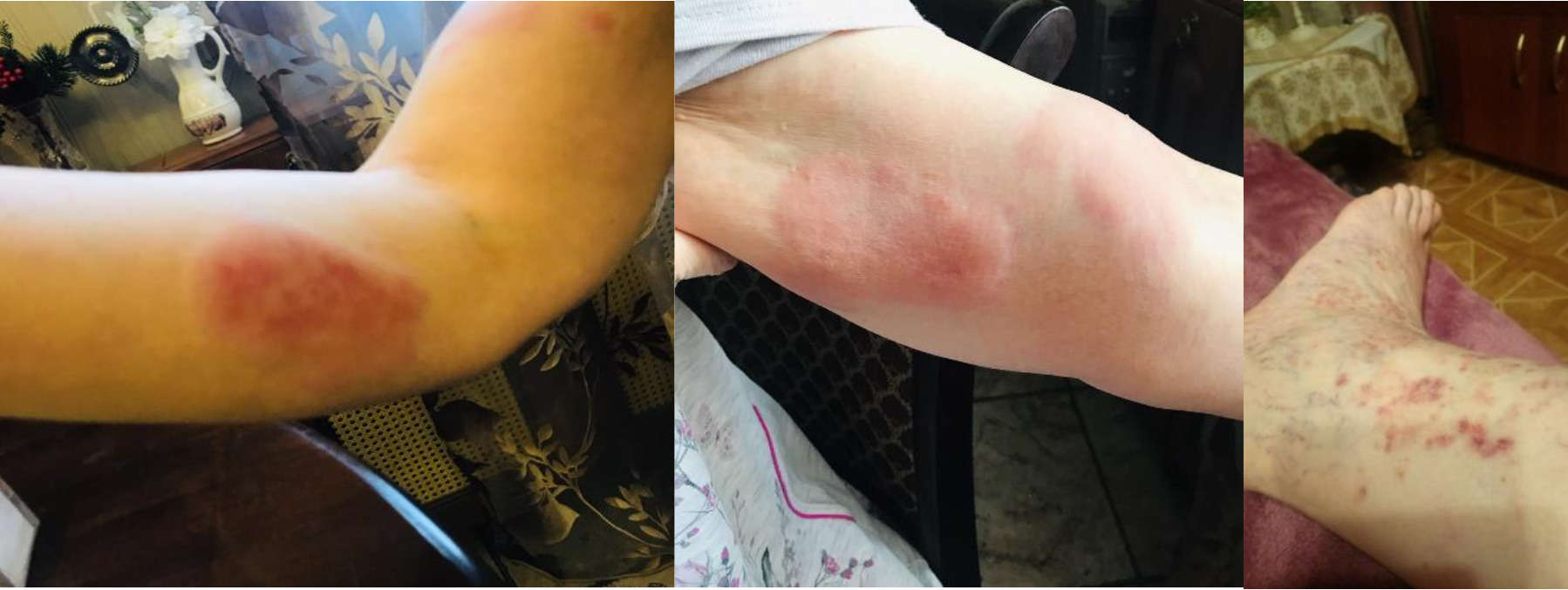
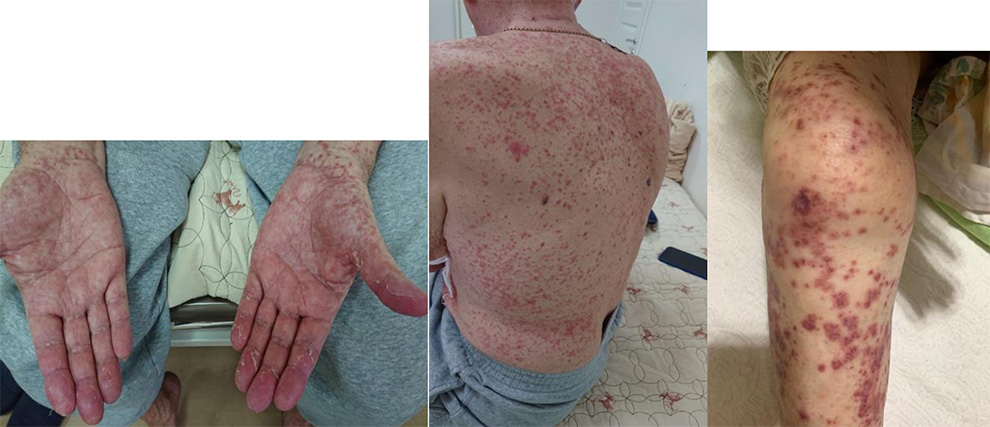
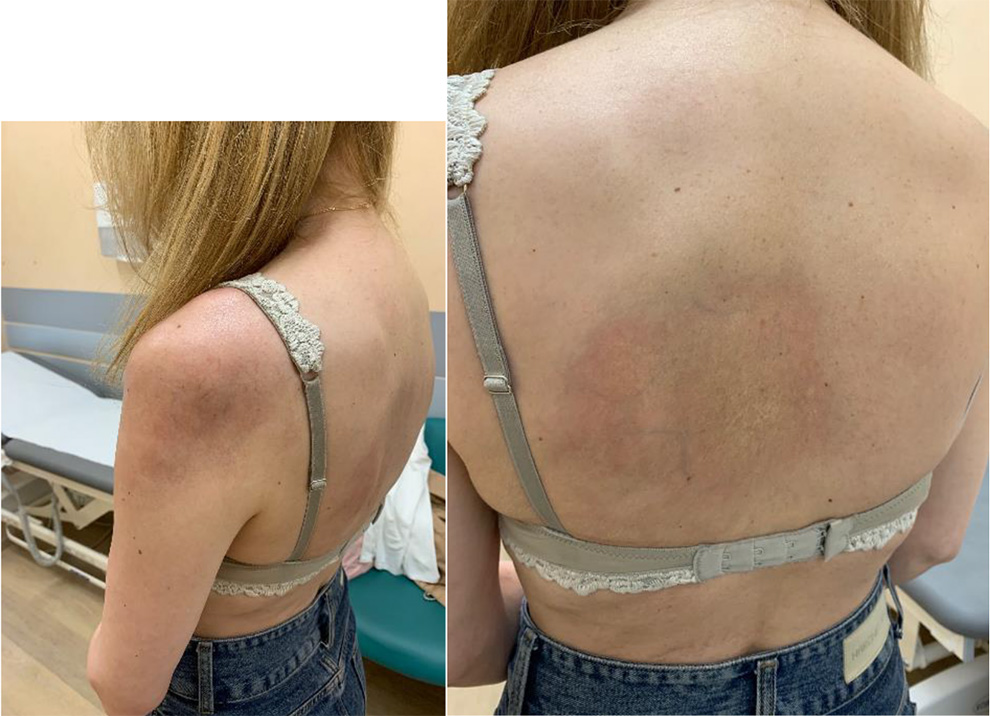
- сосудистые и васкулитные проявления на коже и иные кожные реакции
- резкие перепады артериального давления и пульса, аритмии, тахикардия (в т.ч. ортостатическая тахикардия), головокружение
- когнитивные нарушения (нарушения памяти, расстройства концентрации внимания, дезориентация в пространстве и времени, снижение самокритики)
- психоэмоциональные расстройства (фобии, существенно повышенный уровень тревожности, панические атаки), асоциальное поведение, гиперсексуальность
- выраженная астения
- нарушения сна
- расстройства деятельности желудочно-кишечного тракта (диарея, возникающая волнообразно и не зависящая от диеты и приёма лекарственных препаратов)
- дистермия (продолжительная субфебрильная температура / гипотермия / скачки температуры)
- синдром Гийена-Барре
Рассмотрим некоторые из перечисленных выше проявлений постковидного синдрома и особенности ведения пациентов с данными нарушениями.
Заболевания опорно-двигательного аппарата и болевые синдромы
На фоне распространения новой коронавирусной инфекции отмечается и распространение заболеваний опорно-двигательного аппарата (ОДА) и соответственно болевых синдромов, в связи с чем проблема ревматологических и неврологических проявлений и осложнений Covid-19, а также поиск путей ее решения представляет собой крайне важную задачу современной медицины.
Среди причин прогрессирования и развития болевых синдромов на фоне новой коронавирусной инфекции можно выделить как экзогенные, так и эндогенные причины.
Экзогенные причины:
- режим самоизоляции и карантина, способствующий гиподинамии и развитию избыточной массы тела
- дистанционная работа, при проведении которой часто допускается не эргономичная поза
- отсутствие возможности получения полноценной медицинской помощи
- непосредственное патогенное влияние вируса на нервную, мышечную и хрящевую ткани
- активация цитокинами и хемокинами ноцицепторных сенсорных нейронов
- аутоиммунное поражение нервных стволов, связочно-мышечного аппарата и суставов
- выраженные психоэмоциональные расстройства
По данным различных исследований и наблюдений болевые синдромы у пациентов с COVID-19 широко распространены. Наиболее часто наблюдаются артралгии и миалгии различной локализации (у 30%-88% пациентов с COVID-19), цефалгии (до 85% среди больных с COVID-19) и дорсалгии (до 30% среди пациентов с COVID-19).
В условиях наличия вируса SARS-CoV-2 в организме и его патогенного воздействия своевременная и адекватная терапия и профилактика заболеваний ОДА приобретают существенное значение, поскольку COVID-19 способствует более быстрому развитию и более тяжелому течению данных заболеваний, о чем свидетельствует и собственный опыт, и результаты различных исследований.
Успех ведения и эффективность терапии пациентов данной категории зависит от грамотно проводимого медикаментозного лечения и физической реабилитации.
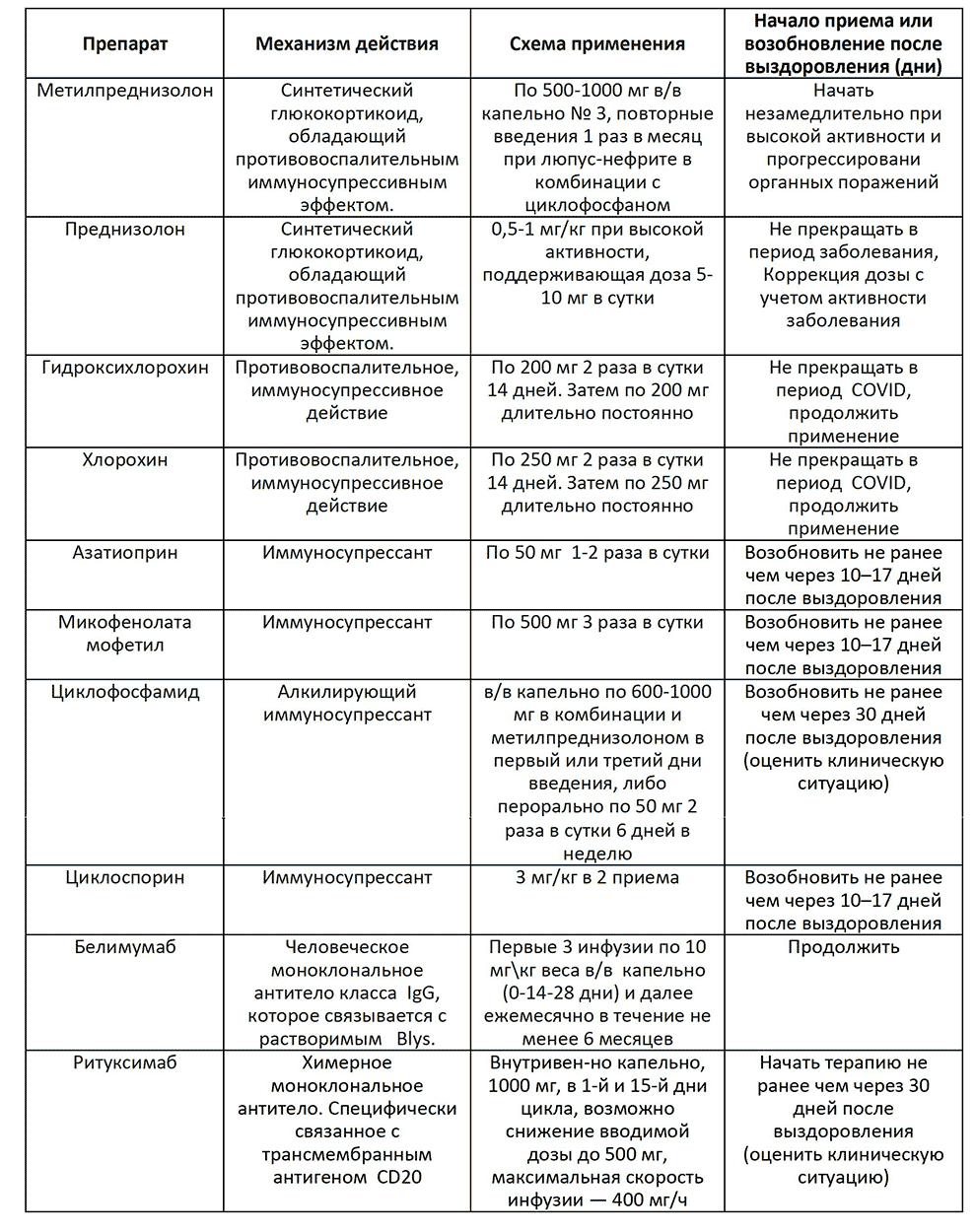
При умеренном повышении концентрации провоспалительных цитокинов и соответственно отсутствии цитокинового шторма, т.е. отсутствии необходимости экстренного применения моноклональных антител, или после подавления цитокинового шторма с помощью данных препаратов, а также в период реконвалесценции необходимо оказание воздействие на патогенетические механизмы развития воспаления и боли у пациентов с нарушениями ОДА, протекающими на фоне COVID-19, с помощью лекарственных средств, которые влияют на большинство описанных выше патогенетических механизмов.
Надо отметить, что пандемические масштабы распространённости COVID-19 способствовали беспрецедентным усилиям мирового сообщества относительно поиска лекарственных препаратов, которые могут быть эффективны при ведении пациентов с новой коронавирусной инфекцией и её осложнениями и последствиями, причем, данная работа проводится в экстренном режиме. В подобных условиях анализ и изучение дополнительных показаний к назначению тех или иных препаратов, возможно, рассматриваемых и в качестве off-label, приобретает особое значение и может иметь крайне важное терапевтическое и прогностическое значение.
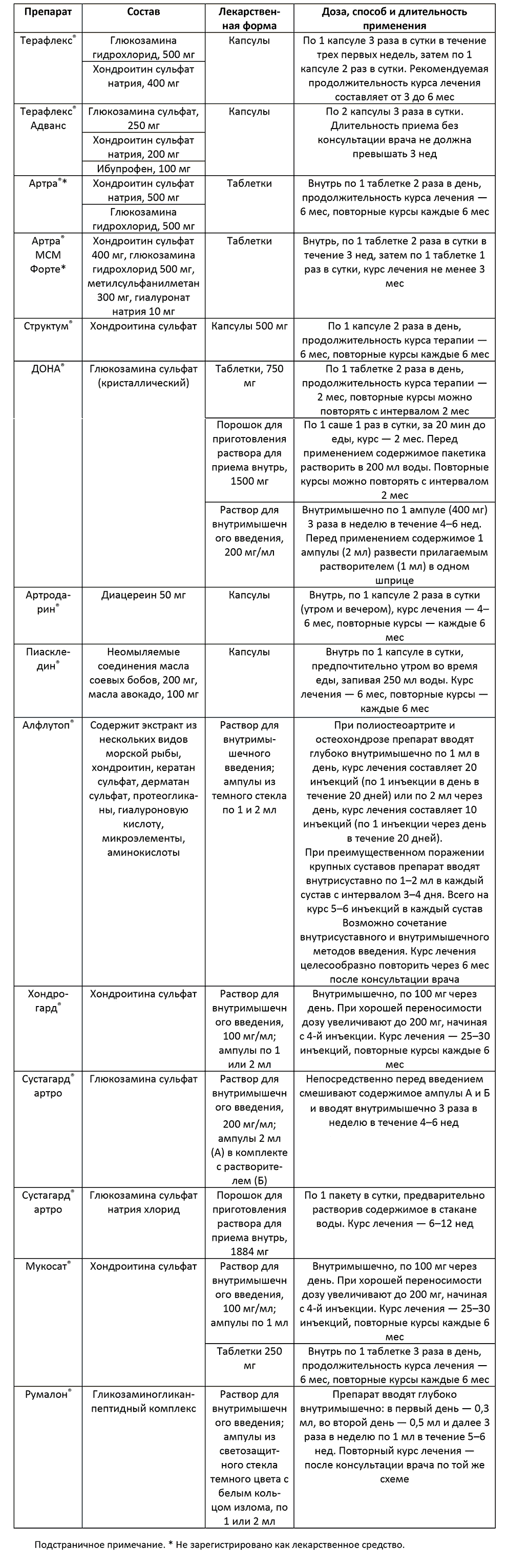
Применение инновационных препаратов, а также использование лекарственных средств, которые всесторонне изучались в течение многих лет, позволили расширить возможности терапии пациентов с инфекцией COVID-19 и её последствиями и осложнениями, в т.ч. и поражением ОДА и болевыми синдромами. С данной точки зрения достаточно широкое распространение при терапии пациентов данной категории нашли такие хорошо известные и широко применяемые до пандемии COVID-19 лекарственные средства как нестероидные противовоспалительные препараты, миорелаксанты, витамины группы В, нуклеотиды, SYSADOA.
Нарушения обоняния и вкуса
Согласно многочисленным данным, полученным из разных стран мира, нарушения обоняния и вкуса отмечаются у 17–98% пациентов с подтвержденным COVID-19.
Нарушения обоняния могут предшествовать появлению кашля или одышки, а также во многих случаях сопровождаться потерей вкуса. Более чем у четверти пациентов дизосмия является начальным симптомом заболевания.
Согласно одному из исследований, нарушения обоняния развивается в среднем через 4,4 суток после инфицирования организма.
Говоря о механизмах развития дизосмии при Covid-19, надо отметить, что изначально специалисты предполагали, что нарушение обоняния при новой коронавирусной инфекции как, например, при гриппе возникает в результате повреждения обонятельного эпителия и гибели ольфакторных нейронов и соответственно носит сенсоневральный характер.
Более позднее исследование убедительно продемонстрировало роль в развитии аносмии также и рецепторов ACE2 (англ. Angiotensin-Сonverting Еnzyme - ангиотензин превращающего фермента 2) и TMPRSS2 (англ.
Transmembrane protease, serine - мембрано-связанной сериновой протеазы).
Данные рецепторы, которые, как известно, SARS-CoV-2 использует для проникновения в клетки, экспрессируются на слизистой оболочке обонятельного эпителия, но не на обонятельных сенсорных нейронах, а на поддерживающих клетках и стволовых клетках базального эпителия, которые на ряду с железами Боумена, в свою очередь, коэкспрессируют рецептор ACE2 SARS-CoV-2 и протеазу белка шипа TMPRSS2 на уровнях, сравнимых с уровнями, наблюдаемыми в клетках легких, в то время как в зрелых обонятельных сенсорных клетках ACE2 и TMPRSS2 не экспрессируются. Данные наблюдения позволили предположить, что SARS-CoV-2 не проникает непосредственно в нейроны, а его мишенью являются поддерживающие и стволовые клетки обонятельного эпителия.
Кроме того, в настоящее время рассматриваются и другие теории нарушения обоняния при COVID-19. Так, одной из причин аносмии при Covid-19 называют образование кальциевых микротромбов в сосудах, которые питают глию – клетки микроокружения нейронов, отвечающих за обоняние. Многие специалисты склонны предполагать смешанный характер аносмии при новой коронавирусной инфекции.
Выделяют следующие виды расстройства обоняния:
- гипосмия – снижения восприятия обоняния
- аносмия – отсутствие обоняния
- паросмия – искажение нормального восприятия запахов (например, вместо запаха шоколада пациент слышит запах гниющих продуктов)
- фантосмия – восприятие запахов при их отсутствии
- какосмия – приступы ощущения неприятных отвратительных запахов.
В случае, когда нарушения обоняния при COVID-19 имеют транзиторный характер, то в проведении системных мер лечения необходимости не возникает. Если аносмия теряет транзиторный характер, персистирует после купирования других симптомов заболевания и существует более двух недель, необходимо проведение контроля обонятельной функции в динамике и применения медикаментозных и немедикаментозных средств для восстановления обоняния.
Прежде всего, применяют обонятельный тренинг, конечная цель которого заключается в обучении пациента, потерявшего обоняние, снова распознавать запахи, а задачи состоят в активации обонятельных рецепторов и реконструкции нейронных связей. Механизм действия данного тренинга основан на пластичности обоняния, т.е. способности нейронов обонятельной зоны к восстановлению и способности головного мозга распознавать, запоминать, хранить запахи и соотносить их с увиденными и услышанными образами. Необходимо отметить, что при проведении данных упражнений пациент тренирует и обоняние, и обонятельную память.
Перед началом курса обонятельного тренинга проводится ольфактометрия. Для выполнения тренинга необходим набор хорошо знакомых ярких и устойчивых запахов, связанных с прямыми образами (кофе, шоколад, ментол, тимьян, клубника, шоколад, жасмин, мандарин, розмарин, бергамот, гардения, роза, лимон, анис, эвкалипт, гвоздика).
Техника обонятельного тренинга заключается в попеременном вдыхание 4-х различных запахов в течение 20 секунд каждый, концентрируясь на особенностях каждого запаха, при этом пациент лишь принюхивается (мелкими легкими вдохами). Тренировка осуществляется ежедневно два раза (утром и вечером) в течение, как минимум, 3-х месяцев. По истечении 3-х месяцев вновь проводится ольфактометрия для определения результатов тренинга. Если восстановление обоняния не наблюдается, тренировка продолжается. Сигналом к началу восстановления нередко служит искажение запахов, обусловленное неполной регенерацией обонятельных рецепторов, которые воспринимают ароматы либо не полностью, либо избирательно.
Для повышения эффективности обонятельного тренинга можно рекомендовать более длительный курс тренировок (более 32 недель), использование запахов с высокой концентрацией, а также смена одорантов каждые 3 месяца.
В рамках комплексного ведении пациентов с нарушением обоняния используются следующие дополнительные методы и средства:
- смазывание висков и переносицы ментоловым маслом
- использование ароматических ламп
- массаж переносицы, запястий, голеней ароматическими маслами
- использование свежевыжатого сока чистотела (интраназально по 1 капле в каждый носовой ход 3 раза в день)
- вдыхание ароматов трав (смесь из ромашки, мяты, тмина, ландыша)
- ингаляции (лимонно-эфирные, камфорно-ментоловые)
- разжевывание гвоздики, кресс-салата и других продуктов, ярко стимулирующих вкусовые и обонятельные рецепторы.
Согласно результатам широкомасштабного исследования, проведенного в трех университетских клиниках Бельгии, при нарушении обоняния, возникшего на фоне COVID-19, наиболее эффективны обонятельный тренинг и цитрат натрия (соль лимонной кислоты).
Одной из причин аносмии при COVID-19 является образование кальциевых микротромбов в сосудах, которые питают глию – клетки микроокружения нейронов, отвечающих за обоняние. В то же время цитрат натрия растворяет микрокристаллы кальция в сосудах и вымывает их из слизистой носа.
Эффективность цитрата натрия при восстановлении обоняния была статистически значимо показана и до появления COVID-19.
Также при нарушении обоняния целесообразно использовать такую медикаментозную терапию, как ингибиторы холинэстеразы, нуклеотиды и витамины группы В. В частности, витамин В12, участвующий в процессах миелинизации обонятельных периферических нейронов и имеющий доказанный эффект в терапии больных с нарушением функции обоняния, особенно у пожилых, пациентов с сахарным диабетом, гипергомоцистеинемией, тромбофилией и других людей, находящихся в группе риска развития дефицита витамина В12. Пероральная терапия тиамином, пиридоксином и цианокобаламином рациональна в рамках проведения реабилитационных мероприятий у лиц, уже перенесших COVID-19 и столкнувшихся с его последствиями в виде клинических признаков недостатка витаминов группы В.
Ряд исследователей свидетельствуют об эффективности при восстановлении обоняния омега-3 жирных кислот (по 500–1000 мг в сутки). Согласно исследованиям других авторов, определенным эффектом обладает комбинация ретинола (витамин A) и цинка, однако к единому мнению относительно эффективности данного сочетания специалисты пока не пришли, и очередные исследования поводятся в настоящее время. При назначении данных препаратов, пациента необходимо предупредить пациента о нежелательности длительного применения высоких доз ретинола.
Интраназальные глюкокортикостероиды рекомендуются к использованию лишь при сопутствующих признаках воспаления слизистой оболочки полости носа и соответствующем коморбидном фоне. Так, согласно положениям документа ВОЗ «ARIA» (англ. Allergic Rhinitis and its Impact on Asthma - Аллергический ринит и его влияние на астму), разработанного Европейской академией аллергологии и клинической иммунологии, пациентам, перенесшим COVID-19 на фоне бронхиальной астмой, аллергического ринита и полипозного риносинусита необходимо продолжение базисной терапии ингаляционными и/или интраназальными кортикостероидными препаратами в обычном режиме. Отмена базисной терапии, например, при сезонном аллергическом рините способствует усилению симптомов, в частности чихания, и соответственно к распространению инфекции. Кроме того, известно, что кортикостероиды способны повышать защитный потенциал эпителиального покрова верхних дыхательных путей, в том числе к воздействию вирусов. Дополнительную безопасность местного применения кортикостероидов обеспечивает их использование в дегидрированной форме.
Астения
Астенический синдром является одним из наиболее частых среди длительно существующих симптомокомплексов у пациентов, перенесших инфекцию COVID-19, нередко наблюдаясь в течение более 100 дней после первоначального инфицирования. Как у пациентов трудоспособного возраста (39±15 лет) со среднетяжелым течением коронавирусной инфекции, так и у пожилых больных, астенический синдром может возникать уже в дебюте заболевания в одинаковом проценте случаев - 63,3%. У половины пациентов моложе 70 лет астенические проявления отмечаются через 1 месяц от начала заболевания, а в 40% случаев - через 2 месяца. Особенно тяжёлые и выраженные постинфекционной астении наблюдаются более, чем у половины (55%) лиц старше 70 лет, перенёсших инфекцию COVID-19.
Под астенией понимают болезненное состояние, проявляющееся повышенной утомляемостью и истощаемостью с неустойчивостью настроения, ослаблением самообладания, нетерпимостью и нетерпеливостью, неусидчивостью, нарушением сна, утратой способности к длительному умственному и физическому напряжению, плохой переносимостью или полной непереносимостью громких звуков, яркого света, резких запахов. Для выявления астенического симптома разработаны специальные шкалы и опросники, среди которых можно выделить субъективную шкала оценки астении МFI-20 и шкалу астенического состояния.
Субъективная шкала оценки астении МFI-20 (англ. Multidimensional Fatigue Inventory) предназначена для экспресс-диагностики астенического состояния. Данная шкала состоит из пяти субшкал, согласно которым оцениваются общие астенические проявления, уровень активности и мотивированности пациента, а также физические и психические проявления астении. Шкала астенического состояния разработана на базе данных клинико-психологических наблюдений и Миннесотского многомерного личностного опросника MMPI (англ. Minnesota Multiphasic Personality Inventory), разработанного американскими психологами в 1940 году, который пользуется большой популярностью среди врачей, психологов, социологов и педагогов. С помощью данного опросника выявляют психосоциальные особенности человека, его психоэмоциональное состояние, а также психологическую совместимость и адаптивность в коллективах, возможность сотрудников занимать определенные должности и ряд других вопросов.
Опросник MMPI включает в себя 566 различных утверждений, на которые испытуемому необходимо дать положительный или отрицательный ответ, на основании которых формируются десять основных клинических шкал, позволяющих сделать заключение о психологических характеристиках личности испытуемого. Кроме того, согласно результатам этого опросника, возможно формирование дополнительных шкал, которые способствуют обнаружению таких личностных особенностей исследуемого человека как склонность к употреблению алкоголя и к совершению преступлений, способность к обучению, эгоистичность, застенчивость, наивность и ряд других.
Ведение пациента с астенией включает в себя четыре основных направления: общие рекомендации, диетические особенности, медикаментозную терапию и психотерапию.
Среди общих рекомендаций прежде всего можно выделить оптимальный режим труда и отдыха, введение в режим дня оздоравливающих адекватных физических нагрузок, достаточно длительный отдых и смена обстановки (отпуск, санаторно-курортное лечение, туристическая поездка), отказ от контакта с вредными воздействиями и ряд других мер.
К диетическим рекомендациям при астении относится прежде всего повышенное содержание в рационе продуктов, содержащих триптофан в достаточно большой концентрации, в частности, бананы, мясо индейки, сыр, хлеб грубого помола, а также продукты с повышенным содержанием витаминов группы В (печень, яйца) и витамина С (шиповник, черная смородина, облепиха, киви, клубника, цитрусовые, яблоки, салаты из сырых овощей и свежие фруктовые соки).
Среди медикаментозных средств при астении применяются адаптогены растительного происхождения: женьшень, родиола розовая, китайский лимонник, элеутерококк, пантокрин, а также препараты, содержащие комплексы витаминов (витамины группы В, С, РР) и микроэлементов (цинк, магний, кальций). И, безусловно, при влиянии на постинфекционную астению необходимо ориентироваться на патогенетическую терапию, учитывая различные механизмы развития астенического состояния. В частности, по данным биохимических исследований показано, что витамин B12 может ингибировать РНК-полимеразную активность вирусного белка NSP12, участвующего в репликации SARS-CoV-2. В структуре NSP12 место связывания витамина B12 перекрывается с таковым у РНК, именно поэтому витамин В12 может ингибировать активность вирусной РНК-полимеразы.
Учитывая необходимость проведения активной как двигательной, так и дыхательной реабилитации, крайне важным представляется обеспечение выраженного медикаментозного влияния на синдром астении, поскольку последний в существенной степени препятствует проведению активной реабилитации и соответственно восстановлению функций пациента.
При выборе медикаментозных средств, способных обеспечить значительную стенизацию организма, необходимо опираться на патогенетические механизмы формирования астенического состояния, развивающегося на фоне коронавирусной инфекции, как то: оксидантный стресс, энергодефицит и другие. В частности, показано влияние комбинированного лекарственного средства, состоящего из янтарной кислоты, никотинамида, инозина и рибофлавина, - Цитофлавина, на ключевые патофизиологические звенья полиорганной недостаточности при инфекции COVID-19 за счет усиления процессов тканевого дыхания и восстановления митохондриального звена энергетического обмена клетки, что позволяет оптимизировать терапию и улучшить течение и исходы заболевания.
Добавление курсового последовательного применения Цитофлавина (10,0 мл на 200 мл физиологического раствора в течение 10 дней 1 раз в день с продолжением пероральной формы препарата - 2 таблетки 2 раза в день в течение 25 дней) в схему комплексной реабилитации постковидного синдрома позволяло достоверно улучшить общее функциональное состояние организма, снизить выраженность астенического синдрома и повысить толерантность к физическим нагрузкам.
Другой лекарственный препарат, содержащий фонтурацетам, Нанотропил Ново, зарекомендовавший себя как эффективное ноотропное средство в терапии заболеваний, сопровождающихся физической и умственно-психической утомляемостью и апатией, также рассматривается в комплексной терапии пациентов с постковидными астеническими проявлениями.
Когнитивные нарушения
Наиболее частыми проявлениями постковидного синдрома наряду с быстрой утомляемостью или слабостью, являются когнитивные нарушения (КН). В частности, по данным онлайн опроса 4182 пациентов, перенесших инфекцию COVID-19, показано, что 85,1% участников испытывали КН, описывая их как «туман в голове» (англ. brain fog). При более подробном анализе когнитивной сферы выявлено, что чаще всего у пациентов наблюдалось снижение концентрации внимания (74,8%), при выполнении интеллектуальной работы (64,9%), нарушение управляющих функций (57,6%), проблемы в принятии решений (54,1%) и замедленность мышления (49,1%). Анализ российской популяции пациентов обнаружил схожую картину постковидных нарушений: у 47,1% из 2649 госпитализированных пациентов с лабораторно подтвержденным диагнозом инфекции COVID-19 наблюдался хотя бы один симптом через 6–8 месяцев после выписки из стационара, причём лидирующими в этом перечне были астения (21,2%) и КН (9,1%). Нарушение внимания является одним из пяти самых частых проявлений перенесённой инфекции COVID-19, отмечаясь почти у половины (44%) пациентов.
Анализ данных 431 051 человека, перенесших коронавирусную инфекцию, из Биобанка Великобритании обнаружил, что только один фактор инфицирования Covid-19 является статистически значимым для последующего нарушения у них когнитивных функций, при этом механизмы и патогенетические процессы данных расстройств не до конца понятны. У пациентов старшего возраста с деменцией инфекция COVID-19 может дебютировать с нетипичных психопатологических симптомов: беспокойства, возбужденности, дезориентации, бреда, отказа от помощи или потери аппетита. Указанные атипичные симптомы могут замедлять процесс постановки правильного диагноза у больных с деменцией, увеличивая риск развития осложнений и смерти. Проведенное в Великобритании наблюдательное исследование с участием 125 пациентов в стационаре с новой коронавирусной инфекцией продемонстрировало необычные проявления инфекционного заболевания, в частности, у 6 пациентов наблюдались неврологические симптомы в виде «когнитивного расстройства, сходного с деменцией».
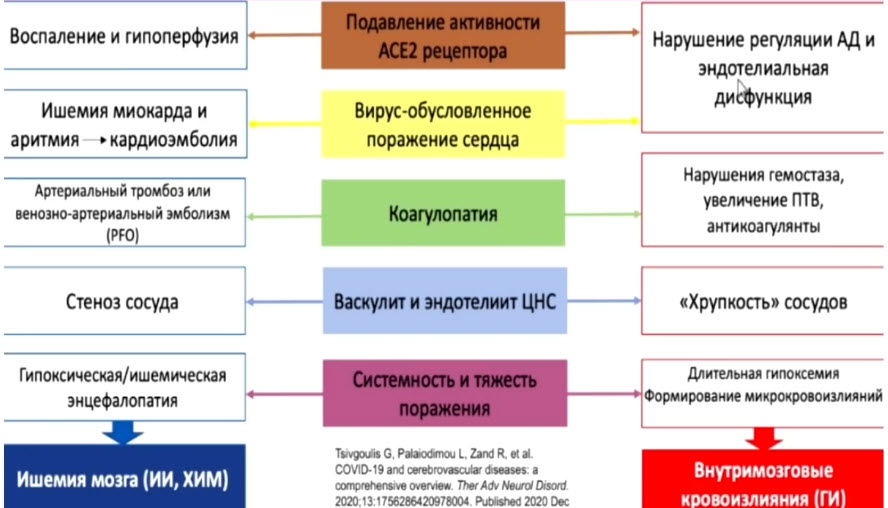
Опубликованные американскими коллегами данные ретроспективного исследования 50 пациентов среднего возраста с неврологическими проявлениями, госпитализированных в связи с инфекцией COVID-19, продемонстрировали в 40% случаев острую цереброваскулярную патологию, в том числе, ишемический инсульт (20%), внутримозговое кровоизлияние (8%) и субарахноидальное кровоизлияние (8%). У 24% больных развивались эпилептические приступы с последующей головной болью и кратковременными нарушениями памяти. Важно отметить, что у пациентов, включенных в исследование, часто наблюдались такие сопутствующие заболевания, как артериальная гипертензия (60%), сахарный диабет 2-го типа (60%) и ожирение (42%).
Основными причинами развития КН являются:
- непосредственное поражение головного мозга вирусом SARS-CoV2 с развитием энцефалита или энцефаломиелита
- постреанимационные осложнения в рамках синдрома последствий интенсивной терапии или ПИТ-синдрома, что в том числе связано с нахождением на искусственной вентиляции легких, медикаментозной седацией и применение ряда лекарственных средств
- проявление цереброваскулярных заболеваний вследствие инфекции COVID-19, опосредованные эндотелиальной дисфункцией, нарушением гемостаза, системной воспалительной реакцией и другими факторами
- постковидный синдром
Результаты проведенного Imperial College London исследования 84 285 людей, перенесших новую коронавирусную инфекцию, свидетельствуют о том, что в ряде тяжелых случаев течения заболевания когнитивный дефицит может длиться месяцами, причём возникновение КН у этих пациентов может быть сопоставимо с последствиями старения мозга на протяжении 10 лет.
На сегодняшний день патогенез КН, связанных с инфекцией COVID-19, не до конца ясен, вместе с тем обсуждается мультифакторная природа возникновения данных нарушений, связанная с нейротропностью и нейроинвазивностью вируса SARS-CoV2, а с другой стороны, с чрезмерным нейровоспалительным ответом организма на тяжелую системную инфекцию, при котором возникает усиленные и нерегулируемые иммунные реакции или «цитокиновый шторм», сопровождающийся выработкой чрезмерного количества провоспалительных цитокинов: TNF, IL-6 и др. Если такая реакция в организме стабильно продолжается, то возникает системное воспаление, нарушается проницаемость гематоэнцефалического барьера с дальнейшим повреждением церебральных нейронов и глиальных клеток. При тяжелом течении инфекции Covid-19 наблюдается чрезмерная выработка провоспалительных цитокинов, а у выживших пациентов сохраняются осложнения заболевания со стороны ЦНС.
Известно, что провоспалительные цитокины нарушают способность микроглиальных клеток фагоцитировать β-амилоид, при накоплении которого формируются амилоидные бляшки, и развивается болезнь Альцгеймера.
Данные нейровизуализационных исследований неоднократно демонстрировали повреждения различных структур головного мозга, связанные с новой коронавирусной инфекцией, одним из наиболее чувствительных среди которых является гиппокамп. Наиболее часто (76%) отмечалось диффузное повреждение субкортикального и глубокого белого вещества головного мозга, реже – микроинфаркты (13%), инфаркты (10%) или внутримозговые кровоизлияния (6%), а также гипоксические повреждения и очаги демиелинизации. Другими патогенетическими механизмами развития КН вследствие инфекции COVID-19 являются эндотелиальная дисфункция, коагулопатия, тромбообразование и другие нарушение гемостаза. Предполагают, что сосудистые факторы могут ухудшать течение имеющейся цереброваскулярной патологии, что в свою очередь приведет к развитию КН или ухудшению имеющегося дефицита.
Важным фактором возникновения и дальнейшего прогрессирования КН у людей во время пандемии COVID-19 является социальная изоляция и одиночество. Ограничительные мероприятия при COVID-19 приводят к изоляции людей, негативному психологическому воздействию и последствиям в виде чувства растерянности, гнева и посттравматического стресса. Одинокие пациенты, уже имеющие КН, подвергаются более высокому риску психологической декомпенсации по сравнению с теми, кто не имеет этих расстройств и живет с семьей. В исследование испанских коллег было показано значительное ухудшение эмоционального статуса и когнитивного дефицита у 40 пациентов с легкой деменцией при болезни Альцгеймера и умеренными КН после 5 недель изоляции в виде апатии, тревоги, возбуждения и аберрантного двигательного поведения, что требовало терапевтической коррекции или назначения фармакологических препаратов.
Выбор терапии пациентам с когнитивными расстройствами осуществляется в зависимости от этиологии и тяжести нарушений, как и последующее динамическое наблюдение и контроль эффективности лечения.
При недементных КН препаратами первой линии являются нейрометаболические средства с вероятным нейропротективным эффектом, тогда как при выраженном когнитивном дефиците базисную терапию составляют мемантин и/или ингибиторы ацетилхолинэстеразы.
Лекарственный препарат, содержащий фонтурацетам, Нанотропил Ново, зарекомендовавший себя как эффективное ноотропное средство в терапии когнитивных нарушений различной этиологии и купирования физической и умственно-психической утомляемости, также рассматривается в терапии пациентов с постковидными когнитивными и астеническими нарушениями. Механизм действия Нанотропила Ново связан с его положительным влиянием на обменные процессы (нейрометаболическое действие), с нейропротекторным действием, повышением уровня моноаминов (норадреналина, дофамина и серотонина) в головном мозге, влиянием на рецепторы NMDA, н-холинорецепторы и синаптическую передачу, что приводит к реализации ноотропного, антиастенического и адаптогенного действий.
В двойном-слепом плацебо-контролируемом рандомизированном исследовании у пациентов с хронической ишемией мозга I–II ст. и умеренными когнитивными нарушениями фонтурацетам в составе Нанотропил® Ново (100 и 200 мг/сут в течение 30 дней) статистически значимо в сравнении с плацебо способствовал улучшению когнитивных функций (по шкале MMSE), уменьшению астении, повышению физической и умственной активности (по шкале оценки астении MFI-20), увеличению концентрации внимания, скорости умственных процессов, эффективности работы (по тесту Шульте).
Важными стратегиями при ведении этих пациентов являются немедикаментозные методы воздействия, коррекция факторов риска и прогрессирования КН, диагностика и терапия коморбидных состояний. В частности, широко встречаемый в популяции дефицит витамина В12 значимо влияет на познавательные функции человека, вызывая потенциально обратимые КН, что обусловлено процессами демиелинизации в ЦНС и патологическими изменениями в белом веществе головного мозга (дисметаболической лейкоэнцефалопатией), нарушением структуры и трофики нервных клеток и развитием гипергомоцистеинемии. С другой стороны, при инфекции COVID-19 и дефиците витамина B12 наблюдаются схожие патогенетические механизмы развития патологического процесса в виде повышения окислительного стресса, уровня гомоцистеина и лактатдегидрогеназы, активации каскада свертывания, внутрисосудистого свертывания и тромбоза и возникновения тромбоцитопении, приводящих в итоге к поражению дыхательной системы, желудочно-кишечного тракта и ЦНС. В частности, в проведенном в Сингапуре исследовании было продемонстрировано, что применение витамина B12, наряду с витамином D и магнием, позволяло у больных с инфекцией Covid-19 достоверно уменьшить выраженность проявлений заболевания и значительно снизить потребности в кислороде и других вариантах интенсивной терапии в стационаре. Кроме того, при инфекции COVID-19 нарушается метаболизм кобаламина, что связано с дисфункцией кишечника, размножением микроорганизмов, вызывающих дефицит кобаламина и нарушение всасывания витамина В12. Таким образом, применение адекватных суточных доз витамина В12 (1000-2000 мкг/сутки на протяжении как минимум 3-х месяцев) в комплексной терапии пациентов с постковидным синдромом патогенетически оправдано и позволяет уменьшить выраженность поражения органов и систем, связанные с инфекцией COVID-19.
Немедикаментозные методы воздействия (физическая активность, когнитивный тренинг и правильное питание) особенно актуальны на начальных стадиях когнитивного дефицита – при синдромах субъективных, легких и умеренных КН. Влияние физической активности на риск КН и деменции было проанализировано в метаанализе S. Guure и соавт., 2017. В метаанализ были включены результаты 45 проспективных наблюдений длительностью от 1 до 28 лет, в которых участвовало 117410 пациентов. В результате было получено, что активный в физическом отношении образ жизни ассоциируется со снижением риска деменции на 21–24%, что статистически значимо. В наибольшей степени физическая активность снижает риск развития болезни Альцгеймера (на 29– 38%), в то время как ее влияние на риск сосудистой деменции оказалось недостоверным. Предполагается, что профилактический эффект физической активности связан со стимуляцией выработки церебральных нейротрофических факторов, что замедляет прогрессирование нейродегенеративного процесса.
Когнитивный тренинг представляет собой систематические упражнения по тренировке памяти, внимания и других высших мозговых функций, которые проводятся под руководством специалиста (обученного врача, нейропсихолога).
Когнитивный тренинг может проводиться индивидуально или в группах, с использованием компьютерных программ или без них. Считается, что когнитивный тренинг, с одной стороны, помогает пациенту адаптироваться и частично преодолеть когнитивный дефект за счет сохранных функций, а с другой стороны, непосредственно влияет на морфофункциональные основы церебральных нейрорепаративных процессов. В систематическом обзоре Buttler M. и соавт. были проанализированы результаты 11 проспективных исследований когнитивного тренинга у здоровых взрослых лиц и у пациентов с синдромом легких (умеренных) КН. Было показано, что у здоровых лиц когнитивный тренинг достоверно улучшает тренируемую функцию, в то время как у пациентов с легкими или умеренными КН – нет.
Тревожные, депрессивные расстройства и нарушение сна Быстрое распространение инфекции Covid-19 и ограниченные возможности лечения этого заболевания приводят к повышению уровня тревожности, возникновению депрессивных расстройств и нарушению сна.
Карантин, изоляция, социальная дистанция, а также эмоциональные реакции на самоизоляцию вносят весомый вклад в психологическое состояние каждого человека, нередко выражающееся неадекватным поведением, эмоциональным дистрессом и защитными реакциями, в частности, страхом, фрустрацией, чувствами гнева, одиночества, скуки, поведением избегания и злоупотреблением алкоголем. Другими негативными психологическими реакциями являются негодование, постоянное беспокойство о здоровье близких и своем, повышенная чувствительность к социальным рискам, неудовлетворенность жизнью, различные фобии, замкнутость, как и компульсивное поведение, нарушение социального поведения и полиморфные соматические симптомы.
Риск впервые выявленных психических нарушений в США в течение 14–90 дней после манифестации инфекции COVID-19 вырос примерно вдвое, а среди госпитализированных пациентов зарегистрирован высокий процент тяжелых тревожно-депрессивных состояний. С одной стороны, выявленные нарушения ожидаемы в условиях пугающей неопределенности, масштабных карантинных мер и изоляции, страха за жизнь, здоровье и экономические последствия пандемии, с другой стороны, последние годы накоплены данные о существенной роли системного воспаления в возникновении депрессивных расстройств и влиянии иммунной системы на эмоциональный фон и настроение. Согласно современным данным литературы, впервые возникшая депрессия может быть инициирована выбросом цитокинов (например, IL-6) во время активной фазы инфекции Covid-19 и уменьшается по мере нормализации уровня цитокинов, независимо от использования антидепрессантов.
При пандемии COVID-19 наблюдается специфический стрессовый синдром, названный «headline stress disorder», характеризующийся высоким эмоциональным ответом в виде выраженной тревоги и проявлениями сильного сердцебиения, нарушением сна, которые в дальнейшем могут привести к психическим расстройствам, причём уровень тревоги и стресса зависит от уровня образования, пола и возраста заболевшего. Аналогичные реакции у пациентов были выявлены при инфекциях, вызванных вирусами SARS-CoV, MERS-CoV и Эбола. Во время начальной стадии пандемии в Китае было установлено, что психологический дистресс испытывают от 7% до 53,8% населения.
В условиях пандемии инфекции COVID-19 тревожные расстройства возникают в связи с определёнными обстоятельствами:
- с угрозой заражения и тяжелого течения заболевания, что приводит к устойчивому стрессу, особенно при повышенной тревожности и наличие хронических заболеваний
- с необходимостью самоизоляции, резким изменением привычного уклада жизни, угрозой ухудшения финансового положения, резким снижением двигательной активности
- с состоянием хронического стресса отрицательно влияет на функции иммунной системы, ухудшая течение хронических заболеваний – факторов риска тяжелого течения инфекции COVID-19.
Вместе с тем, необходимо выделить несколько групп лиц, подвергающихся психологическому воздействию пандемии: медперсонал, пациенты, заболевшие инфекцией COVID-19, и пациенты с уже имеющимися ментальными расстройствами. Возникновение психопатологических расстройств у больных с новой коронавирусной инфекцией связано с несколькими причинами: с имеющейся клинической симптоматикой и прогрессированием болезни, с развитием побочных эффектов проводимого фармакологического лечения, а также с ощущением опасности, боязнью передачи вируса другим людям, социальной изоляцией, ощущением неуверенности, ненадежности, физическим дискомфортом и негативными сообщениями из средств массовой информации. Несмотря на клинически стабильное течение инфекции COVID-19, практически у всех пациентов (до 96,2%) определяются психологические проблемы и симптомы стрессорных нарушений, значимо снижающих качество жизни и нарушающих стабильность профессиональной и повседневной активности, особенно у пациентов старшего возраста. У пациентов с уже имеющимися психическими расстройствами наблюдается менее выраженный эффект лечения и высокий эмоциональный ответ на болезнь.
Показано, что медицинские работники подвергаются наибольшему риску негативного психологического воздействия при пандемиях, особенно, если они непосредственно имеют контакт с заболевшими. В частности, в 27,39%−71,5% случаев развивается стресс, в 50,4% − депрессия, в 34,0% − бессонница и в 29,04%−44,6% − тревога, причём серьезная, умеренная и легкая степень выраженности тревоги наблюдается в 2,17%, 4,78% и 16,09% случаев соответственно. Наиболее выраженные симптомы отмечались у среднего и младшего медперсонала, у женщин и лиц молодого возраста, работающих в «красной зоне». Между психологическими реакциями населения в целом и медработниками не первой линии (т.е. не работающих в красной зоне) отличий выявлено не было.
Серьезное и значимое стрессовое событие в жизни может привести к нарушению сна и циркадных ритмов, в то время как здоровый сон особенно важен для адаптивного преодоления этого кризиса и неопределенности в отношении будущего. Вирус SARS-CoV-2 рассматривается как фактор, способный разобщать фазовую синхронность циркадных ритмов, тем самым снижая их амплитуду и провоцируя развитие внутреннего десинхроноза. Одно из первых исследований, направленных на изучение влияния пандемии Covid- 19 на сон и психологические симптомы у 5 641 взрослых пациентов было проведено в Китае. Онлайн-опрос китайских исследователей на предмет инсомнии, тревожных и депрессивных нарушений во время пика распространения Covid-19 продемонстрировал выраженное влияние пандемии на сон и психологическое состояние опрашиваемых. В частности, обнаружены очень высокие показатели клинически значимой инсомнии (20%), гораздо большие, чем в предшествующей пандемии период, острого стресса (15,8%), тревоги (18,5%) и депрессии (24,5%).
Известно, что пожилые люди имеют значительно более высокую распространенность синдрома обструктивного апноэ во сне, что может увеличить число негативных исходов в этой популяции, поскольку у этих пациентов существует предрасположенность к ухудшению гипоксемических состояний и сердечно-сосудистых событий, увеличивающих в свою очередь вероятность негативных респираторных и сердечных исходов инфекции COVID-19. Вместе с тем, метаанализ 55 исследований c участием 189 159 человек продемонстрировал большую на 23,87% распространенность расстройства сна во время пандемии, независимо от имеющегося диагноза коронавирусной инфекции.
Особенности сна, характерные для пожилых людей, могут лежать в основе их повышенной восприимчивости к инфекции COVID-19 и тяжести заболевания. Пандемия и все связанные с ней обстоятельства (изоляция, социальное дистанцирование, чувство одиночества и т.д.) могут вызвать нарушение сна, как и хронизировать в дальнейшем инсомнию, кроме того, с учётом возможных долгосрочных последствий пандемии для психического здоровья, большая вероятность стойких расстройств сна у ряда людей даже после окончания пандемии, что особенно верно для пожилых людей из-за уровня одиночества и самоизоляции в этих случаях.
Двунаправленные связи между нарушением сна и коронавирусной инфекцией заключаются в следующем:
- имеющаяся инсомния может увеличить вероятность заражения SARS-COV-2
- инсомния может негативно повлиять на прогноз и исходы инфекции COVID-19
- социальная изоляция, карантин и самоизоляция пожилых людей, связанные с инфекцией COVID-19 также могут негативно влиять на сон.
Вирус SARS-CoV-2 способен значимо разобщать фазовую синхронность циркадианных ритмов и приводить к внутреннему десинхронозу, при этом лица пожилого возраста, пациенты с нейродегенеративными заболеваниями и синдромом обструктивного апноэ во сне находятся в группе высокого риска по восприимчивости к этому инфекционному агенту и развитию тяжелой формы инфекции COVID-19. Наиболее значимым последствием недосыпания при инфекции COVID-19 является нарушение иммунного ответа (как врожденного, так и приобретенного), что приводит к иммуносупрессии и увеличению риска вирусных и оппортунистических инфекций. Поэтому нормализация сна является значимой и необходимой терапевтической стратегией как у пациентов с инфекцией COVID-19, так и у людей, находящихся в группе риска развития инсомнии.
Терапия пациентов с аффективными нарушениями и нарушением сна включает нелекарственные и фармакологические методы воздействия.
Среди нелекарственных методов терапии рассматриваются: лечебная физкультура, различные виды психотерапии (рациональная, телесно ориентированная, арт-терапия, групповая) и такие релаксационные методики, как аутогенная тренировка или биологическая обратная связь.
Психофармакотерапевтическое воздействие включает назначение лекарственных средств из группы анксиолитиков, антидепрессантов и нейролептиков, способствующих уменьшению (или редукции) соматовегетативных и других нарушений, обусловленных тревожной или депрессивной симптоматикой. В частности, назначая антидепрессанты соматическим больным, необходимо учитывать феноменологические особенности тревожного или депрессивного расстройства и психическое состояние больного в целом; дополнительные клинические эффекты назначаемого антидепрессанта, а именно: нейротропный, вегетотропный, аналгетический, седативный, анорексигенный и т.д.; отсроченное начало антидепрессивного действия - обычно 2-3 неделя; у пожилых приблизительно в два раза медленнее (к 6-8 неделе), что требует избежать преждевременной отмены препарата (из-за отсутствия клинического эффекта) и частой смены препаратов; индивидуальность дозы и длительность терапии. Учитывая повышенную чувствительность соматических больных к препаратам этой группы, им обычно назначается более щадящий режим терапии, чем при обычных эндогенных депрессиях. Эффективная терапевтическая доза у соматических больных, как правило, в два раза ниже, чем у психиатрических, при этом длительность приема антидепрессантов после регресса симптомов не должна быть меньше 4-5 месяцев во избежание развития ранних рецидивов; по возможности, минимальность взаимодействия антидепрессанта с другими препаратами; безопасность препарата при передозировке (включая случайную); простота режима приема, что значительно увеличивает приверженность больных лечению.
На сегодняшний день накоплены данные эффективного использования алимемазина (Тералиджен) у пациентов с различной степенью тяжести инфекции COVID-19. В частности, у 324 больных с подтвержденным диагнозом COVID-19 различной степени тяжести и психоэмоциональными расстройствами (тревожно-депрессивными, фобическими, обсессивно-компульсивными, вегетативными и нарушениями сна) применение в составе комбинированной терапии Тералиджена (5-10 мг в сутки в течение 10-20 дней) в стационаре и амбулаторных условиях позволило быстро и эффективно купировать имеющиеся нарушения, в том числе в случаях резистентности к другим лекарственным средствам, что безусловно важно для своевременной коррекции психоэмоциональных расстройств у данной категории пациентов.
Тералиджен – анксиолитическое и седативное средство. Оказывает мультимодальное действие, воздействуя на различные типы рецепторных систем (α-адренергическую, Н1-гистаминовую, серотониновую, D2-дофаминовую, М-холинергическую). Тералиджен обладает анксиолитическим, седативным, гипнотическим, вегетостабилизирующим и антигистаминным эффектами. Препарат уменьшает возбуждение, тревогу, фобию, беспокойство, агрессию, вегетативные/соматоформные и др. симптомы. Может применяться на различных этапах лечения пациентов с COVID-19 для коррекции широкого спектра заболеваний с психоэмоциональными, поведенческими, невротическими, вегетативными расстройствами, бессонницей, а также аллергическими реакциями различного генеза.
Тералиджен (5-10 мг/сут в течение 10-20 дней) оказался эффективным для быстрого купирования нозогенных психических реакций, тревожно-фобических и вегетативных симптомов и гиперсимпатикотонии. Тералиджен® наряду с очевидным противотревожным и вегетолитическим эффектом, показал клинически сбалансированный снотворный, седативный и антигистаминный эффект.
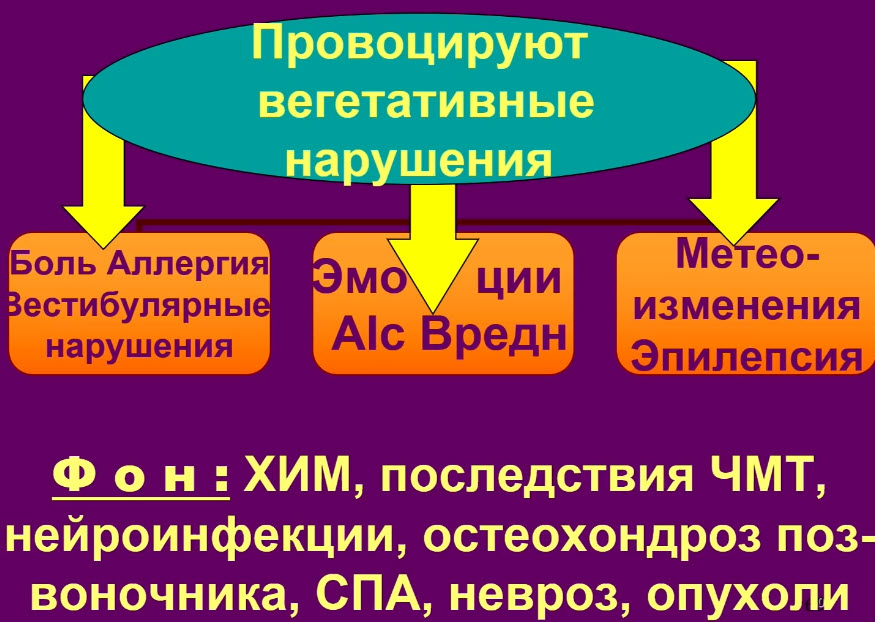
Вегетативные нарушения
В настоящее время пристально изучаются механизмы влияния вируса SARS-CoV-2 на вегетативную нервную систему. Взаимосвязь между ними очевидна, поскольку хорошо известный «цитокиновый шторм» при инфекции COVID-19 является результатом симпатической активации и высвобождения провоспалительных цитокинов. Вегетативная дисфункция, связанная с COVID-19, может быть опосредована как самим вирусом, так и иммунным ответом организма, в частности, ортостатическая гипотензия обусловлена выработкой аутоантител к ɑ-, b-адренорецепторам и мускариновым рецепторам, что позволяет предположить аутоиммунный компонент хронической инфекции COVID-19.
Показано, что коронавирус может также поражать вегетативную нервную систему. Вегетативные нарушения после перенесённой инфекции Covid-19, обусловленные недостаточностью или избыточной активностью симпатических или парасимпатических систем, на сегодняшний день недостаточно изучены, вместе с тем, наблюдается широкий спектр их клинических проявлений, представленность которых, по данным разных авторов, составляет от 2,5% до 26% случаев. В частности, в периоде реконвалесценции у 26% пациентов наблюдается нарушение потоотделения. У больных вследствие инфекции COVID-19 отмечается сочетанное возникновение гипергидроза и постуральной ортостатической тахикардии с устойчивым увеличением частоты сердечных сокращений ≥30 ударов в минуту в течение 10 минут после нахождения в вертикальном положении. Среди нарушений ритма сердца, связанных с вегетативными нарушениями вследствие коронавирусного заболевания, выделяют также синусовую тахикардию и другие варианты наджелудочковой тахикардии, а также, согласно данным метаанализа, устойчивое повышение артериального давления в периоде реконвалесценции.
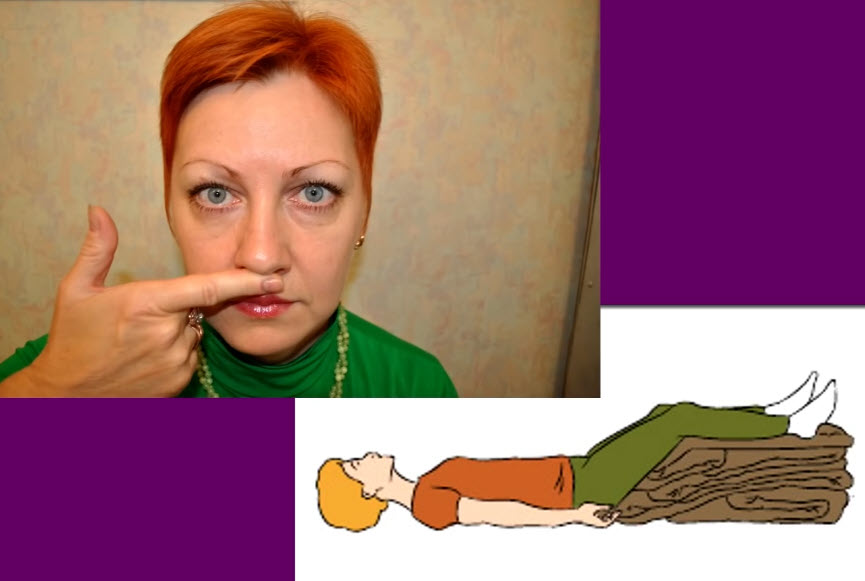
Пациентам, перенесшим COVID-19, нередко необходима скрининговая диагностика нарушений вегетативной нервной системы как отдельного осложнения данного заболевания, значимо влияющего на течение и прогноз патологического состояния. Следует тщательно обследовать всех лиц, у которых наблюдаются одышка, учащенное сердцебиение, усталость, боль в области груди, липотимические и синкопальные состояния. С этой целью применяют инструментальные методы исследования, включающие несколько простых неинвазивных кардиоваскулярных тестов, предложенных в конце 1970- х годов и до сих пор являющихся классическим методом диагностики поражения вегетативной нервной системы: тест «глубокое дыхание», тест Вальсальвы, тест «30/15», ортостатическая проба и тест с использованием изометрической нагрузки. Симпатическую дисфункцию выявляют два основных теста, основанных на изменениях артериального давления: систолический (ортостатическая проба) и диастолический (тест с использованием изометрической нагрузки). Для оценки нарушений парасимпатической иннервации сердца применяются тест «глубокое дыхание», тест Вальсальвы, тест «30/15», основанные на принципах фотоплетизмограммы и выполняющиеся с помощью пульсоксиметра.
Дизавтономия вегетативной нервной системы (ДВНС) - это недостаточность или, напротив, повышенная активность симпатических или парасимпатических компонентов вегетативной нервной системы, имеет широкий спектр клинических проявлений, включая колебания артериального давления, ортостатическую гипотензию, импотенцию, дисфункцию мочевого пузыря и изменения функций кишечника. Острая дизавтономия наблюдается при вирусных инфекциях: при эпидемическом паротите, гепатите С, инфекционном мононуклеозе и ВИЧ, хроническая дизавтономия - при таких заболеваниях, как сахарный диабет, болезнь Паркинсона, алкоголизм и синдром Гийена-Барре. И достаточно часто у пациентов, перенесших инфекцию COVID-19, наблюдается ДВНС, при которой изменения в функционировании одного и более компонента вегетативной нервной системы отрицательно сказываются на здоровье, в частности, нарушение функции желудочно- кишечного тракта: боль и вздутие живота, гастропарез и тошнота или постуральная ортостатическая тахикардия с устойчивым увеличением частоты сердечных сокращений ≥30 ударов в минуту в течение 10 минут после стояния или наклона головы вверх. Кардиологические проявления могут включать боль в груди, выраженные колебания артериального давления (гипертонические кризы, чередующиеся с эпизодами гипотензии), непереносимость физических упражнений и непереносимость ортостаза. Возможными механизмами возникновения ДВНС после инфекции COVID-19 являются повреждение афферентных барорецепторных путей, начиная с барорецепторов в каротидных телах и заканчивая волокнами блуждающего, языкоглоточного нервов и одиночного ядра тракта, поскольку эти области имеют сильную экспрессию ACE2, и нарушение аутоиммунитета. Предполагается, что острая дизавтономия в виде гемодинамической нестабильности, наблюдаемая у больных с инфекцией COVID-19, находящихся в критическом состоянии, может быть объяснена изначальной недостаточностью афферентного барорефлекса, вторичной по отношению к инфекции SARS-COV-2 и вторжению вируса в вышеуказанные церебральные структуры. В группу риска возникновения ДВНС после перенесенной коронавирусной инфекции входят подростки в пубертатном возрасте во время гормональной перестройки, женщины с изначальной лабильностью вегетативной нервной системы и лица с хроническими сердечно-сосудистыми и аутоиммунными заболеваниями.
Лечение вегетативных нарушений у пациентов, перенесших инфекцию COVID-19, включает немедикаментозные и фармакологические направления, в частности, лекарственные средства, подавляющие каскад метаболических и сосудистых нарушений, блокирующие основные пути повреждения нервной системы при COVID-19 и стимулирующие регенеративные нейропластические процессы. Окислительный стресс, активация перекисного окисления липидов, индуцибельной NO-синтазы приводят к избыточному образованию свободных радикалов – молекул, обладающих повышенной реагентной способностью и нарушающих целостность клеточных структур, в первую очередь эндотелия, что вызывает эндоневральную гипоксию и, как следствие, развитие повреждение вегетативной нервной системы. Именно поэтому препараты с таргетным воздействием на указанные процессы являются перспективными для использования в качестве средства патогенетической терапии при вегетативной дисфункции вследствие инфекции COVID-19.
Немедикаментозное лечение ортостатической гипотензии, развившейся у пациента с инфекции COVID-19, должно включать:
- увеличение потребления жидкости в течение дня (2,5 л/сут) и соли (10–20 г/сут), особенно в первой половине дня
- избегание резких переходов в вертикальное положение из положения лежа или сидя, длительного пребывания в стоячем положении и воздействия высоких температур (баня, сауна, горячий душ или ванна)
- ношение компрессионных чулок, бандажа на животе при ходьбе и длительном стоянии, перекрещивание ног в стоячем положении и поднятие головного конца кровати на время сна на 15–23 см
- исключение алкоголя и препаратов, усугубляющих течение ортостатической гипотензии (α- и β-адреноблокаторов, ингибиторов ангиотензинпревращающего фермента, нитратов, блокаторов кальциевых каналов, диуретиков, агонистов дофаминовых рецепторов, опиоидов, миорелаксантов и трициклических антидепрессантов).
При выраженной ортостатической гипотензии и отсутствии артериальной гипертензии лежа возможно применение лекарственных средств, увеличивающих объем циркулирующей крови (минералокортикостероидов или агонистов α-1-адренорецепторов). Важно заметить, что сразу после перенесенной инфекции COVID-19 рекомендовано ограничить тяжелые физические нагрузки с акцентом на дозированную физическую активность и лечебную ходьбу.
Лечение пациентов с инфекцией COVID-19 проводится в соответствии с национальными клиническими рекомендациями, учитывающими особенности патогенеза и течения заболевания, при этом в настоящее время не существует каких-либо алгоритмов или рекомендаций, основанных на принципах доказательной медицины, по лечению неврологических нарушений у этой категории больных. Не в лучшем положении оказываются пациенты, изначально имеющие поражение нейрональных систем головного мозга, в частности, цереброваскулярные заболевания и как следствие – хроническую ишемию головного мозга.
У 304 пациентов с сочетанным поражением головного мозга было продемонстрировано успешное применение этилметилгидроксипиридина сукцината - препарата мексидол, длительная последовательная терапия которого (500 мг (10 мл) на 400 мл физиологического раствора внутривенно капельно - 14 дней с последующим пероральным приемом 250мг 3 раза в день - 2 месяца) обеспечивала статистически значимое улучшение нарушенных функций: более полное и раннее восстановление состояния когнитивной сферы (по шкале МоСА, p<0,01), регресс астенических проявлений (по шкале MFI-20, p<0,05) и нормализацию сна (по опроснику Шпигеля, p<0,01).
Антигипоксантные, антиоксидантные и мембранопротекторные свойства, как и полимодальные механизмы действия этилметилгидроксипиридина (мексидол), позволяют таргетно воздействовать на базисные патологические процессы в клеточных структурах органов и тканей организма, возникающих при широком спектре различных гипоксических состояний, в том числе, при инфекции COVID-19.
Таким образом, терапия пациентов с постковидными нарушениями осуществляется, исходя из ранее имеющегося клинического опыта и данных клинических исследований больных с инфекций COVID-19, накопленных за последние полтора года.