Лекция для медицинских сестер "Требования к обращению с медицинскими отходами. Классификация медицинских отходов" (отрывок из книги "Основы сестринского дела: практикум" - Т. П. Обуховец)
Требования к обращению с медицинскими отходами
В настоящее время сбор, использование, обезвреживание, размещение, хранение, транспортировка, учет и утилизация медицинских отходов должны осуществляться с соблюдением требований СанПиНа 2.1.3684-21 «Санитарно-эпидемиологические требования к содержанию территорий городских и сельских поселений, к водным объектам, питьевой воде и питьевому водоснабжению, атмосферному воздуху, почвам, жилым помещениям, эксплуатации производственных, общественных помещений, организации и проведению санитарно-противоэпидемических (профилактических) мероприятий» (вступ. в силу с 21.03.2021 г. сроком на 6 лет).
Требования к обращению с медицинскими отходами зависят от степени их эпидемиологической, токсикологической и радиационной опасности, а также негативного воздействия на человека и среду обитания человека. Эти Требования регламентируют наличие в составе МО соответствующих помещений, площадок для временного хранения медицинских отходов, а также сооружений по их термической утилизации. В связи с этим на территории всех МО организована система сбора, временного хранения и транспортирования отходов, а в каждом медицинском подразделении назначено ответственное лицо, которое непосредственно на местах первичного сбора отходов должно осуществлять контроль за обращением с отходами и герметизацию одноразовых емкостей (пакетов, баков).
Классификация медицинских отходов МО
Все отходы МО делятся на пять классов. Вся продукция, обеспечивающая систему классификации отходов по классу опасности, промаркирована, взаимно сочетается и обозначена тем же цветом, что и класс опасности отходов.

Вы читали отрывок из книги "Основы сестринского дела: практикум" - Т. П. Обуховец
Дополнительный материал
Виды, методы, уровни дезинфекции
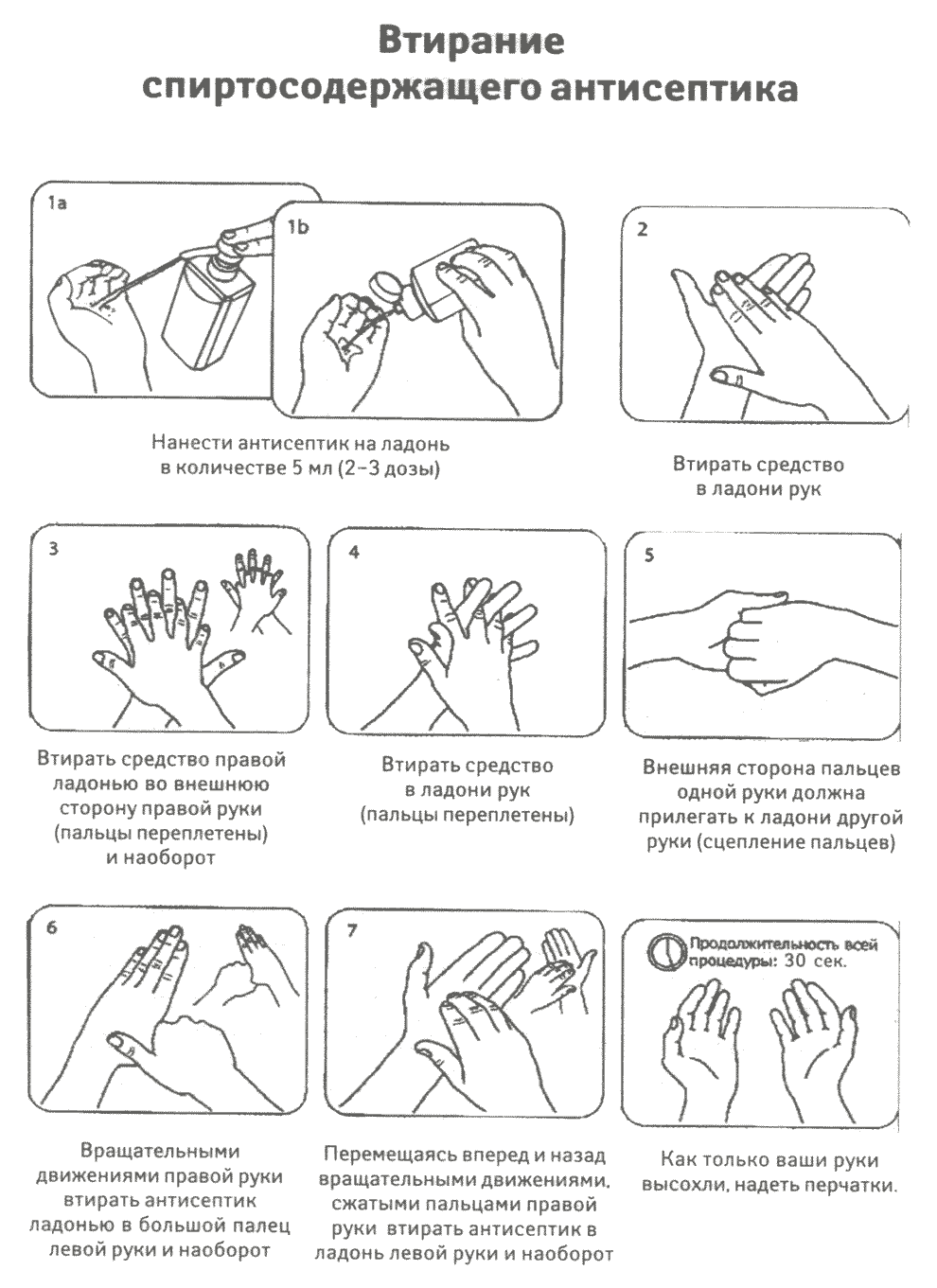
Гигиенический уровень обработки рук
Книга "Основы сестринского дела: практикум"
Автор: Т. П. Обуховец

Учебное пособие составлено в соответствии с ФГОС СПО третьего поколения и требованиями междисциплинарных курсов (МДК) "Выполнение работ по профессии Младшая медицинская сестра по уходу за больными" по специальностям СПО и направлено на формирование профессиональных компетенций у будущих специалистов среднего медицинского звена.
Практикум состоит из двух разделов:
1. "Безопасная среда для пациента и персонала" (МДК 02). В настоящее время вступили в силу новые Санитарные правила и нормы (сокращенно СанПиНы) как основа законодательства: СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", а также другие нормативные документы, в том числе регламентирующие документы по коронавирусной инфекции, обеспечивающие проведение работ с соблюдением современных требований инфекционной безопасности. В этом разделе рассмотрены также вопросы эргономики, биомеханики движений тела медицинского персонала и пациента и представлены методики при обращении с пациентом как на дому, так и в условиях стационара.
2. "Технология оказания медицинских услуг" (МДК 03). Рассматриваются вопросы по оказанию медицинских услуг в пределах своих полномочий, реализации сестринских вмешательств в критической ситуации, осуществления ухода за пациентами различных возрастных групп в условиях медицинской организации и на дому.
Пособие включает схемы, рисунки, иллюстрации, таблицы, задания для самостоятельной работы, тесты, составленные по материалам действующих нормативных документов профессиональной деятельности среднего звена.
Содержание книги "Основы сестринского дела: практикум" - Т. П. Обуховец
Раздел I. МДК 02. Безопасная среда для пациента и персонала
Терминология к I разделу ПМ 04 (МДК 02)
Обеспечение безопасности медперсонала и пациентов
Факторы, влияющие на безопасность пациента и персонала в лечебно-профилактической медицинской организации
Факторы риска в работе сестринского персонала
Соблюдение стандартных мер по созданию безопасной среды для медицинского персонала
Факторы, влияющие на пациента в условиях больничной среды
Проведение работ по соблюдению требований инфекционной безопасности
Понятие об инфекции, связанной с оказанием медицинской помощи (ИСМП)
Основы классификации ИСМП
Классификация инфекций
Источники передачи ИСМП
Типичные места обитания ИСМП
Систематика микроорганизмов, связанных с оказанием медицинской помощи
Пути и механизмы передачи ИСМП
Заболевания, связанные с ИСМП
Основы профилактики ИСМП в медицинских организациях
Основные требования профилактических и противоэпидемических мероприятий
Задачи по профилактике ИСМП для медицинского персонала
Меры контроля и безопасности на рабочем месте в МО
Рекомендации пациенту по соблюдению общих мер профилактики ИСМП
Мытье рук на социальном, гигиеническом, хирургическом уровнях
Уровни деконтаминации рук
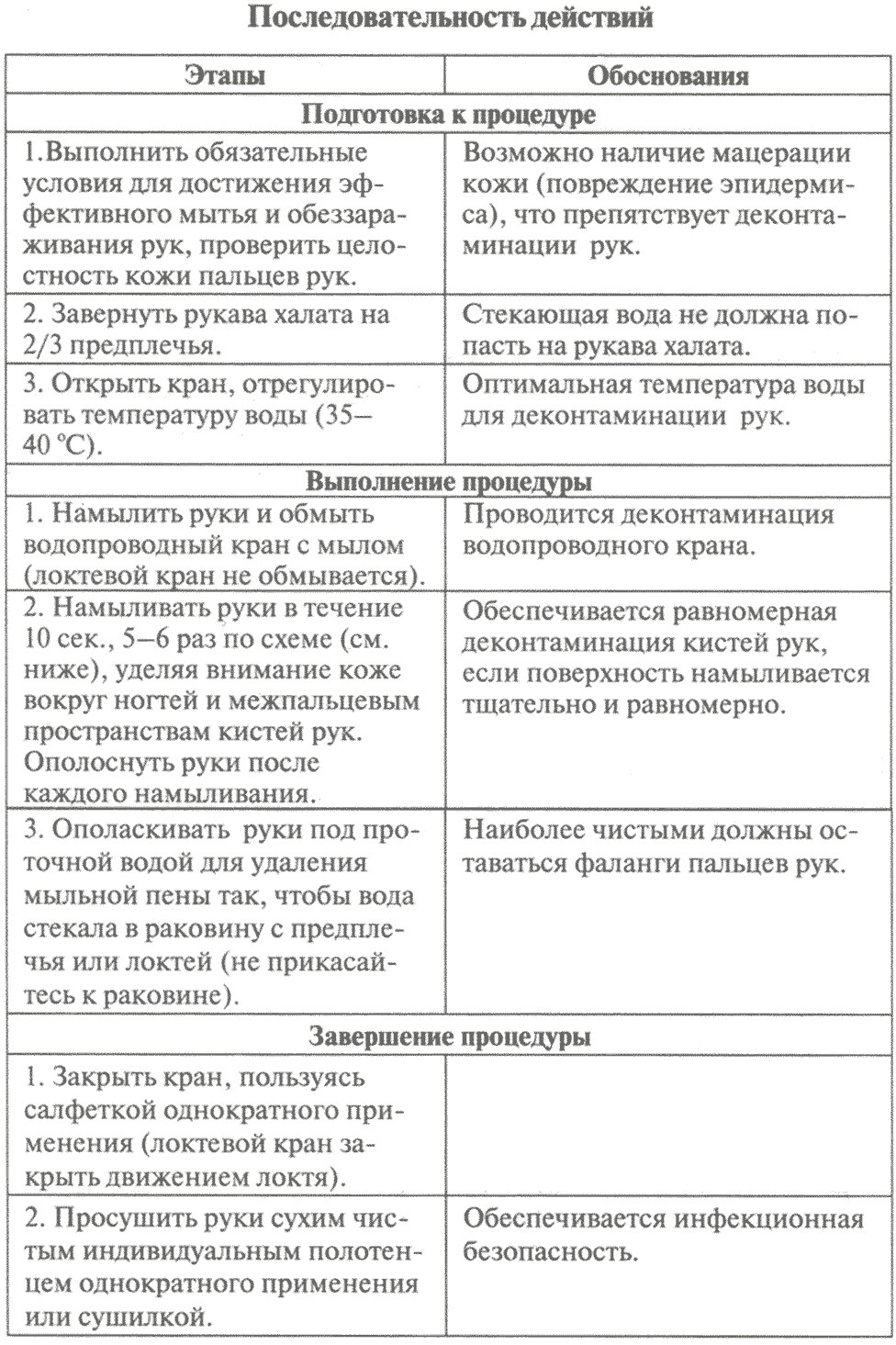
Обычное мытье рук (социальный уровень)
Обеззараживание рук медицинского работника и кожных покровов пациентов при оказании медицинской помощи Кожные антисептики, их классы
0сновы сестринского дела: практикум
Характеристика кожных антисептиков
Использование дозаторов
Гигиенический уровень обработки рук
Использование санитарной одежды (спецодежды) и индивидуальных средств защиты
Использование медицинских перчаток
Оснащение рабочего места адекватно виду выполняемых работ
Основы дезинфекционной деятельности
Виды, методы, уровни дезинфекции
Виды дезинфекции
Методы и способы дезинфекции
Уровни дезинфекции
Характеристика основных средств дезинфекции по группам (классам) химических соединений
Правила охраны труда при работе с дезинфицирующими средствами
Правила оказания помощи при попадании средств дезинфекции на кожные покровы и слизистые
Средства проведения дезинфекционных мероприятий
Требования к оборудованию для дезинфекции
Требования к выбору дезинфицирующих средств
Пользование методическими указаниями к средствам дезинфекции, ПСО и стерилизации
Структура методических указаний
Виды контроля пригодности дезинфицирующих средств Виды дезинфицирующих средств, требования к ним
Техника приготовления дезинфицирующих растворов
Особенности применения дезинфицирующих средств
Экспресс-контроль содержания действующих веществ в рабочих растворах дезинфектантов
Требования к обращению с медицинскими отходами
Классификация медицинских отходов МО
Требования к сбору медицинских отходов
Сбор первичных медицинских отходов в мягкую упаковку
Сбор медицинских отходов в твердую упаковку
Хранение и транспортировка отходов МО
Способы утилизации отходов МО
Дезинфекция предметов ухода, способы дезинфекции
Действия медицинского работника в аварийной ситуации
Особенности гигиенической уборки помещений МО
Проведение профилактической дезинфекции в МО
Схема проведения генеральной уборки процедурного кабинета Бельевой режим стационара ПО
Предстерилизационная очистка (ПСО) изделий медицинского назначения
Понятие о стерилизации
Понятие об автоклавировании
Применение стерилизационных упаковок
Методы стерилизации, режимы, сроки стерильности
Виды контроля проведения дезинфекционных и стерилизационных мероприятий
Подготовка перевязочного материала для стерилизации (салфеток, тампонов, шариков, турунд)
Порядок работ по соблюдению инфекционной безопасности и техники безопасности при выполнении простых медицинских услуг
Соблюдение мер безопасности при обращении с пациентом
Понятие о лечебно-охранительном режиме, его элементы, значение
Режимы двигательной активности пациента
Виды положения пациента в постели
Стандартные меры по созданию безопасной больничной среды для пациента
Основы эргономики
Понятие о биомеханике движений тела человека
Организация эргономичного рабочего места
Биомеханика тела медицинского персонала при перемещении тяжестей
Методики обращения с пациентами
Подготовка к перемещению
Размещение пациента в постели
Безопасное «перекатывание» пациента в постели
Особенности безопасной транспортировки в МО
Транспортировка на носилках
Способы перекладывания тяжелобольных пациентов
Методики безопасного перемещения пациента одной медсестрой
Перемещение пациента двумя медицинскими сестрами
Проведение занятий медицинской сестрой по обучению пациента самоуходу
0сновы сестринского дела: практикум
Раздел II. МДК 03. Технология оказания медицинских услуг
Термины и понятия
Оказание медицинских услуг
Оценивание показателей здоровья пациента
Проведение термометрии, способы измерения температуры тела
Проведение антропометрических исследований
Наблюдение за дыханием
Измерение суточного диуреза и определение водного баланса
Оказание медицинских услуг при приеме пациента в стационар
Устройство и функции приемного отделения стационара
Поступление пациента в стационар
Проведение полной санитарной обработки пациента
Осуществление полной/частичной санитарной обработки пациента
Способы транспортировки пациента в отделение стационара
Осуществление ухода за пациентами различных возрастных групп в условиях учреждения здравоохранения и на дому
Проведение гигиенического ухода
Приготовление постели пациенту
Смена постельного и нательного белья
Смена постельного белья продольным способом (выполняется одной медсестрой)
Смена постельного белья поперечным способом (выполняется двумя медсестрами)
Смена нательного белья пациенту с поврежденной рукой (выполняется двумя медсестрами или одной медсестрой)
Подача подкладного судна тяжелобольному пациенту (пособие при акте дефекации, выполняют медсестра и помощник)
Уход за кожей и влажное обтирание пациента
Подмывание тяжелобольного
Проведение профилактики пролежней
Причины возникновения пролежней
Места образования пролежней
Оценка риска развития пролежней по шкале Ватерлоу
Оценка степени тяжести пролежней
Уход и профилактика пролежней
Выбор противопролежневых матрацев и вспомогательных приспособлений
Возможные проблемы пациента, их решение
Пример составления памятки для пациентов
Пример составления памятки для родственников пациента по профилактике пролежней
Пример расчета дневного рациона питания с целью профилактики пролежней
Соблюдение личной гигиены пациента
Уход за полостью рта
Уход за глазами
Уход за носом
Уход за ушами
Уход за волосами
Мытье ног в постели тяжелобольному
Лечебное питание и кормление пациента
Основные принципы лечебного питания
Основные принципы приготовления лечебных диет
Режим питания
Организация лечебного питания
Планирование необходимой помощи пациенту при возникновении проблем, связанных с кормлением
Методики искусственного кормления пациента
Лекарственная терапия в сестринской практике
Порядок применения лекарственных средств
Способы (пути) введения лекарственных средств
Применение лекарств наружно
Введение лекарственных средств в глаза, нос, уши
Туалет полости носа взрослого пациента с помощью масляных растворов
Закапывание капель в глаза
Закапывание сосудосуживающих капель в нос
Закладывание мази за веко из тюбика
Введение мази в нос
Введение порошка в нос
Введение капель в наружный слуховой ход
Смазывание слизистой глотки
Проведение орошения глотки
Ингаляторное введение лекарственных средств
Применение увлажненного кислорода
Механизм действия оксигенотерапии
Способы оксигенотерапии
Применение систем подачи кислорода
Ингаляторное введение кислорода через носовой катетер с канюлями
Проведение оксигенотерапии с помощью носоглоточного катетера
Проведение оксигенотерапии с помощью кислородной подушки
Подача увлажненного кислорода из кислородной подушки
Осложнения при применении оксигенотерапии
Опасные факторы и меры безопасности при работе с кислородом
Применение лекарственных средств энтерально
Применение нитроглицерина или валидола сублингвально
Применение суппозитория со слабительным действием ректально
Введение лекарственных средств парентерально
Выполнение парентеральных процедур
Сборка шприца однократного применения для инъекции
Набирание в шприц лекарственного средства из ампулы
Набирание в шприц лекарственного средства из флакона
Выполнение внутрикожной инъекции
Выполнение подкожной инъекции
Расчет и введение гепарина инъекционным способом
Профилактика осложнения: кровотечения
Особенности введения инсулина подкожно
Выполнение внутримышечных инъекций
Методики разведения антибиотиков
Стандартный метод разведения
Концентрированный метод разведения
Расчет, разведение и введение антибиотиков внутримышечно
Введение масляных растворов внутримышечно
Введение лекарственных средств внутривенно (струйно)
Введение лекарственных средств внутривенно (капельно)
Особенности введения сильнодействующих растворов сердечных гликозидов
Осложнения при парентеральном применении лекарственных средств
Помощь при анафилактическом шоке
Осложнения при парентеральном введении цитостатиков, их профилактика
Совместимость лекарственных средств
Соблюдение мер профилактики осложнений лекарственной терапии
Применение простейших физиотерапевтических процедур.
Трудотерапия
Понятие простейшей физиотерапии
Постановка медицинских банок
Виды компрессов
Применение грелки
Подача пузыря со льдом
Применение горчицы
Применение гирудотерапевтических технологий
Применение медицинских пиявок
Промывание желудка с применением толстого зонда
Помощь при рвоте
Постановка очистительной клизмы
Постановка лекарственной клизмы
Постановка гипертонической микроклизмы
Постановка масляной микроклизмы
Применение сифонной клизмы
Постановка лекарственной клизмы
Проведение катетеризации мочевого пузыря
Принципы ухода за мочевым катетером
Катетеризация мочевого пузыря женщине
Катетеризация мочевого пузыря мужчине
Уход за промежностью пациента (пациентки) с мочевым катетером
Пособие при стомах
Трахеостома
Стомы пищеварительного тракта
Гастростома
Свищи кишечника — еюностома, илеостома, колостома
Применение калоприемников
Обучение пациента уходу за стомой (колостомой)
Эпицистома
Промывание мочевого пузыря (ирригация) через эпицистостому
Подготовка к лабораторным и инструментальным методам исследования
Лабораторные исследования, их этапы
Типы и виды клинических анализов
Первый преаналитический этап лабораторных исследований
Исследования проб венозной крови
Исследования мокроты
Забор материала из зева
Забор материала из носа
Забор материала на менингококк из носоглотки
Исследования мочи
Исследования кала
Инструментальные методы исследования
Рентгенологические методы исследования, их виды
Подготовка пациента к рентгенологическим исследованиям
Пероральная холецистография
Холеграфия
Ирригоскопия
Внутривенная (экскреторная) пиелография
Эндоскопические исследования
Бронхоскопия
Фиброгастродуоденоскопия
Ректороманоскопия
Колоноскопия
Эндоскопические исследования в урологии
Цистоскопия
Этапы проведения дезинфекции и стерилизации эндоскопов, не проникающих в стерильные полости организма
Возможные осложнения при проведении эндоскопических исследований
Ультразвуковые исследования
УЗИ-эхография
Положения пациента при УЗИ
Узи органов брюшной полости
Узи с определением сократительной способности желчного пузыря
Узи органов малого таза
Узи почек, сердца и сосудов
Реализация сестринских вмешательств в критической ситуации
Сердечно-легочная реанимация вне лечебного учреждения
Оказание первой помощи в случае клинической смерти Понятие о первичном реанимационном комплексе
Действия спасателя в экстремальной ситуации
Определение наличия обструкции дыхательных путей
Первый способ искусственного дыхания одним реаниматором
Восстановление свободной проходимости дыхательных путей
Оказание первой помощи при обструкции дыхательных путей инородным телом пострадавшему в сознании, без сознания, с избыточной массой тела, беременным
Проведение сердечно-легочной реанимации пострадавшему одним и двумя спасателями
Закрытый (непрямой) массаж сердца (ЗМС) у взрослых и пожилых
Полный цикл сердечно-легочной реанимации (СЛР) вне медицинских учреждений
Терминальные состояния, их виды
Сестринская практика в адаптации тяжелобольного человека к возникшему качеству жизни
Принципы обслуживания пациентов в условиях хосписа
Потери, смерть, горе
Стадии траура
Посмертный уход
Приложения
Задания для самоподготовки
Эталоны ответов на задания для самоконтроля
Литература