Маммография при клиническом подозрении на рак молочной железы. Лекция для врачей
Лекция для врачей "Маммография при клиническом подозрении на рак молочной железы" (отрывок из книги "Основы и принципы онкопластической хирургии при раке молочной железы" - Матрай З., Гуляш Г., Ковач Т. И.)
Рекомендации по скринингу рака молочной железы
Международные исследования показали, что ранняя диагностика рака молочной железы и раннее лечение до появления клинических симптомов позволяют снизить смертность от заболевания. Результаты хорошо организованных программ скрининга, прошедших профессиональную проверку, с приверженностью не менее 70 % популяции показывают, что смертность от рака молочной железы может быть снижена более чем на 20—30 %. Было показано, что одним из наиболее важных факторов прогноза рака молочной железы является размер опухоли, который имеет линейную связь с риском метастазирования. Снижающий смертность эффект скрининга рака молочной железы можно объяснить двумя факторами. Во-первых, инвазивные опухоли, выявленные в результате скрининга, меньше, а во-вторых, распространенность рака на поздней стадии (III—IV) также значительно меньше в странах, где программы скрининга работают. Во время скрининга выявляется больше поражений in situ (протоковой карциномы in situ, DCIS), которые можно рассматривать как этап-предшественник формирования инвазивного рака. Лечение прошедших скрининг пациентов мультидисциплинарной командой дополнительно улучшает прогноз.
Скрининг рака молочной железы проводится у женщин, не имеющих симптомов болезни, с помощью рентгеновской маммографии, которая, несмотря на известные ограничения, до сих пор является основным диагностическим инструментом для выявления рака молочной железы. Снижение смертности от рака молочной железы может быть лучше всего достигнуто с помощью организованного маммографического скрининга. Клинические требования можно найти в Европейских руководящих принципах обеспечения качества при скрининге и диагностике рака молочной железы, четвертое обновленное издание которого было выпущено в 2006 г. Цель этого руководства заключается в том, чтобы региональный и международный скрининг проводился на уровне Европейского союза в соответствии со стандартизированными научно подтвержденными критериями. Квалифицированный специалист проводит медицинский осмотр после записи анамнеза и любых симптомов, а затем приступает к выполнению снимка обеих молочных желез в 2 проекциях. Изображения оцениваются двумя рентгенологами, независимо друг от друга. Пациенты с аномальными случаями вызываются для дополнительных исследований (прицельная увеличенная визуализация, тонкоигольная аспирационная биопсия под УЗ-навигацией (ТАБ) или трепан-биопсия под УЗ-навигацией, магнитно-резонансная маммография (МРМ) в диагностическом блоке, используемом программой скрининга, где дальнейшая оценка происходит в соответствии с клиническим маммографическим алгоритмом (рис. 4.1).
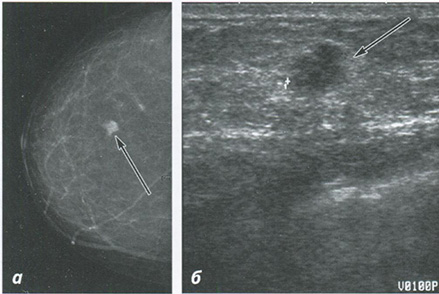
Рис. 4.1. Изображение скрининговой маммограммы (краниокаудальная проекция).
Плотное новообразование с неровным контуром в молочной железе с признаками жировой инволюции (а) (BIRADS4C). УЗ-изображение ткани молочной железы. Асимметричное новообразование с неровным нечетким контуром, гипоэхогенное. Вероятна злокачественная природа новообразования (б)
В тех случаях, когда есть подозрение на злокачественную опухоль, и в подтвержденных случаях лечение пациента осуществляется многопрофильной группой, состоящей из рентгенолога, патолога, цитолога, хирурга, онколога-химиотерапевта и радиотерапевта. Технические аспекты, относящиеся к обеспечению качества, организовываются рентген-лаборантами. Наиболее важные качественные показатели программы скрининга: посещаемость, частота повторного вызова, частота биопсии и репрезентативность выборки, количество выявленных ранних заболеваний, число диагностированных злокачественных опухолей менее 15 мм, соотношение неинвазивных (DCIS) карцином и инвазивных опухолей, соотношение злокачественных и доброкачественных опухолей в случаях хирургического лечения, ложноположительные и ложноотрицательные заключения (частота интервального рака) и состояние лимфатических узлов.
Распределение стадий опухоли, тип проведенных хирургических вмешательств и вид послеоперационного лечения являются хорошими показателями эффективности скрининга. Ожидаемые значения основаны на результатах рандомизированных исследований, и они дают критерии соответствия требованиям, предъявляемым качеству программ скрининга.
Скрининг в группах высокого риска
Женщины, принадлежащие к группе высокого риска по развитию рака молочной железы, — это носители генетической мутации BRCA1 или BRCA2 или носители других генетических мутаций, таких как аномалии, вызывающие синдромы Ли-Фраумени, Бан-найана-Райли-Рувалькабы или Каудена. К группе высокого риска также относятся женщины, которые получили облучение средостения (в основном из-за лимфомы) в возрасте до 30 лет, а также женщины, у которых прогнозируемый риск РМЖ в течение жизни превышает 20—25 %, на основе подтвержденных прогностических моделей. Женщины старше 30 лет с установленным высоким риском должны выполнять скрининговую маммографию ежегодно, а также дополнительно УЗИ и, если возможно, МРТ молочных желез (табл. 4.1). При наличии семейной истории РМЖ для здоровой женщины скрининг рекомендуется начинать на 7 лет раньше возраста родственника на момент постановки диагноза. Для женщин, у которых риск в течение жизни составляет менее 15 %, нет никаких доказательств того, что МРТ молочной железы будет полезным.
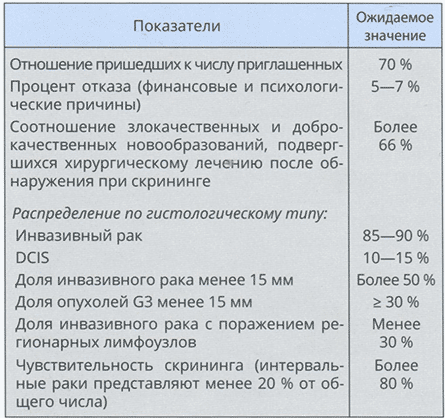
Таблица 4.1 Результаты скрининга рака молочной железы
Маммография
Если есть клиническое подозрение на рак молочной железы, в первую очередь делается рентгеновская маммография, как при скрининге. Выполняются снимки молочных желез в двух проекциях: боковой снимок — медиолатеральная проекция (MLO) и снимок сверху вниз — краниокаудального (СС) радиального направления. Доза облучения отдельной молочной железы от аналоговой рентгеновской маммографии составляет 1 мГр на изображение. Из-за характера изменений рентгенологической картины может потребоваться дополнительное увеличение, анализ микрокальцификаций и уточнение структурных искажений. В зависимости от структурного соотношения фиброзной, железистой и жировой ткани в молочной железе известно несколько различных морфологических типов молочной железы.
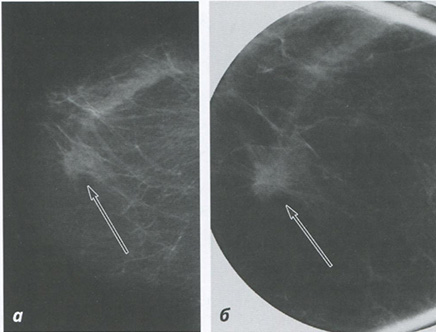
Рис. 4.2. Изображение скрининговой маммограммы (краниокаудальная проекция).
Ткань с выраженным железистым компонентом. Определяется зона высокой плотности на линии соска (BI-RADS 4С) (а). Зона интереса в увеличении: новообразование с заостренными краями (BI-RADS 5). Гистологическое исследование: инвазивный протоковый рак (б)
Плотная структура с высоким содержанием паренхимы является естественной в более молодом возрасте при сохраненном менструальном цикле, но она встречается и в возрасте старше 50 лет, что может быть объяснено индивидуальными генетическими особенностями, а может быть результатом заместительной гормональной терапии. Описание молочной железы должно быть универсальным. Система BI-RADS (Система отчетов и данных по визуализации молочных желез) широко применяется на международном уровне (табл. 4.2, 4.3). Она подразумевает интегральную оценку изменений и интерпретацию этих изменений с учетом вероятности наличия РМЖ. Чувствительность маммографии в среднем составляет 80 %, но она сильно зависит от типа структуры молочной железы; с увеличением плотности молочной железы чувствительность значительно снижается (для молочной железы с высоким процентом жировой ткани она составляет 95 %, для груди с плотной структурой — 50—60 %).
Структура молочной железы симметрична при нормальной маммографии и показывает гармоническую картину, но в отдельных случаях могут появляться структурные изменения, которые в основном проявляются как паренхиматозная асимметрия.
Таблица 4.2 Типы структуры молочной железы по классификации Tabar и система BI-RADS

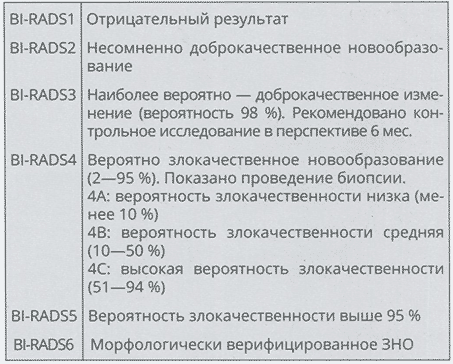
Таблица 4.3 Система визуализации и отчета о результате исследования груди (BI-RADS) Американского колледжа радиологов
Различные рентгенологические изменения могут соответствовать морфологическим изменениям. Злокачественные новообразования в основном имеют пикообразные и узловатые формы. Некоторые опухоли становятся очевидными из-за кальцификации, в то время как другие опухоли, такие как специфический тип лобулярной карциномы, выглядят как диффузное изменение со слегка повышенной плотностью или как структурное искажение. В зависимости от того, насколько изменения являются подозрительными в отношении наличия РМЖ, выставляется оценка от 1 до 5.
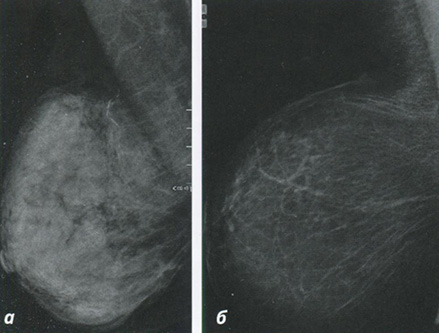
Рис. 4.3. Типы структуры паренхимы железы на маммограмме: а — плотная ткань железы (женщина 55 лет); б — ткань железы с жировой инволюцией (женщина 38 лет)
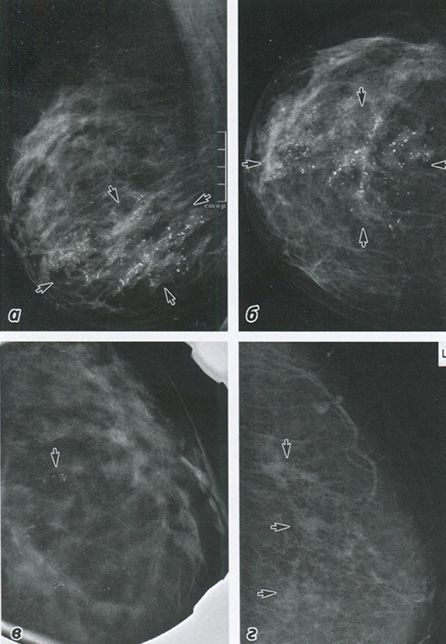
Рис. 4.4. Вид DCIS на маммограмме: а, б — множественные микрокальцинаты по ходу протоков на 6 часах воображаемого циферблата; в — локализованные кластеры микрокальцинатов (6 мм); г — сообщающиеся множественные нарушения структуры железы в виде узлов, но без микрокальцинатов (гистологическое исследование: распространенная DCIS)
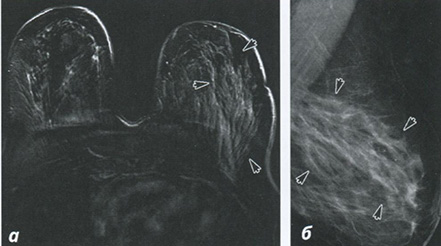
Рис. 4.5. Инвазивная дольковая карцинома: а — МРТ (субтракция) — небольшое усиление контрастирования в положении на 3 часах в левой молочной железе с распространением на грудную стенку; б — маммография (медиолатеральная косая проекция) — увеличение плотности в области на 3 часах слева
Некоторые опухоли не визуализируются на маммографических изображениях, что может частично быть результатом плотной структуры молочной железы, однако чувствительность также может зависеть от гистологического подтипа опухоли (рис. 4.3). Явных маммографических признаков часто нет в случаях лобулярной карциномы, а также при DCIS без отложения кальцинатов (рис. 4.4). Оценка степени поражения на основе рентген-изображения может быть ограничена в случае инвазивной опухоли с обширным внутрипротоковым компонентом (EIC), при DCIS или при мультифокальной лобулярной карциноме (рис. 4.5).
В странах Западной Европы и США аналоговая маммография была заменена цифровой маммографией. Согласно некоторым сравнительным исследованиям, обследования с использованием традиционных и цифровых маммографических методов имеют эквивалентные уровни общей диагностической точности (табл. 4.4). Тем не менее цифровая маммография оказалась более точной для рентгенологически плотных молочных желез и в случаях гетерогенной структуры, для женщин в возрасте до 50 лет и женщин в пременопаузе. С помощью цифрового метода маммографическое изображение может быть скорректировано без дополнительного рентгеновского облучения, таким образом, доза радиации уменьшается и некоторые манипуляции (такие как масштабирование и измерения) могут выполняться с использованием постобработки. Это позволяет применять компьютерную диагностику, которая помогает повышать точность. Кроме того, цифровое изображение является основой для дополнительного пересмотра, который может осуществляться посредствам дистанционного консультирования с помощью телемедицины.
Таблица 4.4 Положительная прогностическая ценность злокачественных новообразований на основе данных маммографической картины

Книга "Основы и принципы онкопластической хирургии при раке молочной железы"
Авторы: Матрай З., Гуляш Г., Ковач Т. И.

Пособие "Основы и принципы онкопластической хирургии при раке молочной железы" будет чрезвычайно полезно всем специалистам, вовлеченным в комплексное лечение пациентов с РМЖ. В нем подробно изложены современные подходы к диагностике, хирургическому, системному и лучевому лечению РМЖ, приведены последние эпидемиологические данные и представления об этиологии заболевания. Для практикующих специалистов-хирургов наибольшую ценность составит подробное изложение самых современных способов хирургического лечения с исчерпывающей доказательной базой исследований применения этих методов.
В течение длительного времени хирургическое лечение рака молочной железы не претерпевало значительных изменений, оставаясь при этом калечащей процедурой с крайне выраженным неблагоприятным влиянием на качество жизни пациентов. Пожалуй, самыми значимыми парадигмальными изменениями в практике хирургов-онкологов, специализирующихся на лечении РМЖ, стало внедрение органосохраняющего лечения и биопсии сигнальных лимфоузлов. Прогрессивное совершенствование лекарственного лечения и лучевой терапии привело к драматическому улучшению результатов лечения пациентов с РМЖ во всем мире.
За последние десятилетия частота локального рецидива неуклонно снижается в общей структуре неблагоприятных событий, что заставляет обращаться мыслями к будущему хирургии рака молочной железы, предвидя деэскалацию лечения и переход к еще менее травматичной хирургии. Между тем пластическая хирургия из сугубо реконструктивного инструмента, появившегося на заре XX в., стала мощнейшей областью медицины, характеризующейся стремительным развитием и внедрением передовых практик в рутинную деятельность. Сравнительно недавно методики пластической хирургии начали успешно применяться в онкологии, породив новую субспециальность — онкопластическая хирургия. Развитию этой дисциплины в России препятствует отсутствие формализованных программ обучения, малое количество центров обучения и обучающих специалистов, отсутствие русскоязычных пособий, и, возможно, главным препятствием являются довлеющие предубеждения и архаичные воззрения. Эта проблематика едина на всем пространстве Центральной и Восточной Европы.
Осознание существующих препон стало причиной создания Центрально-Восточноевропейского консорциума по хирургическому лечению рака молочной железы, к которому присоединился НМИЦ онкологии им. Н. Н. Петрова. В рамках этого международного сотрудничества подготовлена адаптация комплексного пособия по онкопластической хирургии «Основы и принципы онкопластической хирургии при раке молочной железы». Данное пособие будет чрезвычайно полезно всем специалистам, вовлеченным в комплексное лечение пациентов с РМЖ. В нем подробно изложены современные подходы к диагностике, хирургическому, системному и лучевому лечению РМЖ, последние эпидемиологические данные и представления об этиологии заболевания. Для практикующих специалистов-хирургов самую большую ценность составит подробное изложение самых современных способов хирургического лечения с исчерпывающей доказательной базой исследований применения этих методов.
Содержание книги "Основы и принципы онкопластической хирургии при раке молочной железы" - Матрай З., Гуляш Г., Ковач Т. И.
Глава 1. Рак молочной железы: этиология, эпидемиология, скрининг и лечение в Европе сегодня
1.1. Введение 1.2. Рак молочной железы: этиология, эпидемиология, организация скрининга в Европе
1.2.1. Факторы риска развития рака молочной железы
1.2.2. Рак молочной железы в Европе
1.2.3. Рак молочной железы в Европе — смертность от заболевания
1.2.4. Рак молочной железы в Европе — выживаемость
1.2.5. Программы скрининга рака молочной железы в Европе
1.2.6. Как организовано лечение рака молочной железы в Европе
1.2.7. Различия в доступности медицинской помощи при лечении рака молочной железы в Европе
1.3. Доказательная онкология в лечении рака молочной железы
1.4. Специализированный центр патологии молочной железы
1.5. Современные подходы в хирургии рака молочной железы — онкопластическая хирургия
Глава 2. Анатомия молочной железы и аксиллярной области
2.1. Форма, позиция и структурная анатомия молочной железы
2.2. Каркас молочной железы
2.3. Кровоснабжение молочной железы
2.4. Иннервация молочной железы
2.5. Анатомия мышц передней грудной стенки
2.6. Анатомия лимфатической системы молочной железы
2.7. Ключевые анатомические ориентиры подмышечной области с точки зрения хирургии
Глава 3. Молочная железа как эстетическая единица женского тела: теория и клиническая практика
3.1. Введение
3.2. Эстетические единицы и субъединицы молочной железы
3.2.1. Пропорции идеальной молочной железы. Арифметические измерения и геометрические правила, определяющие индивидуальные пропорции молочной железы, анатомические ориентиры и линии, необходимые для их определения
3.2.2. Положение соска на меридиане молочной железы. Практические методы определения положения соска
3.2.3. Связь между пятном молочной железы и антропометрическими пропорциями пациента.
Их влияние на выбор импланта
3.2.4. Расстояние между субмаммарной складкой и соском
3.2.5. Факторы, влияющие на симметричность молочных желез
3.3. Линии разреза на молочной железе
3.4. Реконструктивные операции на молочной железе и мышечные функции на грудной стенке
3.5. Влияние хирургических вмешательств по изменению формы и объема молочной железы на соотношение пятна, паренхимы и кожи молочной железы
3.6. Значение сосково-ареолярного комплекса в эстетической и реконструктивной хирургии молочной железы
Глава 4. Лучевая диагностика заболеваний молочной железы
4.1. Введение
4.2. Рекомендации по скринингу рака молочной железы
4.3. Скрининг в группах высокого риска
4.4. Способы визуализации ткани молочной железы
4.4.1. Маммография
4.4.2. Цифровой томосинтез и контраст-усиленная спектральная маммография
4.4.3. Ультразвуковое исследование
4.4.4. Магнитно-резонансная томография
4.4.5. Компьютерная томография в исследовании молочных желез
4.5. Изотопные исследования
4.6. Предоперационная оценка кровоснабжения тканей для планирования реконструктивно-пластических операций с использованием собственных тканей
4.7. Инвазивные процедуры
4.7.1. Биопсии под контролем визуализирующих методик
4.8. Дуктография
4.9. Роль врача-радиолога в принятии решений о тактике лечения
4.10. Оценка местно-распространенного процесса
4.11. Обследование на предмет наличия отдаленных метастазов
4.12. Предоперационное обследование
4.12.1. Маркировка непальпируемых образований
4.13. Маммографическое исследование операционного материала
4.14. Наблюдение за пациентами, подвергшимися хирургическому лечению
4.15. Радиологические исследования после реконструкции с использованием имплантов
4.16. Заключение
Глава 5. Злокачественные и доброкачественные опухоли молочной железы
5.1. Введение
5.2. Воспалительные заболевания молочной железы
5.3. Пролиферативные поражения молочной железы
5.4. Опухоли и опухолеподобные поражения
5.4.1. Доброкачественные поражения молочной железы
5.4.2. Предраковые заболевания молочной железы
5.4.3. Рак молочной железы
5.4.3.1. Гистологический подтип
5.4.3.2. Гистологическая степень злокачественности
5.4.3.3. Стадирование опухоли
5.4.3.4. Хирургические края резекции
5.4.3.5. Особые клинические проявления
5.5. Другие злокачественные опухоли молочной железы
Глава 6. Мультидисциплинарный подход к лечению рака молочной железы
6.1. Предоперационный мультидисциплинарный подход
6.2. Дополнительные сведения о мультидисциплинарном подходе и структуре функционирования мультидисциплинарных команд
Глава 7. Консультирование пациентов, форма информированного согласия, подготовка к операции
7.1. Введение
7.2. Правовые аспекты консультирования пациентов
7.2.1. Законодательство на практике, рекомендации юриста, специализирующегося на здравоохранении
7.3. Анестезиология в хирургии рака молочной железы
7.4. Хирургическая подготовка, положение больного
Глава 8. Традиционная хирургия рака молочной железы
8.1. Хирургические техники выполнения простой мастэктомии и органосохраняющей операции молочной железы без реконструктивно-пластического компонента
8.1.1. Хирургическая техника простых мастэктомий и классическая органосохраняющая хирургия (лампэктомия, широкое иссечение, квадрантэктомия)
8.1.2. Значимые нюансы при проведении органосохраняющего лечения
8.1.3. Хирургические техники при лечении непальпируемых новообразований молочной железы
8.1.3.1. Техника иссечения опухоли молочной железы с проводной локализацией (WGL)
8.1.3.2. Радиоизотопная методика локализации непальпируемых опухолей (ROLL)
8.1.3.3. Сравнение клинических результатов применения техник WGL и ROLL
8.1.4. Края резекции опухоли
8.1.4.1. Края резекции опухоли после неоадъювантной химиотерапии
8.1.5. Осложнения органосохраняющих операций на молочной железе
8.1.6. Особенности хирургических вмешательств при неинвазивных формах рака молочной железы (карциномы in situ)
8.1.7. Особенности хирургических вмешательств при редких формах рака молочной железы
8.2. Удаление подмышечных лимфатических узлов
8.2.1. Диагностика состояния подмышечных лимфатических узлов
8.2.2. Показания к удалению подмышечных лимфатических узлов
8.2.3. Хирургическая техника аксиллярной лимфодиссекции
8.2.4. Осложнения аксиллярной лимфодиссекции
8.2.5. Локальный рецидив в аксиллярной области
Глава 9. Биопсия сигнальных лимфатических узлов при раке молочной железы
9.1. Введение
9.2. Биопсия сигнальных лимфатических узлов
9.3. Хирургическая техника биопсии сигнальных лимфатических узлов
9.4. Показания и противопоказания к биопсии сигнального лимфатического узла
9.5. Негативный сигнальный лимфатический узел
9.6. Пораженный сигнальный лимфатический узел
9.6.1. Изолированные опухолевые клетки
9.6.2. Микрометастазы
9.6.3. Макрометастазы
9.6.4. Внеаксиллярный лимфодренаж
9.7. Особые клинические ситуации при биопсии сигнального лимфатического узла
9.7.1. Протоковая карцинома in situ.
9.7.2. Биопсия сигнального лимфатического узла в случаях мультицентричного рака молочной железы
9.7.3. Биопсия сигнального лимфатического узла после первичной системной химиотерапии
9.7.3.1. Неоадъювантная химиотерапия и биопсия сторожевого лимфатического узла у пациентов с клинически отрицательными подмышечными лимфатическими узлами при первичной диагностике
9.7.3.2. Неоадъювантная химиотерапия и биопсия сигнального лимфатического узла у пациентов с доказанными метастазами в аксиллярные лимфатические узлы при первичном диагнозе
9.7.4. Биопсия сигнального лимфатического узла при раке молочной железы у мужчин
9.7.5. Биопсия сигнального лимфатического узла при местно-распространенном раке молочной железы и воспалительном неоперабельном раке молочной железы
9.7.6. Биопсия сигнальных лимфатических узлов и рак молочной железы при беременности
9.7.7. Биопсия сигнального лимфатического узла после предыдущей операции на подмышечной
области при рецидиве рака молочной железы
9.7.8. Биопсия сигнального лимфатического узла и одномоментная реконструкция молочной железы
9.8. Заключение и рекомендации
Глава 10. Онкопластические органосохраняющие операции
10.1. Общие принципы онкопластических органосохраняющих операций
10.1.1. Эра органосохраняющей хирургии
10.1.2. Эра онкопластической хирургии молочной железы
10.1.3. Показания к онкопластической органосохраняющей хирургии молочной железы
10.1.4. Стандартизация онкопластических органосохраняющих вмешательств
10.1.4.1. Стандартизированная номенклатура онкопластической хирургии
10.1.5. Алгоритм выбора техник онкопластической хирургии молочной железы
10.1.6. Онкологические результаты онкопластических органосохраняющих операций
10.1.6.1. Края резекции при онкопластической хирургии
10.1.6.2. Локальный контроль при онкопластической органосохраняющей хирургии
10.1.6.3. Осложнения, связанные с онкопластической хирургией и возможной задержкой адъювантного лечения
10.1.6.4. Наблюдение за пациентами после лечения рака молочной железы с помощью онкопластической органосохраняющей хирургии
10.1.7. Отзывы пациентов о результатах онкопластических вмешательств
10.1.8. Практические аспекты онкопластической хирургии молочной железы
10.2. Процедуры для моделирования и редукции молочной железы в пластической хирургии
10.2.1. Сочетание онкологии и пластической хирургии в лечении рака молочной железы
10.2.2. Основные вехи в развитии хирургического лечения рака молочной железы
10.2.3. Факторы, влияющие на форму молочной железы
10.2.4. Процедуры по коррекции молочных желез в пластической хирургии
10.2.4.1. Принципы и виды корректирующих вмешательств по изменению формы молочных желез
10.2.4.2. Показания, предоперационная оценка состояния пациента
10.2.4.3. Предоперационное планирование
10.2.4.4. Формирование холма молочной железы
10.2.4.5. Реорганизация паренхимы и фиксация
10.2.4.6. Длина вертикального разреза и дополнительные разрезы
10.2.4.7. Хирургическая техника
10.2.4.7.1. Периареолярная мастопексия
10.2.4.7.2. Вертикальная и циркумвертикальная мастопексия
10.2.4.8. Алгоритм создания формы молочной железы
10.2.4.8.1. Легкая степень птоза
10.2.4.8.2. Умеренная степень птоза
10.2.4.8.3. Выраженный птоз
10.2.4.8.4. Псевдоптоз
10.2.5. Редукционная маммопластика
10.2.5.1. Показания к редукционной маммопластике
10.2.5.1.1. Редукция молочной железы с эстетической целью
10.2.5.1.2. Редукция молочной железы с реконструктивной целью
10.2.5.1.3. Показания к удалению злокачественной опухоли молочной железы в комбинации с редукционной маммопластикой (онкопластическая техника)
10.2.5.2. Требования и ожидания относительно редукционной маммопластики
10.2.5.3. Выбор техники редукционной маммопластики
10.2.5.4. Кожные разрезы
10.2.5.5. Дермогландулярные лоскуты, обеспечивающие кровоснабжение соска
10.2.5.5.1. Лоскут на верхней дермальной ножке
10.2.5.5.2. Лоскут на нижней дермальной ножке
10.2.5.5.3. Лоскут на медиальной или латеральной дермальной ножке
10.2.5.6. Ремоделирование и фиксация ткани после резекции
10.2.5.7. Кожный разрез и предоперационное планирование дермогландулярных лоскутов
в зависимости от объема резекции
10.2.5.8. Осложнения редукционной маммопластики
10.2.6. Диагностическая лампэктомия
10.2.7. Удаление центральной части молочной железы вместе с сосково-ареолярным комплексом
10.2.8. Удаление периферической части молочной железы вместе с сосково-ареолярным комплексом. Удаленная ткань молочной железы составляет от общего объема железы
10.2.8.1. Устранение дефекта ткани, превышающего объема железы
10.2.8.2. Кожный разрез и удаление опухоли при птозе молочной железы, предоперационное планирование операции
10.2.9. Резекция и лампэктомия при гипертрофии молочной железы и гигантомастии
10.3. Методы онкопластической хирургии молочной железы при центрально расположенных опухолях
10.3.1. Введение
10.3.2. Показания к онкопластической операции по сохранению молочной железы при центрально расположенных опухолях
10.3.3. Методы онкопластической хирургии при центрально локализованном раке молочной железы
10.3.3.1. Периареолярные онкопластические методы
10.3.3.2. Центральная квадрантэктомия
10.3.3.3. Методы маммопластики при центрально расположенных опухолях
10.3.3.3.1. Мастопексия в технике инвертированной Т с использованием нижней питающей ножки
10.3.3.3.2. Онкопластическая техника по Гризотти
10.3.3.3.3. Онкопластика по Regnault для лечения центрально расположенных опухолей
10.3.3.3.4. Ретрогландулярная онкопластика при центрально расположенных опухолях
10.3.4. Клинический результат онкопластических методов лечения центрально расположенных опухолей
10.4. Методы онкопластических операций из периареолярного доступа
10.4.1. Введение
10.4.2. Периареолярная методика онкопластической резекции
10.4.2.1. Модификация техники round block в онкопластической хирургии
10.4.3. Осложнения
10.5. Горизонтальные онкопластические техники
10.5.1. Введение
10.5.2. Хирургическое планирование
10.5.3. Горизонтальные онкопластические методы
Литература
10.6. Техника верхней ножки, инвертированная Т-маммопластика
10.6.1. Введение
10.6.2. Маркировка и хирургическое планирование
10.6.3. Хирургическая техника
10.6.4. Осложнения
10.6.5. Заключение
10.7. Техника вертикальной маммопластики
10.7.1. Введение
10.7.2. Маркировка и хирургическая техника
10.8. Маммопластика по методу инвертированной Т на нижней питающей ножке
10.8.1. Введение
10.8.2. Хирургическая техника
10.8.3. Осложнения
10.8.4. Другие особые соображения о технике
10.9. Онкопластические техники при латеральном расположении опухоли
10.9.1. Введение
10.9.2. Хирургическая техника латеральной онкопластической операции
10.9.2.1. Модифицированная хирургическая техника латеральной онкопластической операции. Модификация Regnault В
10.10. Онкопластическая техника «омега»
10.10.1. Введение
10.10.2. Хирургическое планирование
10.10.3. Техника онкопластической операции по типу «омеги»
10.10.4. Преимущества и недостатки «омега»-техники
10.11. Онкопластическая хирургия при медиальном расположении опухолей молочной железы
10.11.1. Введение
10.11.2. Онкопластические техники, применяемые при опухолях верхнего внутреннего квадранта молочной железы
10.11.3. Онкопластические техники, применяемые при опухолях нижнего внутреннего квадранта молочной железы
10.12. Онкопластическая хирургия в лечении опухолей нижнего полюса молочной железы
10.12.1. Введение
10.12.2. Хирургические техники
10.13. Ретрогландулярная онкопластическая органосохраняющая хирургия
10.13.1. Введение
10.13.2. Показания, противопоказания к применению ретрогландулярной онкопластической органосохраняющей техники
10.13.3. Ретрогландулярная онкопластическая органосохраняющая техника
10.13.4. Клинико-патологические и эстетические результаты ретрогландулярной онкопластической органосохраняющей операции
10.14. Характерные осложнения, деформации и возможные варианты хирургической коррекции после традиционных и онкопластических операций
10.14.1. Введение
10.14.2. Послеоперационное кровоизлияние
10.14.3. Послеоперационное воспаление молочной железы
10.14.4. Жировой некроз
10.14.5. Формирование патологичесих рубцов
10.14.6. Нежелательное увеличение диаметра ареолы
10.14.7. Специфические осложнения после онкопластической операции с применением техники инвертированной Т с нижней питающей ножкой
10.14.7.1. Преходящая лимфедема дермогландулярных лоскутов
10.14.7.2. Частичный и полный некроз дермогландулярных лоскутов
10.14.7.3. ICAP-лоскуты. Хирургическая техника
10.14.7.4. Частичный и полный некроз ареолы сосков
10.14.7.5. Псевдоптоз
10.14.7.6. Новый сосково-ареолярный комплекс, расположенный слишком высоко, или феномен «старгейзер» — «наблюдение за звездами»
10.14.8. Лечение осложнений адъювантной лучевой терапии после органосохраняющих операций
Глава 11. Постмастэктомическая реконструкция молочной железы
11.1. Общие вопросы постмастэктомической реконструкции молочной железы
11.1.1. Введение
11.1.2. Постмастэктомическая реконструкция молочной железы: потребности и знания
11.1.3. Оценка знаний, желаний и психосоциального фона пациента в отношении постмастэктомической реконструкции молочной железы в Центральной и Восточной Европе
11.2. Импланты в реконструктивной хирургии молочной железы
11.2.1. Введение
11.2.2. Типы имплантов молочных желез
11.2.3. Силикон
11.2.4. Силиконовые импланты и канцерогенез
11.2.4.1. Имплант-ассоциированная анапластическая крупноклеточная лимфома
11.2.5. Показания к применению силиконовых имплантов
11.2.6. Противопоказания к применению силиконовых имплантов
11.2.7. Место установки импланта
11.2.8. Выбор правильного импланта
11.2.9. Осложнения
11.2.9.1. Капсулярная контрактура
11.2.9.1.1. Причины развития и формирования патологических капсул
11.2.9.1.2. Классификация Бейкера (клиническая тяжесть капсулярной контрактуры)
11.2.9.1.3. Капсулотомия, 3D архитектурная капсулопластика
11.2.10. Экспандеры
11.2.10.1. Показания к применению экспандера
11.2.10.2. Противопоказания к применению экспандера
11.2.10.3. Осложнения
11.2.11. Ацеллюлярный дермальный матрикс
11.2.12. Облегченные импланты молочных желез. Новое решение для реконструкции молочной железы
11.3. Методы расчета объема молочной железы
11.3.1. Введение
11.3.2. Вариации формы молочной железы и симметрии
11.3.3. Методы измерения объема
11.3.4. Трехмерное моделирование на основе поверхностного сканирования
11.4. Одномоментная реконструкция молочной железы
11.4.1. Введение
11.4.2. Показания для одномоментной реконструкции молочной железы
11.4.3. Онкологические аспекты одномоментной реконструкции молочной железы
11.4.3.1. Одномоментная реконструкция молочной железы и адъювантная терапия
11.4.3.2. Одномоментная реконструкция молочной железы и время адъювантной химиотерапии
11.4.3.3. Возможные корреляции между неоадъювантной или адъювантной химиотерапией и одномоментной реконструкцией молочной железы
11.4.3.4. Влияние адъювантной лучевой терапии на одномоментную реконструкцию молочной железы
11.4.4. Одномоментная реконструкция молочной железы и качество жизни пациентов
11.4.5. Механизм принятия решения об одномоментной реконструкции
11.4.6. Симметризующие операции на контралатеральной молочной железе, реконструкция соска
11.4.7. Ранние и поздние осложнения одномоментной реконструкции молочной железы
11.4.8. Опыт одномоментных реконструкций в Национальном онкологическом институте, Венгрия
11.5. Отсроченная реконструкция
11.5.1. Введение
11.5.2. Показания к выполнению и особенности отсроченной реконструкции молочной железы
11.5.2.1. Онкологические особенности двухэтапных и отсроченных реконструкций молочной железы
11.5.2.2. Факторы, связанные с особенностями пациента
11.5.3. Практические аспекты отсроченной реконструкции молочной железы
11.5.3.1. Техническая оценка
11.5.3.2. Методики отсроченной реконструкции при дефектах после органосохраняющих операций
11.5.3.3. Методики отсроченной реконструкции после радикальной мастэктомии
11.5.3.4. Аутологичные лоскуты в отсроченной реконструкции
11.5.4. Результаты отсроченной реконструкции молочной железы
11.5.4.1. Информация, предоставленная женщинам до операции на молочной железе
11.5.4.2. Типы реконструкций молочной железы
11.5.4.3. Типы контралатеральных и вторичных реконструктивных методик
11.5.4.4. Частота осложнений при отсроченной реконструкции
11.5.4.4.1. Профиль осложнений при различных типах операций
11.5.4.4.2. Осложнения, связанные с имплантом
11.5.4.4.3. Осложнения, связанные с лоскутом
11.5.4.4.4. Осложнения через 3 мес. после операции
11.5.4.5. Противоболевая терапия в первые 24 ч после операции
11.5.5. Доступность психологической поддержки в послеоперационном периоде
11.5.6. Долгосрочные клинические результаты и удовлетворенность пациентов после отсроченной реконструкции
11.5.6.1. Удовлетворенность имплантами
11.5.6.2. Удовлетворенность результатами в донорской области лоскута
11.6. Кожесохраняющая и ареола-/САК-сохраняющая мастэктомия (Золтан Матрай, Георги Тизедес)
11.6.1. Введение
11.6.2. Показания для КСМ, АСМ
11.6.3. Хирургическая техника КСМ
11.6.4. Техника АСМ
11.6.5. Реконструкция молочной железы после КСМ и АСМ
11.6.6. Онкологические аспекты КСМ, АСМ
11.6.7. КСМ и резидуальная ткань молочной железы
11.6.8. Результаты КСМ при местно-распространенном инвазивном раке молочной железы
11.6.9. Немедленная реконструкция и начало адъювантной терапии
11.6.10. Немедленная реконструкция и диагностика местного рецидива
11.6.11. КСМ и лучевая терапия
11.6.12. Осложнения
11.7. Подкожная мастэктомия с сохранением сосково-ареолярного комплекса
11.7.1. Введение
11.7.2. Показания к подкожной мастэктомии и точный отбор пациентов
11.7.3. Микроструктура соска
11.7.4. Хирургическая техника подкожной мастэктомии с сохранением САК
11.7.4.1. Обработка соска
11.7.5. Жизнеспособность соска
11.7.6. Реконструкция после подкожной мастэктомии
11.7.7. Онкологическая безопасность при профилактических операциях
11.7.8. Онкологическая безопасность подкожных операций при раке молочной железы
11.7.9. Эстетические результаты и удовлетворенность пациентов
11.7.10. Резюме
11.8. Реконструкция молочной железы при помощи импланта с полным мышечным укрытием
11.8.1. Введение
11.8.2. Хирургическое планирование
11.8.3. Хирургическая техника
11.8.3.1. Хирургическая техника кожередуцирующей мастэктомии
11.8.4. Осложнения
11.8.5. Заполнение экспандера
11.8.6. Замена экспандера на имплант и симметризация
11.9. Использование ацеллюлярных дермальных матриксов для одномоментной реконструкции имплантом (Тибор Ковач)
11.9.1. Субпекторальная реконструкция молочной железы имплантом с укрытием ADM
11.9.1.1. Введение
11.9.1.2. Показания: отбор пациентов
11.9.1.3. Цели реконструкции с использованием АDМ и импланта
11.9.1.4. Хирургические анатомические аспекты: маркировка
11.9.1.5. Выбор импланта и АDМ
11.9.1.6. Хирургическая техника
11.9.1.7. Послеоперационный уход
11.9.1.8. Лечение и профилактика развития послеоперационных осложнений
11.9.2. Препекторальная реконструкция с применением АDМ
11.9.2.1. История методики
11.9.2.2. Приспособления для замещения недостатка мягких тканей
11.9.2.3. Показания для препекторальной реконструкции имплантом и АDМ
11.9.2.4. Процедура препекторальной реконструкции с использованием АDМ
11.9.2.5. Возможные осложнения препекторальной реконструкции с использованием АDМ
11.9.2.6. Противопоказания к проведению препекторальной реконструкции с применением импланта и АDМ
11.10. Реконструкция молочной железы с использованием кожно-мышечного лоскута широчайшей мышцы спины (ТДЛ)
11.10.1. Введение
11.10.2. Преимущества и недостатки
11.10.3. Хирургическая анатомия кожно-мышечного лоскута широчайшей мышцы спины — дизайн лоскута
11.10.4. Хирургическая техника получения и перемещения торакодорсального лоскута
11.10.5. Модификации стандартной методики ТДЛ
11.10.5.1. Ускоренное выделение кожно-мышечного лоскута широчайшей мышцы спины («fast-track»)
11.10.5.1.1. Ускоренная хирургическая техника для кожно-мышечного лоскута широчайшей мышцы спины
11.10.6. Послеоперационный уход
11.10.7. Осложнения
11.11. Реконструкция молочной железы с помощью кожно-мышечного лоскута широчайшей мышцы спины и экспандера или импланта
11.11.1. Частота применения различных методов реконструкции молочной железы
11.11.2. Показания к реконструкции молочной железы с использованием ТДЛ и эндопротезов
11.11.3. Согласованность при планировании онкологических и пластических хирургических процедур для одномоментной и отсроченной реконструкции молочной железы с использованием ТДЛ и эндопротеза
11.11.4. Предоперационное планирование
11.11.5. Удаление опухоли молочной железы и облученных тканей
11.11.6. Замещение кожи и мягких тканей
11.11.7. Выбор эндопротеза
11.11.8. Выделение кожно-мышечного лоскута широчайшей мышцы спины и его перемещение на грудную стенку
11.11.9. Установка эндопротеза между слоями ткани на грудной стенке 11.11.10. Перенос кожно-мышечного лоскута широчайшей мышцы спины и аугментация с использованием экспандера/импланта двухэтапно. Замена экспандера на имплант
11.11.11. Осложнения, возникающие при реконструкции с помощью ТДЛ и эндопротеза
11.12. Лоскут на прямой мышце живота (TRAM-лоскут)
11.12.1. Введение
11.12.2. Мышцы брюшной стенки и фасция прямой мышцы живота
11.12.3. Кровоснабжение
11.12.3.1. Эпигастральные сосуды
11.12.3.2. Сосуды кожи
11.12.3.3. Венозный отток
11.12.4. Иннервация
11.12.5. Функция прямой мышцы живота
11.12.6. Физикальное обследование пациента
11.12.6.1. Сбор анамнеза
11.12.6.2. Морфологическое обследование
11.12.6.3. Предшествующие рубцы
11.12.7. Дизайн TRAM-лоскута
11.12.8. Положение пациента на операционном столе
11.12.9. Техника выделения TRAM-лоскута
11.12.9.1. Подготовка реципиентной зоны
11.12.9.2. Выделение TRAM-лоскута
11.12.9.3. Транспозиция TRAM-лоскута на грудную стенку
11.12.9.4. Реконструкция брюшной стенки
11.12.9.5. Моделирование лоскута и наложение швов
11.12.10. Особенности лоскута на двойной ножке
11.12.11. Подготовка лоскута
11.12.12. Перевязочные материалы
11.12.13. Послеоперационное положение
11.12.14. Ранний послеоперационный период
11.12.15. Перспективы TRAM
11.12.15.1. Объем лоскута
11.12.15.2. Форма лоскута
11.12.15.3. Повторная операция
11.12.16. Преимущества техники реконструкции TRAM-лоскутом
11.12.17. Недостатки техники реконструкции TRAM-лоскутом
11.12.18. Ранние осложнения реконструкции TRAM-лоскутом
11.12.19. Проблемы брюшной стенки
11.13. Местные лоскуты. Частичное или полное удаление молочной железы с реконструкцией лоскутом
11.13.1. Перемещенный абдоминальный лоскут
11.13.2. Торакоэпигастральный лоскут
11.13.3. Лоскут с перфорантами межреберной артерии (ICAP)
11.13.3.1. Латеральный или медиальный лоскут с перфорантами межреберной артерии в сочетании с перемещенным абдоминальным лоскутом
11.13.4. Лоскут на основе перфорантов торакодорсальной артерии (ТDАР)
11.14. Реконструкция молочной железы свободными лоскутами (Габор Павловикс)
11.14.1. Введение
11.14.2. Микрохирургическая техника
11.14.3. Выбор реципиентных сосудов в реконструкции молочной железы
11.14.4. Назначение лекарственных препаратов в периоперационном периоде
11.14.5. Контроль за кровоснабжением лоскута
11.14.6. Ведение пациентов с осложнениями
11.14.7. Влияние предыдущих оперативных вмешательств на успех операции
11.14.8. Свободные лоскуты из передней брюшной стенки
11.14.8.1. Свободный кожно-мышечный лоскут на основе прямой мышцы живота (TRAM)
11.14.8.2. Свободный мышцесберегающий поперечный кожно-мышечный лоскут на основе прямой мышцы живота
11.14.8.3. Лоскут на основе перфорантов нижней глубокой эпигастральной артерии (DIEP)
11.14.8.4. Лоскут на основе поверхностной нижней эпигастральной артерии (SIEA)
11.14.8.5. Лоскуты с двойным кровоснабжением
11.14.8.5.1. Лоскут передней брюшной стенки с «подкачкой»
11.14.8.5.2. Лоскуты с двумя сосудистыми ножками
11.14.9. Двусторонняя реконструкция
11.14.10. Реконструкция лоскутами с использованием тканей ягодичной области
11.14.11. Заключение
11.15. Специфические осложнения при реконструкции молочной железы после мастэктомии: косметические недостатки и варианты их хирургической коррекции
11.15.1. Введение
11.15.2. Нестабильность или перфорация кожного лоскута после кожесохраняющей мастэктомии и реконструкции имплантом
11.15.3. Феномен «риплинга» после подкожной и кожесохраняющей мастэктомии и реконструкиции с использованием имплантов
11.15.4. Неправильное положение САК после подкожной мастэктомии и реконструкции молочной железы имплантом
11.15.5. Избыточное растяжение мягких тканей срединной линии, медиальное положение имплантов и симмастия после кожесохраняющей и подкожной мастэктомии и одномоментной двухэтапной реконструкции молочной железы
11.15.6. Самопроизвольная эвакуация содержимого экспандера после одномоментной реконструкции
11.15.7. Капсулярная контрактура после подкожной или кожесохраняющей мастэктомии и реконструкции с использованием имплантов
11.15.8. Специфические осложнения после аутологичной реконструкции молочной железы после мастэктомии
Глава 12. Операции по формированию симметрии формы и объема молочных желез, реконструкция соска и ареолы
12.1. Необходимость в симметризации: изменение подхода к удалению опухоли и реконструкции молочной железы
12.2. Связь между удалением злокачественной опухоли молочной железы и достижением симметрии
12.3. Наиболее распространенные причины асимметрии молочных желез
12.3.1. Органосохраняющие операции без реконструкции
12.3.2. Послеоперационная лучевая терапия
12.3.3. Реконструкция молочной железы с помощью эндопротезов
12.4. Формирование соска и ареолы
12.4.1. Введение
12.4.1.1. Положение и разметка нового соска
12.4.2. Техники реконструкции ареолы
12.4.3. Техники реконструкции соска
12.4.3.1. Разделение соска или трансплантат с половиной соска
12.4.3.2. Хирургическая техника лоскута CV
12.5. Проблемы с реконструированным соском
Глава 13. Рак молочной железы после предшествующей эстетической операции
13.1. Введение
13.2. Диагностика рака в ранее аугментированной молочной железе
13.3. Стадия рака, диагностированного в аугментированной молочной железе
13.4. Биопсия сигнального лимфоузла у женщин после аугментации молочных желез
13.5. Особые аспекты хирургической онкологии при операции на аугментированной железе
13.6. Органосохраняющая операция с сохранением импланта
13.7. Органосохраняющая операция с удалением импланта с мастопексией или без нее
13.8. Восстановление дефицита тканей после органосохраняющей операции
13.9. Мастэктомия с заменой импланта или экспандера и/или реконструкция с использованием аутологичной ткани
13.10. Симметризация контралатеральной молочной железы
13.11. Особые аспекты хирургии рака молочной железы после предшествующей мастопексии
13.12. Особенности хирургического лечения гистологически неопределенных и доброкачественных заболеваний после предыдущей эстетической операции на молочной железе
Глава 14. Трансплантация аутологичной жировой ткани при реконструктивных вмешательствах после операций по поводу рака молочной железы
14.1. Введение
14.2. Показания к трансплантации жировой ткани
14.3. Аутологичный жировой графт
14.4. Донорские зоны
14.5. Общая техника аутологичной жировой трансплантации
14.5.1. Локальная инфильтрация тканей и использование тумесцентного раствора
14.5.2. Сбор аутологичного жира
14.5.3. Канюли
14.5.4. Переработка и приготовление жира
14.5.5. Хранение и заморозка жира
14.5.6. Трансплантация жира
14.6. Различные факторы, влияющие на выживаемость жирового графта
14.7. Стволовые клетки жировой ткани
14.8. Адипоциты и рак молочной железы
14.9. Внедрение трансплантации аутологичной жировой ткани в хирургию молочной железы
14.9.1. Информация о пациенте и информированное согласие
14.9.2. Липомоделирование с онкологической точки зрения
14.9.3. Клинико-косметические результаты липомоделирования
14.10. Осложнения после трансплантации аутологичной жировой ткани
14.11. Радиологические последствия пересадки аутологичного жира в молочной железе
14.12. Резюме
Глава 15. Синдром наследственного рака молочной железы и яичников: от настороженности к снижению риска
15.1. Введение
15.2. Наследственный и семейный рак молочной железы
15.3. Синдром рака молочной железы и рака яичников, ассоциированный с BRCA1/2 (HBOC)
15.4. Обнаружение наследственных мутаций генов BRCA
15.5. Оценка риска генетического рака (GCRA): генетическое консультирование и генетическое тестирование в связи с наследственным риском рака молочной железы
15.6. Процесс генетического консультирования
15.7. Генетическая оценка риска развития рака
15.8. Клиническое генетическое тестирование
15.9. Ведение пациентов с повышенным риском развития рака молочной железы
15.9.1. Информированность и изменение образа жизни
15.9.2. Скрининг
15.9.2.1. Рекомендации по скринингу после профилактических операций
15.9.3. Профилактические операции
15.9.3.1. Профилактические операции для рака молочной железы
15.9.3.2. Операции по снижению риска развития рака яичников
15.9.4. Медикаментозная профилактика
15.10. Особенности лечения рака молочной железы у носителей мутации BRCA1/2
15.11. Возможности системного лечения при BRCA-положительном раке молочной железы
15.12. Исследования оценки экономической целесообразности генетического консультирования и генетических тестов
15.13. Психосоциальные последствия
15.14. Резюме
Глава 16. Малоинвазивная хирургия молочной железы
16.1. Введение
16.2. Терапевтическое применение вакуум-аспирационной биопсии
16.3. Эндоскопически ассистированная операция с выделением мышечного лоскута широчайшей мышцы спины
16.4. Эндоскопически ассистированные внутрикапсулярные вмешательства
16.5. Радиочастотная абляция рака молочной железы
16.6. Дуктоскопия
16.7. Роботизированная подкожная мастэктомия и одномоментная реконструкция молочной железы с помощью импланта
Глава 17. Хирургическое лечение рака молочной железы у мужчин
17.1. Введение
17.2. Факторы риска развития рака молочной железы у мужчин
17.3. Диагностика рака молочной железы у мужчин
17.4. Локорегионарное лечение рака молочной железы у мужчин
17.5. Системное лечение рака молочной железы у мужчин
17.6. Наблюдение
17.7. Заключение
17.8. Гинекомастия
17.8.1. Введение
17.8.2. Классификация гинекомастии
17.8.3. Лечение гинекомастии
17.8.3.1. Хирургическое лечение гинекомастии
17.8.3.2. Консервативное лечение гинекомастии
Глава 18. Паллиативное хирургическое лечение рака молочной железы
18.1. Введение
18.2. Хирургическое лечение первичной опухоли при метастатическом раке молочной железы
18.3. Хирургия метастатических очагов
18.3.1. Паллиативная хирургия висцеральных метастазов
18.3.2. Паллиативная хирургия костных метастазов и метастазов в головной мозг
18.4. Лучшее поддерживающее лечение
18.5. Хирургическое лечение местных рецидивов
18.6. Резюме
Литература
Глава 19. Особенности хирургического лечения рака молочной железы у пожилых пациентов
19.1. Введение
19.2. Биологические особенности рака молочной железы у пожилых пациентов
19.3. Особенности диагностики у пожилых пациентов
19.4. Хирургическое лечения рака молочной железы у пожилых пациентов
19.4.1. Особенности органосохраняющих операций и мастэктомии у пожилых пациентов
19.4.2. Радикальное хирургическое лечение первичной опухоли в сравнении с эндокринной терапией
19.4.3. Особенности аксиллярной лимфаденэктомии у пожилых пациентов
19.4.4. Реконструктивные операции у пожилых пациентов
19.5. Заключение
Глава 20. Междисциплинарное лечение рака молочной железы
20.1. Современная адъювантная лучевая терапия рака молочной железы
20.1.1. Введение
20.1.2. Принципы лучевой терапии
20.1.3. Технические аспекты лечения рака молочной железы и их практическое применение
20.1.4. Показания к лучевой терапии
20.1.5. Нежелательные эффекты лучевой терапии
20.2. Системное лечение рака молочной железы
20.2.1. Общие рекомендации по терапии
20.2.2. Системная терапия рака молочной железы
20.2.2.1. Введение
20.2.2.2. Эндокринная терапия при раке молочной железы
20.2.2.2.1. Гормональная депривационная терапия: аналоги агонистов гонадотропин-рилизинг-гормона и ингибиторы ароматазы
20.2.2.2.2. Лечение блокированием гормон-рецептора: селективный модулятор рецептора эстрогена и «чистые антиэстрогены»
20.2.2.2.3. Показания к эндокринной терапии
20.2.2.2.3.1. Адъювантная эндокринная терапия
20.2.2.2.3.2. Неоадъювантная эндокринная терапия
20.2.2.2.3.3. Паллиативная эндокринная терапия
20.2.2.3. Эндокринная терапия и молекулярно-ориентированные методы лечения
20.2.2.4. Химиотерапия и таргетная терапия рака молочной железы
20.2.2.4.1. Адъювантная химиотерапия и таргетная терапия ингибиторами HER при раке молочной железы
20.2.2.4.2. Первичная системная (неоадъювантная) химиотерапия и биологическая терапия рака молочной железы
20.2.2.4.3. Химиотерапия при местном рецидиве рака молочной железы
20.2.2.4.4. Химиотерапия и таргетная биологическая терапия при IV стадии рака молочной железы (отдаленный метастаз)
20.2.2.4.4.1. HER2-положительный рак молочной железы
20.2.2.4.4.1. HER2-рецептор-отрицательный рак молочной железы
20.2.2.5. Лучшая поддерживающая и паллиативная помощь
20.3. Последующее наблюдение за больными раком молочной железы (Золтан Матрай)
20.3.1. Введение
20.3.2. Цели клинического наблюдения за пациентами, перенесшими рак молочной железы
20.3.3. Протокол наблюдения за пациентами с ранней стадией рака молочной железы
20.3.4. Протокол наблюдения за пациентами с местно-распространенным раком молочной железы и мониторинг лечения больных раком молочной железы IV стадии
20.4. Психоонкологические аспекты рака молочной железы
20.4.1. Введение
20.4.2. Результаты исследований.
20.4.2.1. Пациенты, родственники, специалисты
20.4.2.2. Пациенты женского пола с диагнозом рак молочной железы
20.4.2.3. Предоперационное состояние стресса
20.4.2.4. Носители мутаций гена BRCA
20.4.3. Психические трудности и симптомы, связанные с хирургическим лечением рака молочной железы
20.4.3.1. Образ тела, отношения и сексуальность
20.4.3.2. Болевой синдром
20.4.3.3. Психическое расстройство
20.4.3.3.1. Признаки психической дезадаптации
20.4.3.3.2. Кризис.
20.4.4. Лечение
20.4.4.1. Показания к онкопсихотерапевтическим вмешательствам
20.4.4.2. Психологические вмешательства и методы
20.4.4.3. Психологический скрининг
20.4.4.4. Важность психосексуального образования, предшествующего онкологической помощи
20.4.4.5. Предоперационное психосоциальное обучение
20.4.4.6. Расслабление
20.4.4.7. Кризисное вмешательство
20.4.4.8. Психоонкологическая поддержка
20.4.5. Перспективы: настоящее и будущее психоонкологии
20.5. Роль медсестер по уходу за пациентами с раком молочной железы в междисциплинарном подходе к лечению рака молочной железы
20.5.1. Введение
20.5.2. Роль медсестры по уходу за пациентами с раком молочной железы в специализированной помощи
20.5.3. Подготовка медсестер по уходу за пациентами с раком молочной железы
20.5.4. Эффективность медсестер по уходу за пациентами с раком молочной железы на основе литературных данных
20.6. Современная физиотерапия и реабилитация после операций на молочной железе (Сюза Капитани)
20.6.1. Введение
20.6.2. Стадии лимфедемы
20.6.3. Лечебная физкультура в раннем послеоперационном периоде
20.6.4. Программа ранних упражнений после лампэктомии, квадрантэктомии или мастэктомии
20.6.5. Программа ранних упражнений после имплантации экспандера
20.6.6. Программа упражнений после реконструкций с использованием лоскутов TRAM, DIEP и ТДЛ
20.7. Медицинские приборы в реабилитации после операции на молочной железе (Лазло Тох)
20.7.1. Введение
20.7.2. Восстановление образа тела с использованием наружных протезов
20.7.2.1. Устройства, используемые в раннем послеоперационном периоде
20.7.2.2. Когда используются временные протезы молочной железы
20.7.2.3. Устройства для постоянного использования после частичного или полного удаления молочной железы
20.7.3. Основные аспекты ухода
20.7.4. Цели ухода
20.7.5. Полновесные силиконовые протезы молочных желез
20.7.6. Легковесные протезы
20.7.7. Протезы для замещения части железы
20.7.8. Самоклеящиеся силиконовые протезы, которые прикрепляются непосредственно к стенке грудной клетки
20.7.9. Сосок
20.7.10. Типы и использование протезов.
20.7.10.1. Симметричные протезы для использования на любой стороне
20.7.10.2. Асимметричные протезы для использования на определенной стороне
20.7.10.3. Протезы, изготовленные на заказ
20.7.11. Аксессуары
20.7.11.1. Специальные бюстгальтеры после мастэктомии
20.7.11.1.1. Использование и функции постмастэктомических бюстгальтеров
20.7.11.2. Компрессионные бюстгальтеры
20.7.11.3. Постмастэктомические купальники
20.7.12. Парики































0 комментариев