Последствия недостаточности питания. Основы нутритивной поддержки в онкологии. Лекция для врачей
Лекция для врачей "Последствия недостаточности питания. Основы нутритивной поддержки в онкологии" (отрывок из книги "Основы нутритивной поддержки в онкологической клинике" - Салтанов А. И.)
Понятия. терминология. Эпидемиология
Показания к НП опираются на современные представления о недостаточности питания. На наш взгляд, этот термин предпочтителен по сравнению с другими обозначениями данного патологического состояния — трофическая или нутритивная недостаточность.
Для диагностики степени недостаточности питания предложено много критериев, однако наиболее распространена оценка недостаточности питания по темпам потери массы тела (МТ), предложенная A.Goode в 1981 г.:
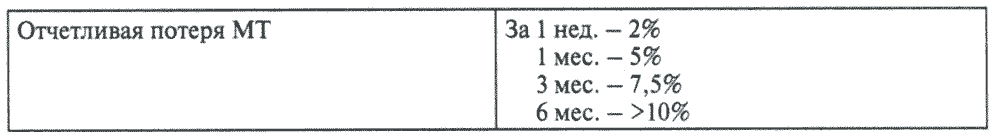
У онкологического больного, находящегося на лечении в клинике, недостаточность питания может прогрессировать в результате суммирования различных факторов. Это: 1) простое длительное голодание в результате блокады опухолью естественных путей приема пищи; 2) недостаточное восполнение энергетических затрат в результате повышенного обмена веществ (состояние гиперметаболизма); 3) распад тканевых белков (гиперкатаболизм) и липолиз; 4) сочетание так называемой опухолевой анорексии с нейрогенной на фоне опухолевого и «госпитального стресса».
В последние годы интенсивно изучается влияние реакции системного воспалительного ответа на рост опухоли, вызванной выбросом в кровь биологически активных соединений, обусловливающих дальнейшее развитие синдрома кахексии-анорексии.
Эпидемиология недостаточности питания
Поданным ESPEN (2000 г.), первое место в клинической медицине по распространенности недостаточности питания занимает онкология — 46—88% пациентов (см. табл. 1.1—1.3).
Наиболее часто нутритивная недостаточность встречается при раке желудка и поджелудочной железы (75—80%), однако имеет место и при опухолях других локализаций — легких, ободочной кишки, простаты (54—64%), молочной железы, различных саркомах, гемобластозах (31—40%). У 40% онкологических больных наличие выраженной гипотрофии не позволяет осуществлять адекватное лечение (Knox L.S. et al., 1995).
Таблица 1.1 Распространенность недостаточности питания (ESPEN, 2000)

Таблица 1.2 Частота недостаточности питания у онкологических больных (Knox L.S. et al., 1995)

Таблица 1.3 Частота недостаточности питания при опухолях различных локализаций и форм (ESPEN, 2000)

По данным ECOG (2004), при обследовании более 3000 пациентов потеря веса на 10% за 6 мес. до химиотерапии была выявлена в среднем у 60% больных, из них при раке яичка - у 25%, раке молочной железы - 36%, саркоме мягких тканей - 39%, раке легкого — 50%, лимфомах - 55%, раке простаты — 56%, нейробластоме — 56%, мелкоклеточном раке легкого — 60%, раке легкого — 61%, колоректальном раке — 54%, раке пищевода - 79%, раке поджелудочной железы - 83%, раке желудка - 83%.
Формы недостаточности питания
Катаболизм висцеральных протеинов проявляется нарушением целостности клеток (loss of cellular integrity), расстройствами иммунитета, снижением функции энзимов, что в целом приводит к тяжелым последствиям (рис. 1.1).
Формы дефицита питания подразделяют на острые и хронические.
Острая недостаточность питания (типа «квашиоркор») описывается как белковое истощение с сохранением запасов жира. Больной, несмотря на отсутствие существенных потерь веса и даже кажущуюся полноту, теряет большое количество белка. Термин «квашиоркор» взят из африканского названия «красный Кваши» (на русский язык переводится как «золотой или красный мальчик по имени Кваши»), обозначает злокачественное расстройство питания («детская пеллагра») в форме острой белковой недостаточности.
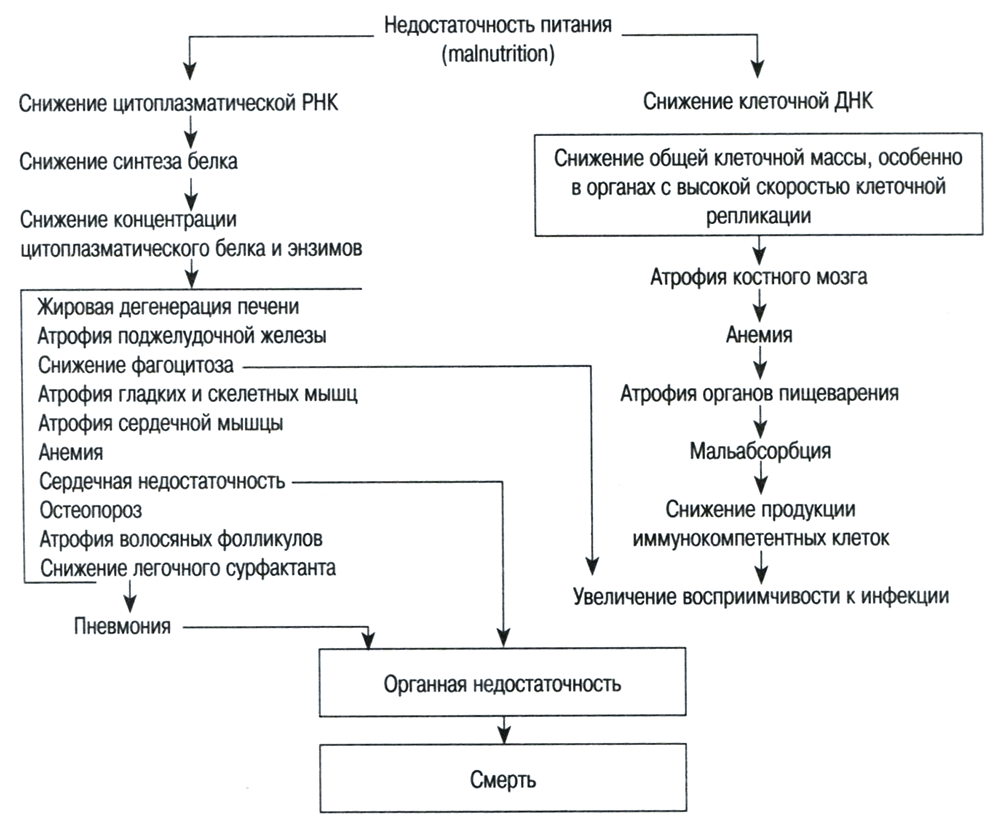
Рис. 1.1. Патогенез и последствия недостаточности питания онкологических больных.
Симптомы: истощение висцеральных белков, нормальный или даже увеличенный уровень жира в организме, нормальный или повышенный вес больного, отеки, изменения волос (сухость и непрочность), вялое и медленное заживление ран, признаки сниженной иммунологической реактивности.
Стрессорная форма голодания сопровождается повышенной секрецией ряда катаболических гормонов, среди которых особое значение имеют адреналин, глюкагон и кортикостероиды. Повышение активности этих гормонов обусловливает развитие липолиза, глюконеогенеза и дальнейший катаболизм белков. Стресс-гормоны вызывают гипергликемию на фоне инсулинорезистентности, т.е. состояние преддиабета.
К. Barendregt, P.V.Soeters (2004) описывают голодание при стрессе как квашиоркор. При этом развивается гипоальбуминемия, в связи с чем возможно появление отеков (также за счет нарушения сосудистой проницаемости под влиянием цитокинов). В результате этих процессов вода, электролиты и альбумин диффундируют во внесосудистый сектор. Снижение объема циркулирующей крови (ОЦК) вызывает вторичный гиперальдостеронизм, что еще более усиливает отечность тканей.
Клинически острую фазу стрессорного голодания описывают как сочетанное снижение концентрации альбумина, преальбумина и трансферрина, повышение индикаторов воспалительной реакции, уровня внеклеточной и общей воды в организме, резко отрицательный азотистый баланс, повышение энергетических затрат и потребностей (гиперметаболизм). МТ в этой фазе может не снижаться.
Вклад в острую форму недостаточности питания вносит синдром системного воспалительного ответа (ССВО, SIRS), детально исследованный в последнее десятилетие.
Медиаторы ССВО (Бэлк Р., 1995; Зильбер А. П., 1995; Bone R.C., 1996; Гельфанд Б. Р. и др., 1996; Bone R., 1999) представлены следующими группами биологически активных веществ:
• цитокины — хемокины, колониестимулирующий фактор, интерлейкины, интерфероны, фактор некроза опухоли (TNF);
• плазматические энзимные факторы - комплемент, факторы свертывания, фибринолитические факторы, калликреин/кинины;
• метаболиты арахидоновой кислоты (эйкозаноиды) — лейкотрие-ны, простагландины, тромбоксаны;
• фактор, активирующий тромбоциты;
• токсические продукты кислородного обмена — перекиси, гидроксид-радикалы, супероксиданионы;
• прочие — эндотелии, оксид азота, протеазы.
Если при большинстве заболеваний инфекционного характера источниками выделения в кровь цитокинов являются макрофаги и нейтрофилы, то при злокачественных опухолях выброс цитокинов осуществляется самими новообразованиями. Роль цитокинов представлена более подробно в разделе «Синдром анорексии-кахексии» (см. гл. 2). Здесь же хочется подчеркнуть, что острая форма недостаточности питания у онкологических больных развивается при воздействии двух основных факторов — стрессорного и воспалительного. Работы последних лет, посвященные так называемому окислительному стрессу, позволяют считать не менее важным в генезе острой недостаточности питания оксидантный фактор. Именно при сочетании этих трех факторов (стрессорного, воспалительного и оксидантного) и развивается кахексия - практически неуправляемое и, в большинстве случаев, терминальное состояние недостаточности питания.
Хроническая форма недостаточности питания (типа «маразм») обусловлена истощением и белковых, и жировых запасов. Описывается как классическая форма истощения (так называемый голодный пациент с анамнезом недоедания без явлений гиперкатаболизма).
Симптомы: существенное снижение уровня соматических белков по сравнению с висцеральными, истощение запасов жира, постепенное нарастание истощения.
В клинической практике, особенно в онкологии, чаще наблюдается смешанная форма недостаточности питания, при которой имеются признаки и маразма, и квашиоркора.
Весьма важным является современное представление о фазах перехода недостаточности питания к болезни. Учитывается ряд факторов, среди которых одними из ведущих являются нарушения нервнопсихической сферы.
Согласно современной концепции, симптомы острого воспалительного ответа суммируются с так называемой нейрогенной анорексией. При этом недостаточность питания в большей степени приобретает признаки квашиоркора. Это особенно остро проявляется при синдроме полиорганной недостаточности.
Таблица 1.4 Клинические формы недостаточности питания

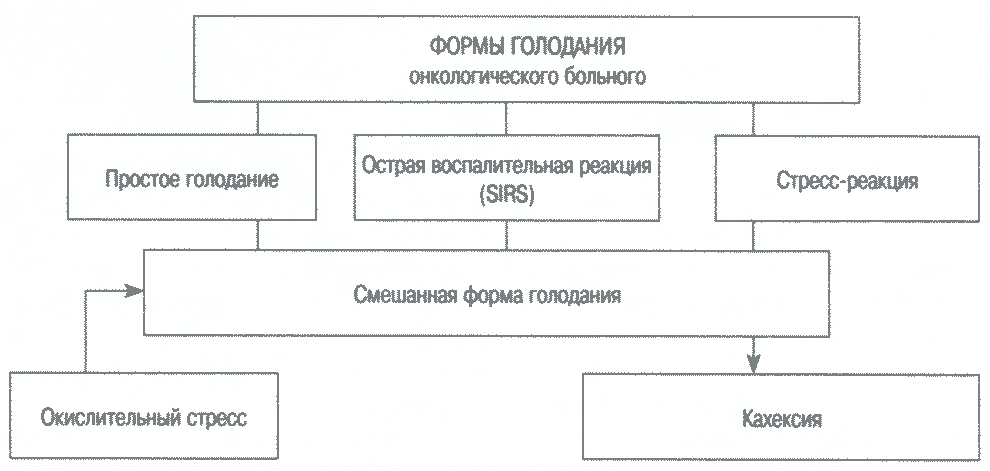
Рис. 1.2. Формы голодания онкологических больных.
Следует отметить, что у больных, страдающих злокачественными опухолями, темпы и интенсивность нарастания симптомов недостаточности питания могут значительно отличаться, что во многом зависит от биологической агрессивности новообразования.
Таким образом, учитывая гетерогенность популяции онкологических больных и разнообразные причины, являющиеся приоритетными в каждом отдельном случае, следует установить форму голодания с характерными для нее изменениями метаболизма (простое длительное голодание, голодание у больных с признаками реакции системного воспалительного ответа, голодание в условиях стресса). В запущенных стадиях опухолевого процесса преобладает смешанная форма голодания, ведущая к кахексии (рис. 1.2).
В онкологической клинике достаточно большой процент составляют больные без видимых проявлений недостаточности питания, встречаются больные с повышенной МТ (Шапошников А.В., 2002). Отсутствие симптомов недостаточности питания не должно усыплять бдительность врача, так как это происходит за счет процессов, временно компенсирующих белковые и энергетические потери. Об этом неустанно напоминают ведущие нутрициологи, работающие в онкологических клиниках (Bozzetti Е, Cozzaglio L. et al.). Именно эти исследователи неоднократно указывали и на возможность образования порочного круга: воздействие недостаточности питания на рост опухоли и наоборот — воздействие опухоли на прогрессирование питательной недостаточности.
Последствия недостаточности питания
В хирургии и, в частности, в онкохирургии, недостаточность питания может приводить к следующим нежелательным последствиям:
• более частому развитию раневой и нозокомиальной (госпитальной) инфекции;
• замедленному заживлению операционной раны;
• увеличению продолжительности ИВЛ;
• увеличению продолжительности лечения в условиях палаты интенсивной терапии;
• повышению медикаментозной нагрузки и затрат на лечение больного.
Кроме того, известны последствия недостаточности питания в отношении функции органов и систем организма. Так, G.L.Hill (1992) отметил угнетение психологического состояния госпитализированных больных. Особой проблемой является истощение миокарда при недостаточности питания, что ведет к сердечной недостаточности и нарушениям гемодинамики, которые, в свою очередь, усиливают недостаточность питания, замыкая порочный круг в развитии так называемой сердечной кахексии. Реальную опасность представляет недостаточность питания и для респираторной функции, что может определяться истощением мышц диафрагмы и вести к снижению объемов и емкостей легких. Описаны нарушение температурной реакции на холод у людей, находящихся в состоянии недостаточности питания, а также невозможность адаптироваться к понижению температуры окружающей среды.
При недостаточности питания резко снижается клеточный и гуморальный иммунитет. Имеются, в частности, указания на то, что при существенной потере веса (>10%) клеточный иммунитет ослаблен. Т-клеточная функция изменяется при определенных онкогематологических заболеваниях; В-клеточный иммунитет страдает в большей степени при хроническом лимфолейкозе и миеломной болезни. Дефицит иммуноглобулина А, отмечаемый у многих пациентов с недоеданием, может играть роль в абсорбции эндотоксинов и бактериальной транслокации в систему циркуляции.
Влияние недостаточности питания на желудочно-кишечный тракт (ЖКТ) является предметом особого обсуждения (см. гл. 2, раздел «Синдром кишечной недостаточности»).
Вы читали отрывок из книги "Основы нутритивной поддержки в онкологической клинике" - Салтанов А. И.
Купить книгу "Основы нутритивной поддержки в онкологической клинике" - Салтанов А. И.

Книга "Основы нутритивной поддержки в онкологической клинике"
Автор: Салтанов А. И.
Настоящая книга посвящена основным проблемам нутрициологии в онкологической клинике. Среди них одной из главных является оценка недостаточности питания онкологических больных. Этот раздел включает эпидемиологию, формы и последствия недостаточности питания у больных, страдающих злокачественными новообразованиями. Представлены наиболее значимые синдромы недостаточности питания в условиях метаболического ответа на тяжелое заболевание - синдромы анорексии-кахексии, гилерметаболизма-гиперкатаболизма. Особо выделен синдром кишечной недостаточности, прогрессирование которого ведет к полиорганной недостаточности и критическому состоянию пациента.
Отражены местные и системные факторы патологического воздействия злокачественной опухоли на статус питания. Представлены сведения о роли лечебных факторов, носящих по отношению к опухоли агрессивный характер и, вместе с тем, создающих побочные эффекты, требующие сопроводительной интенсивной терапии с включением в нее нутритивной поддержки.
В руководстве представлены современные методы оценки статуса питания и расчеты энергетических потребностей. Значительное место уделено вопросам применения средств парентерального и энтерального питания в современной онкологической клинике.
Представлены тактические и технические вопросы нутритивной поддержки при хирургическом лечении больных и при развитии хирургических осложнений. Отражена проблема нутритивной поддержки при осложнениях лучевой и химиотерапии, при лечении больных с сопутствующим диабетом, печеночной и почечной недостаточностью. Отдельная глава посвящена алгоритмам и протоколам нутритивной поддержки в онкологической клинике.
Предназначена для врачей-онкологов, реаниматологов и специалистов по интенсивной терапии, а также клинических ординаторов и аспирантов указанных специальностей.
Купить книги по нутрициологии в интернет-магазине медицинской книги shopdon.ru
Содержание книги "Основы нутритивной поддержки в онкологической клинике" - Салтанов А. И.
Часть 1. Недостаточность питания
Глава 1. Понятия. Терминология. Эпидемиология
1.1. Эпидемиология недостаточности питания
1.2. Формы недостаточности питания
1.3. Последствия недостаточности питания
Глава 2. Синдромы недостаточности питания
2.1. Патофизиология метаболического ответа на повреждение
2.2. Синдром анорексии-кахексии
2.3. Синдром гиперметаболизма-гиперкатаболизма
2.4. Синдром кишечной недостаточности
Глава 3. Факторы патологического воздействия на статус питания
3.1. Влияние опухоли
3.2. Влияние лечебных (ятрогенных) факторов
3.2.1. Хирургическое лечение
3.2.2. Лучевая терапия
3.2.3. Химиотерапия
Глава 4. Оценка статуса питания и энергетических потребностей
4.1. Оценка статуса питания
4.2. Расчеты потребности в энергии и нутриентах
Часть 2. Парентеральное и энтеральное питание
Глава 5. Исторические аспекты искусственного питания
5.1. Парентеральное питание
5.2. Энтеральное питание
Глава 6. Субстраты для обеспечения энергией при парентеральном питании
6.1. Средства обеспечения организма энергией
6.1.1. Углеводы
6.1.2. Жировые эмульсии
Глава 7. Субстраты, применяемые для пластических целей
7.1. Смеси кристаллических аминокислот
7.2. Фармаконутриенты
7.2.1. Аминокислоты
7.3. Микронутриенты
7.4. Растворы кристаллических аминокислот со специфическим фармакологическим действием
7.5. Технологии парентерального питания
Глава 8. Энтеральное питание
8.1. Способы энтерального питания
8.1.1. Энтеральное зондовое питание
8.2. Питательные смеси
8.2.1. Характеристика полимерных сбалансированных смесей (ПСС)
8.2.2. Питательные смеси с пищевыми волокнами (ПВ)
8.2.3. Смеси для перорального применения
8.3. Новые препараты для энтерального питания
Часть 3. Нутритивная поддержка онкологических больных в период лечения
Глава 9. Нутритивная поддержка в онкохирургии
9.1. Нутритивная поддержка в периоперационном периоде
9.2. Нутритивная поддержка в плановой онкохирургии
9.2.1. Нутритивная поддержка при раке желудка
9.3. Моторно-эвакуаторные нарушения
9.4. Острый панкреатит
9.5. Свищи желудочно-кишечного тракта
9.6. Синдром короткой кишки
9.6.1. Выбор препаратов для энтерального питания
9.7. Перитонит
Глава 10. Нутритивная поддержка при осложнениях лучевой и химиотерапии
10.1. Печеночная недостаточность и рациональная нутритивная поддержка
10.2. Нутритивная поддержка при мукозитах, обусловленных химио- и/или лучевой терапией
Глава 11. Нутритивная поддержка при сопутствующей патологии
11.1. Нутритивная поддержка при сахарном диабете
11.2. Нутритивная поддержка при почечной недостаточности
11.2.1. Влияние нарушения функции почек на белковый метаболизм при ОПН
11.2.2. Оценка выраженности белкового катаболизма
11.2.3. Метаболизм глюкозы при ОПН
11.2.4. Метоболизм липидов при ОПН
11.2.5. Метаболический эффект экстракорпоральной терапии
11.2.6. Влияние питания на почечную функцию при ОПН
11.2.7. Принципы принятия решения по питательной терапии при ОПН
11.2.8. Энтеральное питание при ОПН
11.2.9. Рекомендации при нутритивной поддержке при ОПН
Глава 12. Протоколы и алгоритмы нутритивной поддержки
Приложения
Приложение 1. Растворы кристаллических аминокислот
Приложение 2. Жировые эмульсии
Приложение 3. «Все в одном»
Приложение 4. Полимерные сбалансированные смеси для энтерального питания
Приложение 5. Полуэлементные смеси для энтерального питания
Приложение 6. Микроэлементы
Купить книги по нутрициологии в интернет-магазине медицинской книги shopdon.ru























0 комментариев