Бесплодие и эндометриоз. Клинические формы бесплодия, ассоциированного с эндометриозом. Лекция для врачей
Лекция для врачей "Бесплодие и эндометриоз. Клинические формы бесплодия, ассоциированного с эндометриозом" (отрывок из книги "Бесплодие и эндометриоз. Версии и контраверсии" - В. Е. Радзинский, М .Р. Оразов)
Клинические формы бесплодия, ассоциированного с эндометриозом
Ключевые положения
В отношении эндометриоз-ассоциированного бесплодия в настоящее время доказано следующее.
1. Клинические формы инфертильности зависят от локализации гетеротопий: овариальный эндометриоз, трубно-перитонеальный, миометральный, эндометриальный (ассоциированный с патологическими изменениями в эндометрии) факторы (уровень доказательности II).
2. Врачи должны быть осведомлены о возможности атипичной локализации эндометриоидных гетеротопий (уровень доказательности I)2.
3. Симптомы и признаки, связанные с эндометриозом:
- усталость, симптомы ментального дистресса;
- дисменорея;
- хроническая тазовая боль;
- диспареуния;
- циклические диспептические расстройства;
- бесплодие (уровень доказательности III).
Согласно международным руководствам с соблюдением стандартов надлежащей клинической практики (Good clinical practice, GCP):
- рекомендовано исключать эндометриоз-ассоциированное бесплодие при наличии таких «гинекологических» симптомов, как:
- дисменорея;
- нециклическая боль в области таза;
- диспареуния;
- бесплодие;
- рекомендовано исключить эндометриоз у женщин репродуктивного возраста с негинекологическими циклическими симптомами1’2:
- дисхезией;
- дизурией;
- гематурией;
- ректальным кровотечением;
- болью в плече.
Дискуссионные аспекты. Все исследования имели ретроспективный дизайн и не показали прогностическую ценность указанных симптомов в отношении наличия эндометриоза (уровень доказательности III).
Существует множество клинических форм эндометриоза, каждая из которых вносит свой вклад в формирование инфертильности. Всё чаще звучит мысль о том, что любая локализация гетеротопий представляет собой патогенетически отдельное поражение*.
Мысль эта хоть и не бесспорна, но может быть полезной при обсуждении эндометриоз-ассоциированного бесплодия, поскольку очевидно, что многообразие локализаций гетеротопий обусловливает разные причины невозможности зачатия. Заболевание, распространяясь лимфогенным и гематогенным путями, поражает практически все органы и ткани: в первую очередь органы малого таза — матку, яичники, фаллопиевы трубы, крестцово-маточные связки, толстую кишку и мочевой пузырь (рис. 3-1), реже — почки, лёгкие, конъюнктиву глаз, носовую полость.
Pro
Федеральные клинические рекомендации (2016) содержат несколько классификаций эндометриоза:
- по морфофункциональным особенностям;
- по клиническим проявлениям;
- по анатомическим характеристикам;
- по необходимому объёму вмешательства.
Сейчас есть возможность рассчитывать индекс фертильности при эндометриозе (endometriosis fertility index, EFI) для прогнозирования вероятности беременности у пациенток с бесплодием после хирургических диагностики и лечения.
Наконец, унификация диагнозов сегодня должна соответствовать регламенту международной классификации болезней 10-го пересмотра (МКБ-10). Разработаны классификации аденомиоза, эндометриом, ретроцервикального эндометриоза. Каждая из них включает четыре стадии распространения эндометриоидного процесса.
Главной классификацией, кроме МКБ-10, продолжает оставаться предложенная ещё в 1979 году (40 лет назад!) Американским обществом фетильности (American fertility society, AFS), переименованным с 1995 года в Американское общество репродуктивной медицины (American society of reproductive medicine, ASRM). В 1997 году классификация AFS/ASRM была пересмотрена и дополнена. Система основана на оценке тяжести заболевания при лапароскопической визуализации (табл. 3-1):
- I стадия (5 баллов и менее);
- II стадия (6-15 баллов);
- III стадия (16-40 баллов);
- IV стадия (более 40 баллов).
___________________________
* Различия форм эндометриоза нашли отражение в обновлённой МКБ-11, которая вступит в силу с 1 января 2022 года. По этой классификации аденомиоз выделен как самостоятельное заболевание.
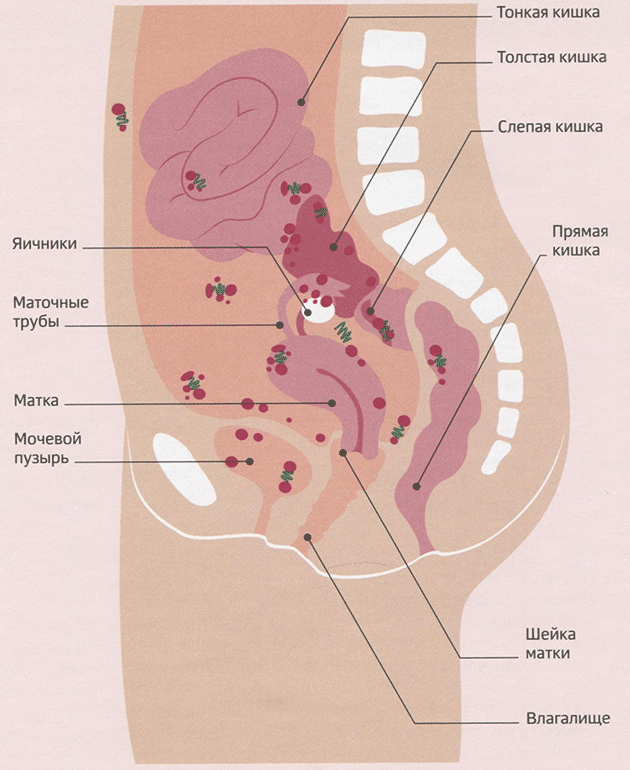
Рис. 3-1. Локализация эндометриоидных очагов.
Таблица 3-1. Классификация AFS/ASRM
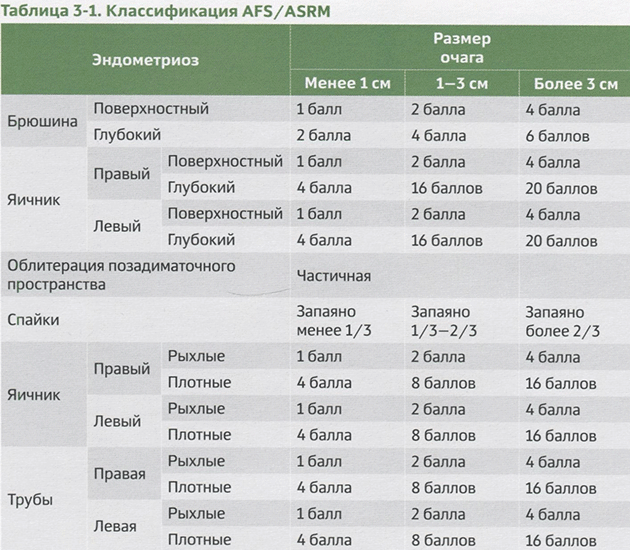
Такой подход обоснован прежде всего международным стандартом оценки тяжести эндометриоза и сравнения терапевтических результатов (удобно сопоставлять разные исследования). Классификация AFS/ASRM входит в оценку индекса EFI (рис. 3-2). Кроме того, в опросник EFI включена шкала LF (least function score) для расчёта наименьшей функции: необходимо выбрать наименьший балл в каждой из колонок (слева и справа) и сложить их. Например, в случае отсутствия одного из яичников нужно удвоить выбранный балл из другой колонки.
Индекс фертильности варьирует от 0 до 10, а для прогноза частоты наступления беременности используют номограмму (рис. 3-3).
Шкала LF для определения минимальной сохранённой функции
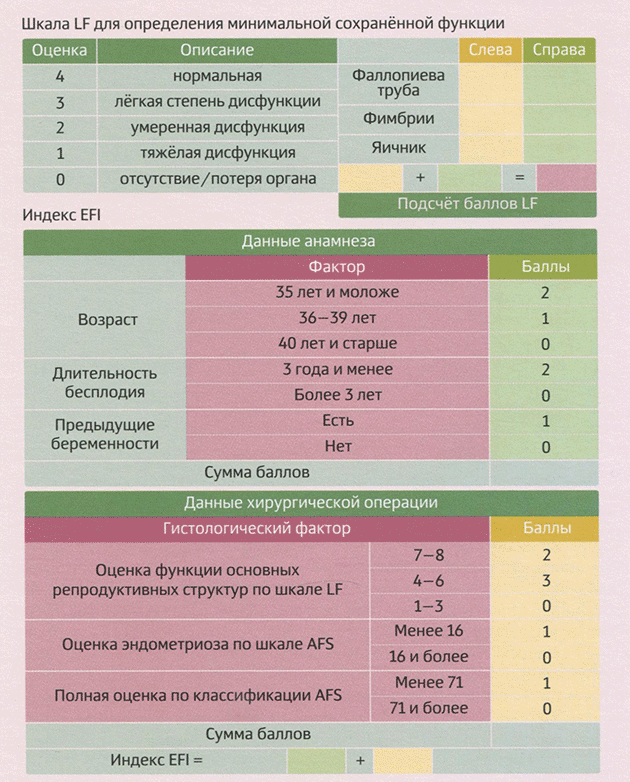
Рис. 3-2. Опросник для подсчёта индекса EFI. Он позволяет предсказать вероятность наступления беременности в естественном цикле у женщин с хирургически подтверждённым эндометриозом.
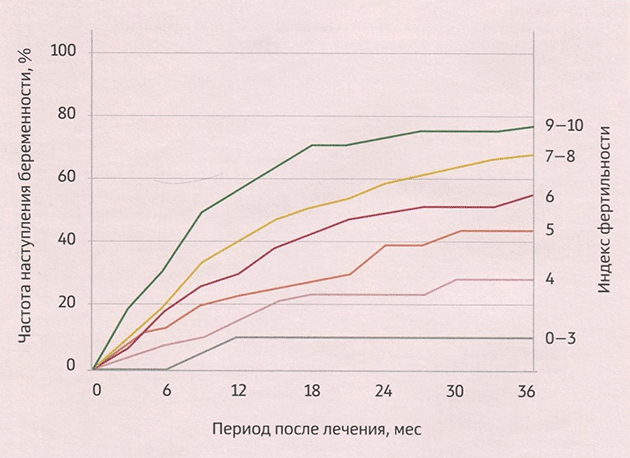
Рис. 3-3. Клиническая оценка индекса фертильности EFI.
Классификация AFS/ASRM не лишена недостатков, главный из которых — частое несоответствие стадии распространения и истинной тяжести поражения, а также отсутствие должной оценки инфильтративных форм (ретроцервикальный эндометриоз и др.). В связи с этим для описания более тяжёлых инвазивных форм заболевания в дополнение к классификации хирургами-эндоскопистами в 2005 году был разработан новый инструмент — классификационная система ENZIAN22. Однако она не систематизирована, принята не во всех странах и больше направлена на прогнозирование заболевания. Основное преимущество шкалы ENZIAN — топографическое отображение эндометриоза.
Et contra
Интерпретация результатов по существующим классификациям неоднозначна: хотя лапароскопия с последующим морфологическим исследованием и представляет собой «золотой стандарт» диагностики, перитонеальный эндометриоз сложно распознать визуально, очаги глубокого инфильтративного эндометриоза часто скрыты под брюшиной, а отрицательные результаты морфологического исследования не исключают заболевания.
Классификация AFS/ASRM не лишена недостатков, главный из которых — частое несоответствие стадии распространения и истинной тяжести заболевания.
Кстати, именно этим проблемам был посвящён Глобальный консенсус по эндометриозу в 2016 году. Эксперты Всемирного общества по эндометриозу (World endometriosis society, WES) пришли к выводам: современные классификации требуют серьёзной переработки. И работа в этом направлении уже началась.
Точка зрения
Пока мы ждём модернизации или создания новых классификационных инструментов, следует признать: однозначно установить факт наличия, стадию и клиническую форму эндометриоза подчас не просто трудно, но в некоторых случаях практически невозможно. Результативность напрямую зависит от квалификации хирурга и его способности осмысливать разнообразные симптомы, вызванные локализацией гетеротопий. Что уж говорить об обнаружении действительной причины бесплодия при эндометриозе! Ведь все перечисленные классификации не способны полноценно его охарактеризовать.
Трубно-перитонеальное бесплодие на фоне эндометриоза с позиций доказанного и дискутабельного
Трубно-перитонеальное бесплодие — наиболее логичное следствие наружного эндометриоза. Локализация очагов может быть и перитонеальная, и яичниковая, и собственно тубарная. Однако парадоксален тот факт, что у пациенток с наружным генитальным эндометриозом при начальных стадиях распространённости в большинстве случаев маточные трубы проходимы. На фоне воспалительных явлений с изменённой иммунной активностью гетеротопии приобретают тенденцию к распространению, чем и обусловлен выраженный хронический спаечный процесс (рис. 3-4). Очень часто его случайно находят при лапароскопии, проводимой по поводу бездетности. Не менее 30% всех причин трубно-перитонеальной инфертильности женщин составляет именно эндометриоз.
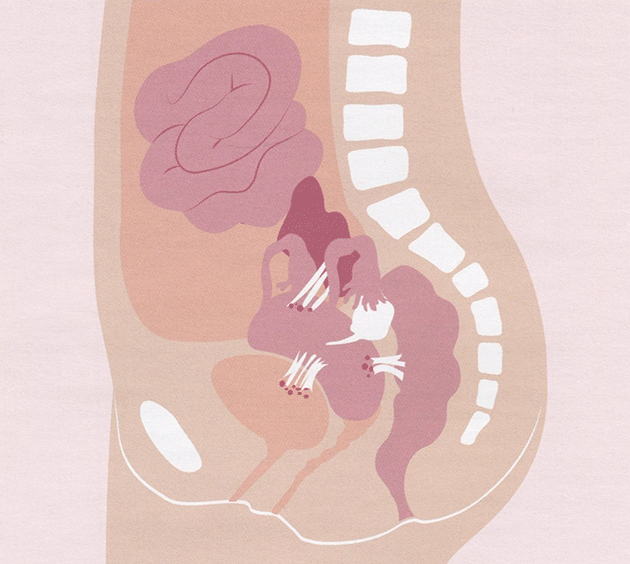
Рис. 3-4. Спаечный процесс при наружном генитальном эндометриозе.
Pro
Отсутствие беременности — лишь симптом, с которым бесплодная пара приходит к врачу. Задача же специалиста — максимально быстро выявить истинную причину инфертильности, поставив диагноз. При этом крайне важно соблюдать оптимальный стандартизованный алгоритм — его нарушение затягивает обследование, увеличивает риск врачебной ошибки, то есть направляет по заведомо ложному маршруту. Порядок диагностических действий хорошо известен. Однако анамнез пар, длительно обследуемых по поводу бесплодия, нередко говорит о вопиющем пренебрежении начальными этапами обследования.
Врачам хорошо известен порядок диагностических действий. Однако анамнез пар, длительно обследуемых по поводу бесплодия, нередко говорит о вопиющем пренебрежении начальными этапами обследования.
Порой акушер-гинеколог в первую очередь ведёт поиск эндокринных, ановуляторных факторов инфертильности даже у женщин с регулярным циклом и отсутствием клинических проявлений эндокринопатий. Поэтому клиницистам крайне важно знать, что после тщательного сбора анамнеза и исключения мужского фактора бездетности для уточнения диагноза необходимо сделать гистеросальпингографию (ГСГ) любым доступным способом — рентгеновскую или сонографическую. Они обладают сопоставимыми чувствительностью (84%) и специфичностью (74,5%) в выявлении трубно-перитонеального бесплодия. Методика хорошо известна и описана во многих учебниках и пособиях.
Публикации последних лет подчёркивают, что гистеросальпингография (ГСГ) имеет не только диагностическую значимость: исследователи из Омана в 2013 году продемонстрировали некоторые терапевтические свойства рентгеноконтрастных веществ в отношении эндометриоза в маточных трубах. Интересно, что много современных, не старше пятилетних, публикаций неожиданно посвящено известному более полувека контрастному веществу липиодолу, используемому для сальпингографий. Несколько рандомизированных контролируемых исследований свидетельствует о его благотворном влиянии на фертильность женщин, страдающих эндометриоз-ассоциированным бесплодием. Этот эффект авторы объясняют в первую очередь механическим удалением соединительнотканных разрастаний в маточных трубах. Кроме того, отмечают вероятный иммунобиологический эффект.
Так, в рандомизированном контролируемом исследовании, проведённом в Австралии в 2014 году, констатировали беременность после гистеросальпингографии (ГСГ) с липиодолом у 50 из 124 женщин (40,2%) в возрасте до 40 лет с двусторонней трубной непроходимостью разного генеза, включая эндометриоз. Выборка пациенток с трубно-перитонеальным бесплодием, хотя и меньшая по объёму, показала сопоставимые результаты: восемь из 17 (47,1%) пациенток самостоятельно забеременели после гистеросальпингографии (ГСГ) с липиодолом. Эти результаты авторы объясняют снижением экспрессии остеопонтина и уменьшением содержания NK-клеток в эндометрии и брюшине, что оказывает поддержку «имплантационного окна».
Справедливости ради следует отметить, что описанные данные сопоставимы с более ранними работами. Однако в условиях рандомизированных контролируемых исследований эффективность липиодола никогда не сравнивали с хирургическим вмешательством — удалением эндометриоидных гетеротопий.
Публикации последних лет подчёркивают, что ГСГ имеет не только диагностическую значимость: были продемонстрированы некоторые терапевтические свойства рентгеноконтрастных веществ в отношении трубного эндометриоза.
Выполнение ГСГ с липиодолом может быть эффективно для преодоления трубно-перитонеального бесплодия супружеских пар в силу своей безопасности, минимальной инвазивности, дешевизны и возможности многократного повторения. Так, в Консенсусе по лечению эндометриоза Европейского общества по репродукции человека и эмбриологии (European society of human reproduction and embryology, ESHRE), в разработке которого принимали участие 56 представителей из 34 национальных и международных медицинских и немедицинских организаций, большинство экспертов сошлись во мнении, что такое вмешательство улучшает показатели наступления беременности и живорождений у женщин с эндометриоз-ассоциированным бесплодием и инфертильностью неясного генеза.
В исследовании 2012 года было показано, что пациентки с трубно-перитонеальным бесплодием имеют гораздо больше удачных исходов беременностей, наступивших с помощью ВРТ, в сравнении с теми, у кого была диагностирована I—II стадия по классификации AFS/ASRM.
Исходя из вышеизложенного, можно заключить, что терапия бездетных пациенток с трубным эндометриозом даёт большую эффективность (что подтверждают результаты ВРТ), чем лечение женщин с другой локализацией гетеротопий или с более тяжёлыми стадиями заболевания.
Et contra
Несмотря на ранее описанные преимущества гистеросальпингографии (ГСГ), «золотой стандарт» в диагностике трубного бесплодия — лапароскопическая хромопертубацияили её сочетание с ГСГ. Преконцепционный лапароскопический адгезиолизис при трубно-перитонеальном факторе эндометриоз-ассоциированной инфертильности улучшает репродуктивные исходы на 60%. Недостатки данной процедуры — дороговизна, инвазивность и анестезиологический риск.
Нужно добавить, что в сложившейся ясности изложенных фактов о трубно-перитонеальном факторе эндометриоз-ассоциированного бесплодия есть и «ложка дёгтя». В крупном контролируемом исследовании, проведённом в Индии в 2014 году, сравнивали репродуктивные исходы ВРТ у женщин с III—IV стадией эндометриоза и с неэндометриоидным трубным бесплодием (контроль). Было обнаружено, что качество и количество полученных ооцитов и потенциал фертилизации были значительно хуже у женщин с эндометриозом в сравнении с пациентками контрольной группы, то есть, помимо нарушения проходимости маточных труб, существуют дополнительные факторы, препятствующие преодолению бесплодия.
Точка зрения
Вопрос истинного влияния эндометриоидного процесса на возникновение трубно-перитонеального бесплодия по-прежнему открыт и, видимо, взаимосвязан с дополнительным негативным влиянием на ооциты при овариальной форме заболевания.
Овариальный эндометриоз и бесплодие: существует ли взаимосвязь?
Овариальный эндометриоз — наиболее распространённая форма наружного генитального эндометриоза. Он известен с тех самых пор, как в 1860 году К. фон Рокитанским впервые была описана «шоколадная киста» яичника, названная так из-за специфического дёгтеобразного содержимого. Такие кистозные изменения выявляют у 10-15% женщин, оперированных по поводу объёмных образований органов малого таза.
Часто, протекая бессимптомно, заболевание бывает случайной находкой: при пальпации обнаруживают увеличенный яичник и/или отмечают новообразование при рутинном ультразвуковом исследовании (УЗИ). Подозрение на овариальную эндометриому может возникнуть, когда женщины предъявляют жалобы на тянущую боль внизу живота. Микроперфорация или разрыв камеры кисты с истечением содержимого в брюшную полость сопровождается вторичным вовлечением брюшины и развитием хронического спаечного процесса, а иногда развитием клинической картины «острого живота».
Pro
Связь овариального эндометриоза и бесплодия вроде бы достаточно очевидна. Она основана не только на осложняющем его спаечном процессе (при этом важны длительность заболевания и размер новообразований), но и на возможном снижении овариального резерва у пациенток с эндометриомой, а также на неэффективности гормональной терапии и недостаточном ответе на стимуляцию яичников. Всё это вместе имеет следствием низкую эффективность преодоления бездетности, в том числе и при ВРТ.
Наличие эндометриомы неблагоприятно воздействует на овариальный резерв, снижение этого показателя становится ещё более очевидным вскоре после хирургического удаления образования.
Чем больше длительность существования образования, число эндометрием и их размеры, тем хуже ответ на гормональную стимуляцию овуляции, а значит, необходимы повышенные дозы гонадотропинов? Однако почему так происходит?
По мнению итальянских специалистов, для эндометриомы характерно механическое растяжение здоровой ткани яичника, и именно это ухудшает качество ооцитов. Тем не менее вывод авторов о независимости этих ухудшений от размера самой эндометриомы малологичен. Стоило бы ожидать обратного: чем больше размер опухоли, тем сильнее растянута соседняя ткань и тем ниже фертильность. Интересно и то, что механическое растяжение яичниковой ткани почему-то не ухудшает репродуктивную функцию при других новообразованиях.
Ответ на этот вопрос дают исследования (Япония, 2012): с помощью трансвагинального УЗИ измеряли плотность фолликулов в ткани яичников, прилежащей к разным новообразованиям. Оказалось, что этот показатель при одинаковом растяжении яичниковой ткани был значительно меньшим при эндометриоме, чем при других опухолях и кистах.
Возможно, провоспалительные изменения фолликулярной жидкости оказывают влияние на оогенез, при этом отмечают удлинение фолликулиновой фазы, уменьшение размеров доминантных фолликулов, активацию апоптоза клеток кумулюса. Нарушение нормальной гистоархитектоники коры яичников при овариальном эндометриозе влияет на пул примордиальных фолликулов. Помимо этого отмечают дистрофические процессы в тека- и гранулёзных клетках фолликулов, изменение состава фолликулярной жидкости, повышенный апоптотический индекс клеток гранулёзы, дегенерацию ооцитов.
Чем больше давность образования, число эндометриом и их размеры, тем хуже ответ на гормональную стимуляцию в программах ВРТ.
Дополнительным доказательством того, что эндометриома отрицательно влияет на ткань яичника, может быть анализ уровня антимюллерова гормона (АМГ) в крови. Его концентрация, считают итальянские коллеги (2014), значительно меньше, чем у пациенток того же возраста как без образований, так и с другими объёмными новообразованиями яичников или с трубно-перитонеальным бесплодием.
Et contra
Существует научно доказанная позиция: несмотря на пониженный ответ на стимуляцию яичников гонадотропинами у женщин с двусторонними (!) эндометриомами, количество эмбрионов высокого качества, успешных имплантаций и достигнутых в итоге беременностей и живорождённых детей у таких пациенток приблизительно такое же, как и в контрольной группе. Отсутствие влияния овариального эндометриоза на исход экстракорпорального оплодотворения (ЭКО) в сравнении с неэндометриоидным трубно-перитонеальным бесплодием было подтверждено целым рядом исследователей.
Изучение развития ооцитов, полученных из яичников с односторонними неоперированными эндометриоидными кистами, в сравнении с ооцитами из нетронутого контрлатерального яичника не выявило разницы в числе полученных ооцитов, количестве успешных подсадок, результатом которых стали жизнеспособные высококачественные эмбрионы.
Мнения относительно овариального резерва при эндометриоме яичника также контраверсионны. Хотя ряд исследований 1993-2014 годов доказывает значительное снижение овариального резерва у пациенток с образованиями; целый ряд работ, опубликованных в 2012-2015 годах, постулирует обратное.
Так, например, в итальянском исследовании 2015 года в течение 6 мес с помощью УЗИ отслеживали овуляции у 244 женщин с односторонней эндометриомой. Различий числа овуляций в зависимости от стороны патологического процесса, от числа гетеротопий в яичнике или их размера обнаружить не удалось. За время наблюдения 43% (105 из 244), то есть почти половина пациенток с эндометриомами, смогли самостоятельно забеременеть (95% ДИ 36,7-49,5%)53. Более точные, чем УЗИ, методы диагностики овариального резерва (уровень АМГ и ряд других маркёров) у женщин с овариальным эндометриозом также не показывают корреляций между поражениями яичников и овуляторной функцией.
Интересно, что разные по дизайну исследования продемонстрировали сопоставимые результаты обследования женщин, у которых на фоне эндометриомы развивалось бесплодие: 35,3% (у 307 из 870)55 и 36,4% (у 150 из 412).
Точка зрения
Сегодня многие авторы постепенно приходят к выводу, что эндометриома не связана с повышенным риском бесплодия. Следовательно, необходимость её удаления — дискуссионный вопрос, особенно при небольших размерах и при отсутствии какой-либо симптоматики, кроме жалоб на бездетность. Ведь само по себе оперативное вмешательство сделает то, к чему наличие эндометриомы доказанно не приводит, — снизит столь ценный овариальный резерв, ухудшив прогноз положительного результата ВРТ.
В доказательство последнего утверждения можно привести данные коллег из Франции, подсчитавших, что при удалении эндометриомы диаметром 5 см происходит потеря в среднем 46 ооцитов из остающейся здоровой ткани яичника.
Эндометриома не связана с повышенным риском бесплодия, поэтому необходимость её удаления — дискуссионный вопрос, особенно при небольших размерах и при отсутствии какой-либо симптоматики.
Интересно масштабное исследование 2012 года, в котором оценивали уровень АМГ до и после хирургического лечения эндометрием. По заключению авторов, ни эндометриоз вообще, ни эндометриома яичника в частности не снижают фолликулярный пул, оцениваемый по концентрации АМГ. Тем не менее после первого же хирургического лечения содержание этого гормона существенно падало — без взаимосвязи с рецидивами!
Однако отсутствие оперативного вмешательства при эндометриомах ввиду канцерогенного риска — весьма контраверсионная тема. В 2018 году опубликованы результаты крупномасштабного популяционного исследования рисков гинекологического рака в зависимости от локализации эктопированного эндометрия у 49 933 пациенток с хирургически подтверждённым эндометриозом. В течение 5-10 лет после хирургического лечения была установлена прямая корреляция (ОР 1,76; 95% ДИ 1,47-2,08) между эндометриозом и раком яичников. Риск резко возрастал при эндометриоидном (ОР 3,12; 95% ДИ 2,15-4,38) и светлоклеточном (ОР 5,17; 95% ДИ 3,20-7,89) гистологическом типе опухоли. При эндометриомах опасность овариальной малигнизации была наиболее высокой — ОР 4,72 (95% ДИ 2,75-7,56) и ОР 10,1 (95% ДИ 5,50-16,9) соответственно, тогда как при перитонеальной и глубокой инфильтративной формах эндометриоза риск не велик.
В других исследованиях связь между обсуждаемым заболеванием и овариальным раком не подтверждена. Авторы этих работ заявляют, что нет каких-либо доказательств того, что эндометриоидные гетеротопии обязательно подвергаются злокачественному перерождению. Генетические мутации были найдены в некоторых эндометриомах женщин с уже подтверждённым раком в том же самом яичнике, но подобные («связанные с раком») аберрации были также выявлены и в очагах глубокого инфильтративного эндометриоза, тогда как близкорасположенные опухоли не были обнаружены.
Однако, несмотря на контраверсионность мнений о риске малигнизации эндометриоидных гетеротопий, согласно российским клиническим рекомендациям, все образования в области придатков матки, выявленные во время гинекологического осмотра и/или при использовании визуализационных методик, должны быть тщательно исследованы и удалены оперативно с обязательным гистологическим исследованием удалённого очага. При возникновении подозрения на эндометриоидную кисту яичников нужно следовать рекомендациям по ведению женщин с овариальными опухолями, включая УЗИ и определение уровня опухолевых онкомаркёров, в том числе раковый антиген 125 (cancer antigen 125, СА-125).
Аденомиоз и бесплодие — логично о неоднозначном
Аденомиоз поражает, по разным подсчётам, от 5 до 50% женщин репродуктивного возраста. Такой широкий разброс данных связан с неточными критериями постановки диагноза (недоказанная гипердиагностика или, наоборот, недооценка состояния) и включением в исследуемые когорты пациенток с асимптомным течением или, напротив, только с клинически манифестированным аденомиозом.
Нелишним будет напомнить, что наиболее типичную клиническую картину аденомиоза составляют дисменорея, меноррагии и полименорея, нередко сопровождающиеся анемизацией пациентки.
Pro
Связь между наличием аденомиоза и репродуктивным потенциалом женщины до сих пор достоверно не ясна. На сегодняшний день существуют данные, что у женщин с аденомиозом наблюдают снижение фертильности. Итальянский систематический обзор с метаанализом современных публикаций об аденомиозе, проведённый в 2014 году, показал, что пациентки с доказанным аденомиозом имели значительно более низкие показатели наступления беременности (24,5%), чем женщины без аденомиоза (43,2%), с достоверным снижением риска (отношение шансов [ОШ] 0,55; 95% ДИ 0,32-0,96)64.
Одним из возможных механизмов отрицательного влияния аденомиоза на фертильность считают альтеративные изменения соединительно-маточной зоны с нарушением её гистоархитектоники и координационной активности миометрия.
Другой потенциальной причиной признают хронический аутоиммунный эндометрит, распространённость которого статистически значимо выше (в 2,7 раза) у женщин с эндометриозом в сравнении с женщинами без него (42,3 против 15,4% в контрольной группе) по результатам эндоскопического исследования полости матки — 38,5 против 14,1% — согласно данным морфологического исследования. Подобные результаты получены японскими исследователями, которые подтвердили, что эндометриоз ассоциирован с хроническим эндометритом, его выявили у 52,9% пациенток по сравнению с 27% женщин контрольной группы.
Et contra
Однако упомянутый выше метаанализ указывает на контраверсионные результаты разных авторов. Как бы то ни было, у 48,1% (99 из 206) пациенток с аденомиозом наступила беременность — в сравнении с 55,1% (383 из 695) в группе контроля.
Таким образом, выдвинутая гипотеза о меньшей фертильности пациенток с аденомиозом статистически не подтверждена, о чём свидетельствует ОШ - 0,84 (95% ДИ 0,67-1,06; р=0,22).
Почему результаты столь противоречивы? Чаще всего это итог неодинаковых методов исследования. Например, работы, основанные на данных УЗИ, вряд ли могут быть расценены как статистически достоверные. Напротив, применение МРТ даже без морфологического исследования увеличивает ценность выводов при изучении аденомиоза.
Так, из пациенток с аденомиозом, верифицированным посредством УЗИ, самопроизвольно забеременели 44,7% женщин (109 из 244), тогда как в группе контроля (без сонографических признаков маточной формы эндометриоза) — 48,3% (529 из 1095). В данном исследовании негативного влияния аденомиоза на фертильность женщин не обнаружено (ОШ 0,84; 95% ДИ 0,68-1,04). Тем не менее при использовании более достоверного метода исследования — МРТ — наличие внутреннего эндометриоза матки уменьшает шанс забеременеть почти вдвое (ОШ 0,4; 95% ДИ 0,25-0,64), что подтверждает гипотезу об отрицательном влиянии аденомиоза на фертильность.
Точка зрения
Итак, детальный анализ результатов множества исследований часто даёт недостаточно полную картину для адекватных выводов о влиянии аденомиоза на формирование бесплодия.
Скорее всего воспалительные изменения в эндометрии, нарушение его восприимчивости, синтеза факторов роста, а значит, снижение эффективности нидации и имплантации, а также других механизмов, описанных в предыдущих главах, уменьшают вероятность наступления беременности у женщин с истинным аденомиозом.
В 2012 году в Великобритании была статистически доказана более низкая эффективность имплантации перенесённого эмбриона при аденомиозе, из-за чего беременности в программах ВРТ наступали реже, чем у других пациенток, и в большинстве случаев заканчивались спонтанным абортом (ОШ 2,12; 95% ДИ 1,2-3,75). В целом аденомиоз оказывает негативное влияние на микроокружение плодного яйца, не способствуя нормальной имплантации, независимо от качества ооцитов и эмбриона.
Купить медицинскую литературу по акушерству и гинекологии в интернет-магазине shopdon.ru
Книга "Бесплодие и эндометриоз. Версии и контраверсии"
Автор: под ред. В. Е. Радзинского, М .Р. Оразова

Очередное нестандартное издание посвящено одной из главных проблем современной гинекологии – бесплодию, ассоциированному с эндометриозом. Эндометриоз до сих пор остаётся феноменом, скрывающим своё истинное лицо, “болезнью загадок и предположений”, а инфертильность на его фоне оказывается “проблемой внутри проблемы”. Гипотезы о том, как именно эндометриоз становится причиной бесплодия или снижает фертильность, противоречивы, и варианты врачебной тактики могут быть различными – и поэтому главной задачей книги было высветить все существующие дискуссионные вопросы.
В нестандартном ключе контраверсий (разделы “Pro”, “Et contra”, “Точка зрения”) представлены сведения о распространённости, этиологии и патогенезе бесплодия, обусловленного эндометриозом, с позиций доказательности обобщён мировой опыт диагностики, консервативных и хирургических методов лечения. В издании подробно и тщательно суммированы результаты наиболее значимых доказательных исследований по теме эндометриоза и инфертильности.
Издание предназначено исключительно для думающих акушеров-гинекологов и руководителей женских консультаций, родильных домов и перинатальных центров, гинекологических отделений многопрофильных стационаров, сотрудников и руководителей кафедр акушерства и гинекологии, слушателей всех форм непрерывного медицинского образования, аспирантов, клинических ординаторов и студентов медицинских вузов.
Купить медицинскую литературу по акушерству и гинекологии в интернет-магазине shopdon.ru
Содержание книги "Бесплодие и эндометриоз. Версии и контраверсии" - В. Е. Радзинский, М .Р. Оразов
ГЛАВА 1. Распространённость и факторы риска бесплодия, обусловленного эндометриозом
Много ли бесплодия, ассоциированного с эндометриозом?
Факторы риска эндометриоз-ассоциированного бесплодия
ГЛАВА 2. Патогенетические основы эндометриоз-ассоциированного бесплодия
Клеточный иммунитет в патогенезе эндометриоза и вызванного им бесплодия
Дендритные клетки
Естественные киллеры (ЦК-клетки)
Цитокины и хемокины в патогенезе эндометриоза.
Найдены ли маркёры?
Цитокины
Хемокины
Эндометриальная ткань в норме и при эндометриозе. Есть ли различия?
Бесплодие, обусловленное эндометриозом: полиморфизм генов
ГЛАВА 3. Клинические формы бесплодия, ассоциированного с эндометриозом
Трубно-перитонеальное бесплодие на фоне эндометриоза с позиций доказанного и дискутабельного
Овариальный эндометриоз и бесплодие: существует ли взаимосвязь?
Аденомиоз и бесплодие — логично о неоднозначном
ГЛАВА 4. Современные возможности диагностики бесплодия, связанного с эндометриозом
Аппаратная диагностика. Обзор
Сонографическое исследование
Магнитно-резонансная томография
Гистероскопия
Гистеросальпингография
ГЛАВА 5. Преодоление бесплодия при эндометриозе:
версии и контраверсии
Влияние хирургического лечения эндометриоза на фертильность
Может ли медикаментозная терапия эндометриоза улучшить фертильность?
Консервативное лечение эндометриоз-ассоциированного бесплодия
Контролируемая стимуляция овуляции и внутриматочная инсеминация
Экстракорпоральное оплодотворение пациенток с эндометриоз-ассоциированным бесплодием
ГЛАВА 6. Эндометриоз после реализации репродуктивной функции. Врачебная тактика
Гестагены
Диеногест
Дидрогестерон
Медроксипрогестерон
Норэтистерон
Левоноргестрел
Комбинированные гормональные контрацептивы
Агонисты ГнРГ
Ингибиторы ароматазы
Нестероидные противовоспалительные средства
Перспективные методы лечения эндометриоза
Ингибиторы ангиогенеза
Селективные модуляторы прогестероновых рецепторов
Селективные модуляторы эстрогеновых рецепторов
Приложение. Клинические рекомендации по эндометриозу (Минздрав России, 2016)
Купить медицинскую литературу по акушерству и гинекологии в интернет-магазине shopdon.ru












0 комментариев