Ишемическая болезнь сердца. Патологическая анатомия. Лекция для врачей
Лекция для врачей "Ишемическая болезнь сердца. Патологическая анатомия" (отрывок из книги "Патологическая анатомия по Роббинсу: учебник" - Кумар Винай)
Ишемическая болезнь сердца
Термин «ишемическая болезнь сердца» предложен для обозначения нескольких взаимосвязанных синдромов, обусловленных ишемией миокарда, то есть нарушением равновесия между потребностями миокарда и обеспечением сердца кровью (перфузия) и доставкой кислорода и питательных веществ в миокард. Большую часть энергии миокард получает за счет окислительного фосфорилирования в митохондриях кардиомиоцитов, поэтому функция сердца напрямую зависит от непрерывности потока крови, насыщенной кислородом, по коронарным артериям. Несмотря на прогресс медицины, произошедший за последнюю четверть века, различные формы ИБС остаются главной причиной смерти в Соединенных Штатах и других развитых странах. А во всем мире на ИБС ежегодно приходится 7,5 млн смертей.
ИБС более чем в 90% случаев возникает в связи со снижением кровотока в коронарных артериях в результате обструкции просвета атеросклеротическими бляшками (см. глава 10). (ИБС возникает при относительной или абсолютной недостаточности коронарного кровотока в результате закупорки просвета коронарной артерии тромбом, тромбоэмболом, атероматозными массами, спазма, а также при повышенной потребности миокарда при недостаточности коронарного кровотока. Вместе с тем в коронарных артериях имеются атеросклеротические бляшки со степенью стеноза просвета сосуда более чем на 70%. — Примеч. ред.) Таким образом, ИБС часто рассматривается как синоним болезни коронарных артерий. В большинстве случаев различные синдромы ИБС — это позднее проявление атеросклероза коронарных артерий, который развивался постепенно на протяжении нескольких десятилетий (начиная с детства или подросткового возраста). Гораздо реже ИБС развивается при повышении потребности организма в кислороде (например, при увеличении частоты сердечных сокращений или гипертензии); уменьшении объема крови (например, при гипотонии или шоке); уменьшении насыщения крови кислородом (например, при пневмонии или застойной сердечной недостаточности) или уменьшении способности эритроцитов связывать кислород (например, при анемии или отравлении угарным газом).
Клинические проявления ИБС являются следствием недостаточного кровоснабжения сердца и могут включать в себя один или более сердечных синдромов.
- Стенокардия (angina pectoris, что в буквальном смысле означает «боль в груди»): ишемия вызывает боль, но не приводит к гибели кардиомиоцитов. Стенокардия может быть стабильной (логично, что такая стенокардия развивается только при определенном уровне физической нагрузки), может быть связана со спазмом сосудов (стенокардия Принцметала, или спонтанная стенокардия) или быть нестабильной (которая возникает при незначительном напряжении или даже в покое).
- Острый инфаркт миокарда: тяжелая и продолжительная ишемия с гибелью кардиомиоцитов.
- Хроническая ИБС с последующим развитием застойной сердечной недостаточности: прогрессирующая декомпенсация сердечной деятельности развивается после острого инфаркта миокарда или после повторных мелких ишемических инфарктов и в конце концов приводит к сердечной недостаточности.
- Внезапная сердечная смерть может наступить из-за повреждений в миокарде, связанных с инфарктом миокарда, но гораздо чаще возникает в результате летальной аритмии без некроза кардиомиоцитов (см. далее в разделе «Аритмии»), развившейся в течение первых 5 ч после сердечного приступа (Примеч. ред.)
Термин «острый коронарный синдром» используется при любом из трех тяжелых проявлений ИБС — при нестабильной стенокардии, остром инфаркте миокарда и внезапной сердечной смерти.
Эпидемиология
У почти 700 000 американцев ежегодно возникает ИБС, и практически половина больных умирает от ИБС. И несмотря на эти высокие цифры, сегодня мы можем говорить о впечатляющем прогрессе в лечении ИБС по сравнению с прошлым веком. Например, после пика 1963 г. смертность от ИБС в Соединенных Штатах снизилась на 50%. Это улучшение в значительной степени можно связать с воздействием на факторы риска (отказ от вредных привычек или изменение условий, способствовавших развитию атеросклероза)! (см. глава 10), в том числе внедрение программ направленных на борьбу с курением, лечение артериальной гипертензии и сахарного диабета и использование препаратов для снижения уровня холестерина. Небольшой вклад в снижение смертности был связан с успехами диагностики] и лечения ИБС, включая использование ацетилсалициловой кислоты (Аспирина) для профилактики ИБС, контроль за аритмиями, открытие кардиологических отделений, разработка эффективного тромболизиса при инфаркте миокарда, внедрение ангиопластики и эндоваскулярного стентирования и коронарного шунтирования. Снижение показателей смертности от ИБС стало представлять проблему в связи с увеличением продолжительности жизни среди «бэби-бумеров», а также с эпидемией ожирения, охватившей США другие страны.
Патогенез
ИБС является, прежде всего, прямым следствием недостаточного коронарного кровоснабжения по сравнению с потребностями миокарда. Такое нарушение равновесия возникает при сочетании ранее существовавшей окклюзии коронарных артерий («фиксированной») атеросклеротической бляшкой и только что возникшего тромбоза и/или спазма сосудов. Атеросклеротическое сужение может возникнуть в любой коронарной артерии — в левой передней нисходящей, левой огибающей и правой коронарной артерии, при этом в одной или одновременно в нескольких. Клинически значимые атеросклеротические бляшки могут располагаться где угодно, но, как правило, формируются в непосредственной близости от устьев левой передней нисходящей и левой огибающей артерий и по всей длине правой коронарной артерии. Иногда вовлекаются ответвления коронарных артерий (например, диагональные ветви левой передней нисходящей артерии, ветви тупого края левой огибающей артерии или задняя нисходящая ветвь правой коронарной артерии).
Атеросклеротические бляшки, которые забывают менее 70% просвета коронарных сосунов, как правило, протекают без симптоматики, даже при повышенной нагрузке. А если бляшки закрывают более 70% просвета коронарного сосуда, то возникает так называемый критический стеноз и появляются клинические симптомы три повышенной нагрузке на сердце. При критическом стенозе определенные уровни нагрузки вызывают боль в груди, что свидетельствует о стабильной стенокардии больного. Стеноз с закрытием 90% просвета сосудов и более может привести к нарушению коронарного кровотока и развитию симптоматики даже в состоянии покоя и к одной из форм ИБС — нестабильной стенокардии (см. далее).
Очень важно понимать, что при медленном и постепенном закрытии просвета коронарной артерии атеросклеротической бляшкой (на протяжении многих лет) происходит перестройка (ремоделирование) других коронарных артерий, что может компенсировать кровоснабжение зоны риска; коллатеральное кровообращение в дальнейшем позволяет сохранить миокард, пока не разовьется полная окклюзия сосуда. К сожалению, при остром коронарном синдроме нет времени для формирования коллатерального кровообращения, и поэтому развивается инфаркт.
Ниже приведены состояния, которые вносят вклад в развитие атеросклероза коронарных артерий.
- Воспаление играет важную роль на всех этапах атеросклероза — с момента формирования до разрыва покрышки бляшки (см. главу 10). Атеросклероз начинается со взаимодействия эндотелиальных клеток с циркулирующими лейкоцитами, что приводит к мобилизации и активации Т-лимфоцитов и макрофагов. Эти клетки обеспечивают последующую пролиферацию гладкомышечных клеток, образование внеклеточного матрикса, формирование липидного ядра, накопление холестерина, отложение солей кальция и образование некротического детрита. На более поздних стадиях происходит дестабилизация атеросклеротической бляшки под действием металлопротеиназы, которую секретируют макрофаги, что приводит к формированию нестабильной атеросклеротической бляшки (Примеч. ред).
- Тромбоз, связанный с разрывом покрышки бляшки, часто вызывает острый коронарный синдром. Частичное закрытие просвета сосуда свежим тромбом, возникающим в месте нарушения целостности атеросклеротической бляшки, со временем может привести к нестабильной стенокардии, инфаркту или внезапной смерти. С другой стороны, даже частичное закрытие просвета сосуда тромбом значительно ухудшает кровоснабжение и может стать причиной небольшого инфаркта субэндокардиальной зоны миокарда (субэндокардиальный инфаркт). Организующиеся тромбы вырабатывают мощные активаторы пролиферации гладкомышечных клеток, что усиливает атеросклеротические поражения. Пристеночный тромб коронарной артерии может стать эмболом. И действительно, при аутопсии можно обнаружить небольшие эмболы в дистальных внутриорганных сосудах миокарда (вместе с микроинфарктами) у больных нестабильной стенокардией. При самом худшем сценарии полная обструкция просвета сосуда тромбом (при разрыве атеросклеротической бляшки) приводит к массивному инфаркту миокарда.
- Спазм сосудов становится причиной значительного сужения просвета. Более того, за счет местного механического сдавливания спазм сосудов может привести к разрыву бляшки. Спазм сосудов возникает из-за стимуляции гладкомышечных клеток стенки артерии в зоне атеросклеротической бляшки:
- циркулирующими адренергическими агонистами;
- локально высвобождающимся содержимым тромбоцитов;
- нарушенным равновесием между расслабляющими факторами эндотелиального происхождения (оксид азота) и сокращающими факторами (эндотелии) в связи с эндотелиальной дисфункцией;
- медиаторами, высвобождаемыми периваскулярными клетками воспаления.
Нестабильная бляшка
Развитие ишемии миокарда зависит не только от степени и выраженности атеросклеротических процессов, но и от динамических изменений в структуре бляшек коронарных сосудов. У большинства больных нестабильная стенокардия, инфаркт миокарда и внезапная сердечная смерть возникают из-за дестабилизации бляшки и последующего тромбоза — отсюда и происхождение термина «острый коронарный синдром» (рис. 11.7).
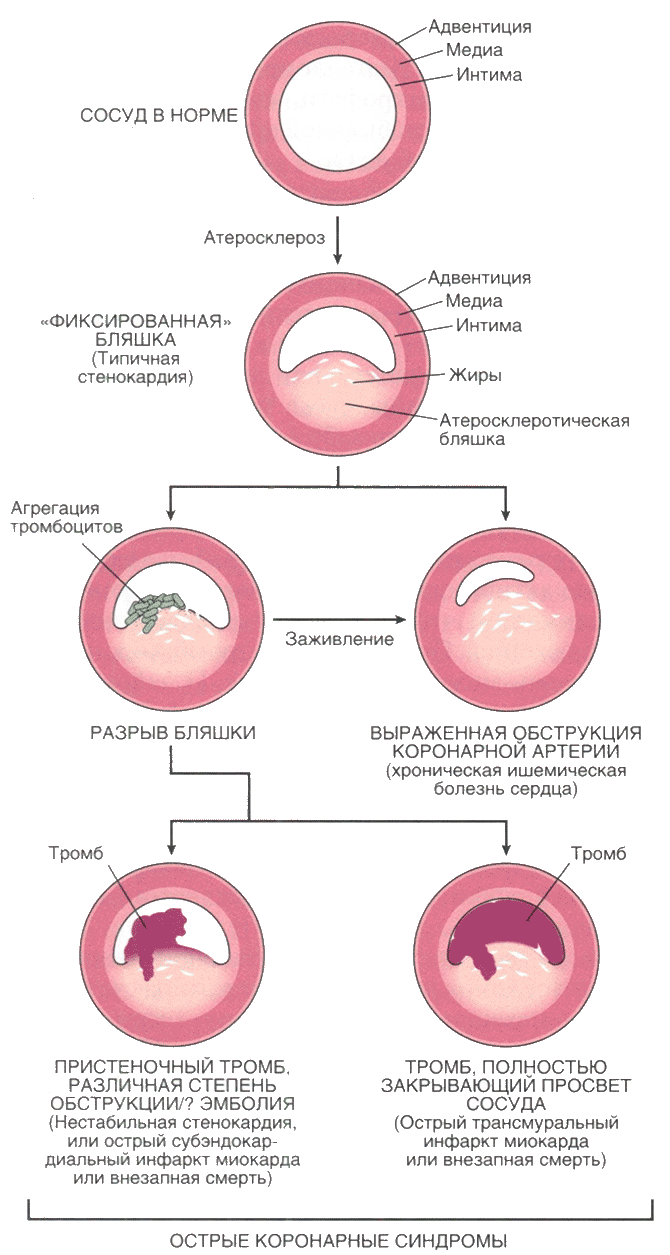
Рис. 11.7. Схема последовательного прогрессивного поражения коронарных артерий и развития различных вариантов острого коронарного синдрома. (С изменениями из: Schoen F.J. Interventional and Surgical Cardiovascular Pathology: Clinical Correlations and Basic Principles. Philadelphia: W.B. Saunders, 1989. P. 63)
Все начинается с внезапного нарушения целостности (от поверхностных дефектов до разрыва) покрышки атеросклеротической бляшки, частично закрывающей просвет сосуда. Этот процесс протекает с вовлечением нескольких механизмов повреждения: разрыв, трещины или изъязвление покрышки бляшки, что сопровождается «обнажением» высокотромбогенных компонентов или субэндотелиальной базальной мембраны и приводит к тромбозу. Кроме того, кровоизлияние в ядро бляшки способствует увеличению ее объема и стремительному уменьшению просвета сосуда.
Факторы, вызывающие дестабилизацию бляшки, включают повреждение эндотелия и апоптоз, возможно, в сочетании с воспалением и токсическим воздействием. С другой стороны, при остром повреждении бляшки также вовлекаются факторы, которые воздействуют на ее устойчивость к механическому повреждению. Они включают сочетание внутренних факторов, в том числе структуру бляшки (см. главу 10), с внешними факторами, такими как давление крови и реактивность тромбоцитов.
• Бляшки с крупным атеросклеротическим ядром или тонкой фиброзной покрышкой склонны к разрыву и поэтому относятся к самым уязвимым. Трещины часто возникают в зоне соединения фиброзной покрышки с прилегающим «нормальным» участком артерии, находящимся за пределами бляшки, где механическое напряжение выше, а фиброзная покрышка потоньше. Фиброзная покрышка постоянно подвергается изменениям (ремоделированию); хрупкое равновесие между синтезом коллагена и его разрушением определяет механическую прочность покрышки и стабильность бляшки. Коллаген образуется гладкомышечными клетками и разрушается под действием металлопротеаз, вырабатываемых макрофагами. Следовательно, атеросклеротические бляшки с единичными гладкомышечными клетками или с большим числом клеток воспаления наиболее подвержены разрыву. Интересно, что статины (ингибиторы гидрокси-метил-глутарил-СоА-редуктазы, ключевой фермент, участвующий в синтезе холестерина) могут дать дополнительное преимущество при лечении болезней коронарных артерий и ИБС, поскольку снижают активность воспалительных процессов в атеросклеротических бляшках и повышают стабильность бляшек, а не просто снижают уровень холестерина.
• Важное влияние внешних факторов на атеросклеротическую бляшку. Адренергическая стимуляция вызывает повышение артериального давления и спазм сосудов, тем самым оказывая физическое воздействие на бляшку. И действительно, влияние адренергического всплеска (процесс пробуждения и вставание с кровати) можно связать с высокой частотой острых инфарктов миокарда, которые возникают во временном промежутке с 6 ч утра и до 12 ч дня. Выраженный эмоциональный стресс также вызывает адренергическую стимуляцию, что объясняет зависимость между стихийными бедствиями (землетрясения и наводнения) и волной инфарктов миокарда у предрасположенных лиц.
В большинстве случаев стеноз сосудов, который наблюдается у больных, перенесших инфаркт миокарда, не был критическим. Как отмечалось выше, симптомы стенокардии, как правило, возникают при стабильных бляшках, которые закрывают просвет более чем на 70%. Морфологические и клинические исследования показывают, что 2/3 разорванных бляшек находили в сосудах со стенозом 50% и меньше; и в 85% случаев отмечалась окклюзия просвета 70% или меньше. Таким образом, можно сделать печальный вывод, что большая часть взрослого населения без каких-либо симптомов подвергается высокому риску развития смертельного сердечного приступа. И в настоящее время невозможно предсказать, когда возникнет разрыв бляшки у любого человека.
Разрыв покрышки атеросклеротической бляшки с последующим тромбозом без окклюзии коронарной артерии встречается довольно часто, возникает неоднократно и нередко протекает без осложнений в бляшке. Заживление таких субклинических повреждений в атеросклеротической бляшке с сопутствующим тромбозом становится важным механизмом прогрессивного увеличения бляшки (см. рис. 11.7).
Стенокардия
Стенокардия определяется как приступ боли в груди, связанный с проходящей, обратимой ишемией миокарда. Боль, возможно, является следствием вызванного ишемией высвобождения аденозина, брадикинина и других молекул, которые стимулируют вегетативные афферентные волокна. Выделяют три варианта стенокардии.
- Типичная, или стабильная, стенокардия — предсказуемый приступ боли в груди, связанный с определенным уровнем стресса или увеличением нагрузки на сердце (например, тахикардия). Классическим описанием боли является чувство «сдавливания» или сжатия за грудиной с иррадиацией вниз — в левую руку или в левую часть челюсти (отраженная боль). Боль обычно исчезает в покое (при уменьшении нагрузки на сердце) или после приема препаратов, например нитроглицерина, которые расширяют сосуды и увеличивают коронарный кровоток.
- Стенокардия Принцметала, или спонтанная (вариантная) стенокардия, возникает в покое и связана со спазмом коронарной артерии. Хотя такие спазмы, как правило, возникают в сосудах с атеросклеротическими бляшками, но даже в неизмененных сосудах может возникать спазм. Больные со стенокардией Принцметала обычно хорошо отвечают на сосудорасширяющие препараты, такие как нитроглицерин и блокаторы кальциевых каналов.
- Нестабильная стенокардия (или прогрессирующая стенокардия) характеризуется нарастающей болью, которая возникает при незначительной нагрузке или в покое. Нестабильная стенокардия связана с нарушением целостности бляшки и последующим тромбозом, дистальной тромбоэмболией (закрытие просвета мелких ветвей) и/или спазмом сосудов. Кроме того, нестабильная стенокардия нередко служит предвестником инфаркта миокарда в результате полной окклюзии просвета сосудов.
Инфаркт миокарда
Инфаркт миокарда обычно называют сердечным приступом, он проявляется некрозом сердечной мышцы в результате ишемии. Основная причина ИБС — атеросклероз коронарных артерий сердца. Хотя инфаркт миокарда может возникнуть в любом возрасте, частота встречаемости повышается по мере старения и увеличения факторов риска атеросклероза (см. главу 10). Тем не менее примерно 10% всех инфарктов миокарда возникает в возрастной группе до 40 лет и 45% — до 65 лет. Инфаркт с одинаковой частотой встречается у представителей белой и черной расы. Риск инфаркта миокарда у мужчин значительно выше по сравнению с женщинами, хотя различия между полами стирается в старшей возрастной группе. Похоже, что репродуктивный период защищает женщин от этого заболевания. Однако в менопаузе, которая сопровождается снижением уровня эстрогенов, происходит обострение ИБС, которая становится самой частой причиной смерти пожилых женщин.
Патогенез
Подавляющее большинство инфарктов миокарда вызвано острым тромбозом коронарных артерий (см. рис. 11.7). В большинстве случаев нарушается целостность (разрыв или эрозия) покрышки атеросклеротической бляшки, что становится «плацдармом» для образования тромбов, окклюзии сосуда с последующим развитием трансмурального инфаркта миокарда, соответствующего бассейну пораженного сосуда. Однако в 10% случаев всех инфарктов трансмуральный инфаркт возникает в отсутствие окклюзии; такие инфаркты связывают со спазмом коронарных артерий или эмболией от пристеночных тромбов (например, при фибрилляции предсердий) и вегетаций клапана. Но иногда при инфаркте миокарда (субэндокардиальном) тромбы и эмболы не находят. В таких случаях выраженный диффузный атеросклероз
коронарных артерий становится причиной маргинального кровоснабжения сердца; длительный период сердце работает с повышенной нагрузкой (при тахикардии или артериальной гипертензии), что может привести к ишемическому некрозу миокарда в участках, которые питают дистальные веточки коронарных артерий. Помимо атеросклероза и тромбоэмболических состояний ишемия миокарда может возникнуть при нарушении кровообращения в мелких артериолах миокарда, например, при васкулитах, отложении амилоида и серповидноклеточной анемии.
Окклюзия коронарных артерий
Типичный инфаркт миокарда возникает при следующей последовательности событий.
- В атеросклеротической бляшке внезапно нарушается целостность покрышки в результате повреждения эндотелия, кровоизлияния внутрь бляшки или действия механических сил; происходит обнажение коллагеновых волокон, расположенных под эндотелием; некротический детрит бляшки попадает в кровь.
- Тромбоциты прилипают (адгезия), агрегируются и активируются, высвобождая тромбоксан А2, АДФ и серотонин, что вызывает дальнейшую агрегацию тромбоцитов и спазм сосудов (см. главу 4).
- Активация процесса свертывания под действием тканевого фактора и других механизмов, которые усиливают рост тромба.
- В течение нескольких минут тромб может полностью закрыть просвет коронарных артерий. Доказательством такого сценария служат результаты аутопсий погибших от острого инфаркта миокарда, а также исследований, представивших высокую частоту окклюзии просвета сосудов на ранних стадиях инфаркта. При ангиографии, проведенной в первые 4 ч инфаркта, в 90% случаев выявляется тромбоз коронарных артерий. Однако, когда ангиография проводилась через 12—24 ч после возникновения симптоматики, тромбоз обнаруживался только у 60% пациентов, даже без терапевтического вмешательства. Это значит, что в некоторых случаях окклюзия может разрешаться спонтанно благодаря растворению тромба или в связи с расслаблением сосуда после спазма. Понимание закономерностей развития типичного инфаркта миокарда позволяет проводить патогенетическое лечение: ранний тромболизис и/или ангиопластика становятся залогом успешного лечения, направленного на ограничение площади некроза в миокарде.
Ответная реакция миокарда на ишемию
Ухудшение кровоснабжения миокарда приводит к глубоким функциональным, биохимическим и морфологическим последствиям. В течение нескольких секунд после обструкции сосудов нарушается аэробный гликолиз, что приводит к снижению уровня АТФ и накоплению побочных продуктов обмена глюкозы (например, молочной кислоты) в кардиомиоцитах. Нарушения функции кардиомиоцитов проявляются потерей сократительной способности, которая возникает практически через одну минуту от начала ишемии. Ультраструктурные изменения (которые включают расслабление миофибрилл, истощение запасов гликогена, отек цитоплазмы и митохондрий) также возникают достаточно быстро. Такие ранние изменения в целом носят обратимый характер. И только выраженная ишемия, которая продолжается не менее 20—40 мин, вызывает необратимые повреждения и коагуляционный некроз кардиомиоцитов (см. главу 2). При более длительной ишемии возникают повреждения сосудов, что приводит к тромбозу микроциркуляторного русла.
Таким образом, восстановление кровоснабжения в миокарде до появления необратимых повреждений кардиомиоцитов сохраняет жизнеспособность клеток; и это основная причина ранней диагностики инфаркта миокарда, проведения тромболизиса или ангиопластики. Тем не менее, как будет обсуждаться ниже, неблагоприятные последствия могут быть связаны также и с реперфузионными повреждениями. Но даже при своевременном восстановлении кровоснабжения после ишемии миокард еще в течение нескольких дней практически не функционирует. Такие изменения связаны со стойким нарушением биохимических процессов в клетках, что приводит к снижению сократительной функции («оглушенный» миокард). «Оглушенный», или «уснувший», миокард является достаточно серьезным состоянием и может вызвать сердечную недостаточность, носящую кратковременный (обратимый) характер.
Ишемия миокарда вносит вклад в развитие аритмий, что, вероятнее всего, связано с электрической нестабильностью той области сердца, которая подверглась ишемии. Хотя массивные повреждения миокарда могут привести к смерти, тем не менее внезапная сердечная смерть при ишемии миокарда чаще всего (в 80—90%) развивается из-за фибрилляции желудочков, что связано с электрической нестабильностью миокарда.
Необратимые ишемические изменения в кардиомиоцитах вначале возникают в субэндокардиальной зоне (рис. 11.8). Как было отмечено ранее, эта область особенно чувствительна к ишемии, потому что получает кровь из коронарных артерий в самую последнюю очередь в условиях ухудшения кровоснабжения; а еще потому, что эта зона испытывает относительно высокое пристеночное давление, которое препятствует притоку крови. При длительной ишемии волна гибели клеток распространяется и на другие зоны миокарда в связи с нарастающим тканевым отеком и высвобождением АФК и медиаторов воспаления. Инфаркт, как правило, достигает своего пика в течение 3—6 ч. И без лечения в зону инфаркта вовлекается вся толща миокарда (трансмуральный инфаркт). Только терапевтическое вмешательство в этот критический период может уменьшить размеры инфаркта микарда в «зоне риска».
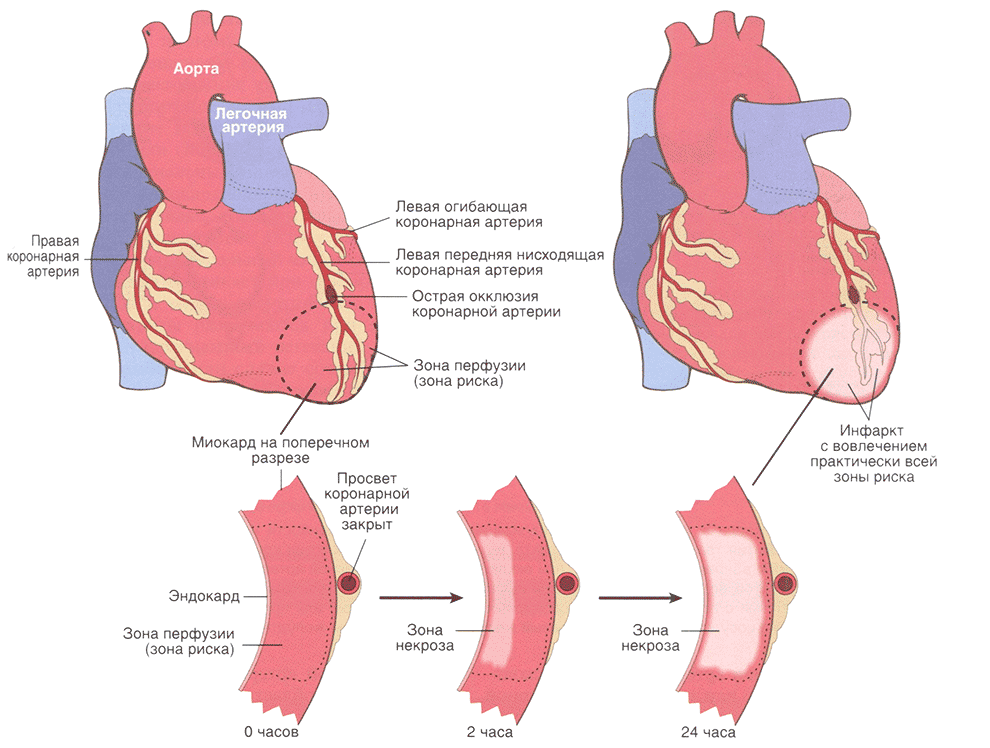
Рис. 11.8. Прогрессирование некроза миокарда при окклюзии коронарной артерии. Сегмент миокарда в толще стенки желудочка из-за расположения в бассейне сосуда, подвергшегося окклюзии, представляет зону риска (отмечено пунктиром). Некроз начинается с субэндокардиальной области в центре участка ишемии, и со временем площадь некроза увеличивается и захватывает всю толщу стенки. Обратите внимание, что узкая полоска миокарда, расположенная непосредственно под эндокардом, остается сохранной и не подвергается некрозу, потому что путем диффузии осуществляется поступление кислорода из желудочка
Признаки инфаркта миокарда
Локализация инфаркта, его размеры и морфологические проявления зависят от многих факторов:
- размера и степени вовлеченности сосуда в патологический процесс (рис. 11.9);
- темпов развития окклюзии и ее продолжительность;
- метаболических потребностей миокарда (зависящих от уровня артериального давления и частоты сердечных сокращений);
- степени коллатерального кровообращения.
Острое закрытие проксимального сегмента левой передней нисходящей артерии является причиной 40—50% всех инфарктов миокарда и, как правило, приводит к инфаркту передней стенки левого желудочка, передних двух третей межжелудочковой перегородки и большей части верхушки сердца; при дистальной окклюзии этого же сосуда инфаркт развивается только на верхушке сердца. Аналогично острая окклюзия проксимального участка левой огибающей артерии (составляет 15—20% всех инфарктов миокарда) становится причиной некроза боковой стенки левого желудочка, а окклюзия проксимального сегмента правой коронарной артерии (30—40% всех инфарктов миокарда) вовлекает большую часть правого желудочка. Острую обструкцию левой коронарной артерии образно называют «создатель вдов» из- за высокой частоты смертельных исходов вследствие вовлечения обширных участков миокарда. (Нисходящую межжелудочковую ветвь левой коронарной артерии называют «артерия жизни и смерти». — Примеч. ред.)
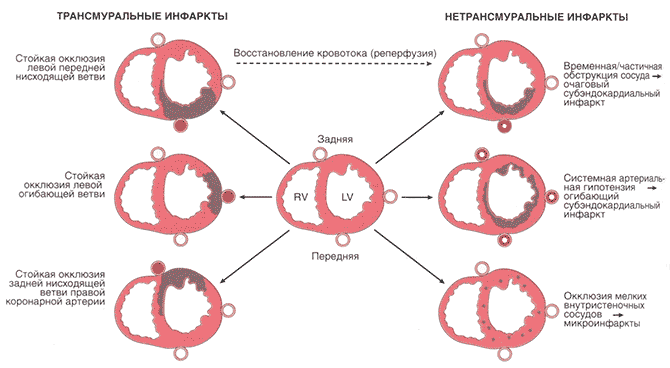
Рис. 11.9. Инфаркт миокарда в зависимости от локализации и степени выраженности недостаточности кровоснабжения. Слева — вариант развития трансмурального инфаркта, возникающего при окклюзии крупной коронарной артерии. Правый желудочек вовлекается в ишемический процесс при окклюзии правой коронарной артерии (на рисунке не показано). Справа — варианты инфарктов, возникших при частичной или временной окклюзии (наверху), на фоне системной артериальной гипотензии при сочетании с поражением трех коронарных артерий (в центре) или при окклюзии мелких внутриорганных (интрамиокардиальных) сосудов (внизу). RV — правый желудочек; LV — левый желудочек
Задняя треть межжелудочковой перегородки и задняя стенка левого желудочка получают кровь из задней нисходящей артерии. Задняя нисходящая артерия отходит или от правой коронарной артерии (90%), или от левой огибающей артерии (10%). В зависимости от того, какая коронарная артерия (правая коронарная артерия или левая огибающая артерия) продолжается в заднюю нисходящую артерию и кровоснабжает заднюю треть перегородки, та считается доминирующим сосудом. Так, при праводоминирующем типе коронарной системы окклюзия правой коронарной артерии может привести к ишемии правого желудочка, а при леводоминирующем типе коронарной системы окклюзия левой коронарной артерии, как правило, вовлекает в патологический процесс весь левый желудочек и перегородку.
Окклюзия может возникать в ветвях коронарных артерий, например диагональных ветвях, отходящих от передней нисходящей артерии, или маргинальных ветвях левой огибающей артерии. Интересный факт, что атеросклероз — это в первую очередь патология субэпикардиальных сосудов; выраженный атеросклероз и тромбоз внутриорганных интрамиокардиальных ветвей коронарных артерий встречается крайне редко — хотя возможны васкулит, спазм или окклюзия эмболами.
Несмотря на то что все три крупные коронарные артерии в анатомическом плане зрения относятся к конечным артериям, тем не менее они связаны между собой многочисленными анастомозами (коллатеральное кровообращение). Анастамозы в условиях нормы закрыты, но сужение просвета одной артерии обеспечивает поступление крови из области более высокого давления в область низкого давления через коллатеральные каналы. И таким способом постепенно расширяющаяся коллатеральная сосудистая сеть обеспечивает адекватное питание тех областей миокарда, которые находятся в бассейне кровоснабжения окклюзированного субэпикардиального сосуда. В зависимости от размера вовлеченного сосуда и степени выраженности коллатерального кровообращения инфаркт миокарда может протекать по следующим сценариям.
- Трансмуральный инфаркт миокарда вовлекает всю толщу стенки желудочка и обусловлен окклюзией субэпикардиального сосуда при сочетании хронического атеросклероза и острого тромбоза. При трансмуральном инфаркте миокарда обычно на ЭКГ происходит подъем сегмента ST, проявляется отрицательный зубец Q, уменьшается амплитуда зубца R. Такие инфаркты называют инфарктами миокарда с подъемом сегмента ST. (Они также называются Q-позитииными инфарктами. — Примеч. ред.)
- Субэндокардиальный инфаркт миокарда охватывает внутреннюю треть миокарда. Такие инфаркты, как правило, не проявляются подъемом сегмента ST или волной зубца Q на ЭКГ (так называемые инфаркты миокарда без подъема сегмента ST), хотя при них может быть снижение сегмента ST или аномалия зубца Т. Как уже отмечалось ранее, субэндокардиальная область наиболее уязвима к снижению кровоснабжения и гипоксии. И поэтому в условиях острого нарушения коронарного кровообращения даже временное уменьшение поступления кислорода (при гипотонии, анемии или пневмонии) или усиленное потребление кислорода (при тахикардии или гипертензии) может привести к субэндокардиальным ишемическим повреждениям. Субэндокардиальный инфаркт может развиться в случаях, когда вызвавший окклюзию тромб подвергается лизису раньше, чем развивается трансмуральный инфаркт.
- Микроинфаркт возникает при окклюзии мелких сосудов и может отсутствовать на ЭКГ. Микроинфаркты развиваются при васкулите, эмболии фрагментами вегетаций, пристеночном тромбозе или спазме сосудов в связи с повышением уровня катехоламинов из-за воздействия эндогенных факторов (например, феохромоцитома или острый стресс) или экзогенных факторов (например, кокаин).
Морфология
Практически при всех трансмуральных инфарктах (50% или более стенки желудочка) в процесс вовлекается стенка левого желудочка и/или межжелудочковая перегородка. Примерно в 15-30% всех инфарктов задней стенки или заднеперегородочной области процесс распространяется на правый желудочек. Изолированные инфаркты правого желудочка встречаются только в 1-3% случаев. Даже при трансмуральных инфарктах сохраняется узкая зона (около 0,1 мм) жизнеспособного субэндокардиального миокарда благодаря поступлению питательных веществ и кислорода непосредственно из просвета желудочка.
Макроскопические и микроскопические проявления инфаркта миокарда зависят от давности повреждения. Поврежденный миокард при прогрессировании процесса проходит через целую серию характерных морфологических изменений — от коагуляционного некроза, острого воспаления, затем хронического воспаления до фиброза (табл. 11.2). В исходе некроза миокарда всегда формируется рубец без каких-либо других проявлений регенерации. Исследования, которые посвящены изучению тканевых стволовых клеток и возможности использования их для восстановления функции миокарда, проводятся, но до сих пор не принесли никаких результатов.
Макроскопическая и микроскопическая диагностика острого инфаркта миокарда достаточно сложная, особенно если смерть наступает в течение нескольких часов. Если инфаркт миокарда возник меньше чем 12 ч назад, то при макроскопическом исследовании его не видно. Тем не менее инфаркт, возникший более 3 ч назад, можно выявить при использовании специальных красителей, например трифенилтетразолин хлорида, который является субстратом лактатдегидрогеназы.
Уровень этого фермента резко снижается в области ишемического некроза (он высвобождается из поврежденных клеток), поэтому область инфаркта не окрашивается (бледная), в то время как старые рубцы выглядят белыми и блестящими (рис. 11.10). (Другая проба проводится с теллуритом калия. При этом окись теллура черного цвета образуется только в сохранноммиокарде. Зона ишемии не окрашивается. — Примеч. ред.) Уже через 12-24 ч инфаркт миокарда можно увидеть при макроскопическом исследовании: зона инфаркта имеет красновато-синюшный цвет, что связано с застоем крови. И после 12-24 ч зона инфаркта становится все более и более очерченной, имеет вид мягкого участка желто-коричневого цвета. На 10-14-й день зона инфаркта окружена «венчиком» из грануляционной ткани, включающей полнокровные сосуды. В дальнейшем зона инфаркта превращается в рубцовую ткань.
Таблица 11.2. Динамика морфологических изменений в инфаркте миокарда
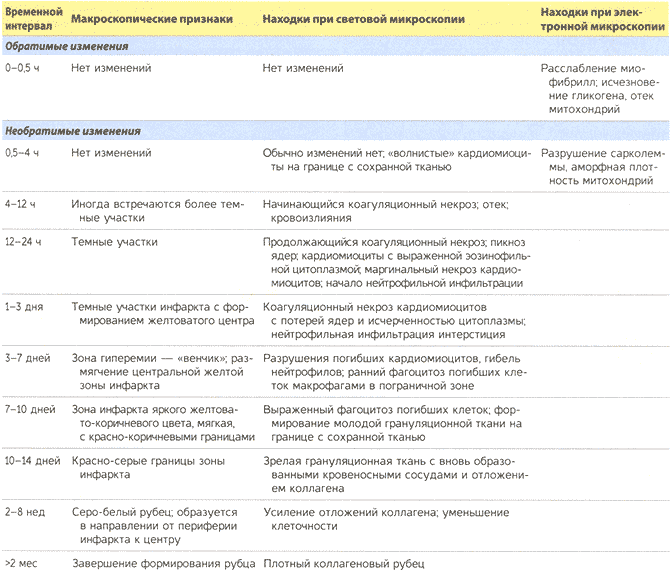
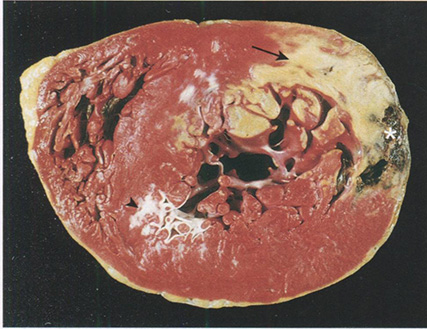
Рис. 11.10. Острый инфаркт миокарда заднебоковой стенки левого желудочка. Зоны некроза (стрелка) не окрашиваются трифенилтетразол хлоридом, что связано с исчезновением фермента после гибели клеток. Обратите внимание на рубец на передней стенке (стрелка слева), что указывает на ранее перенесенный инфаркт. Справа звездочкой отмечено кровоизлияние, связанное с разрывом стенки желудочка в зоне инфаркта; разрыв стенки левого желудочка стал причиной смерти больного (заднебоковая стенка левого желудочка находится в верхней части рисунка)
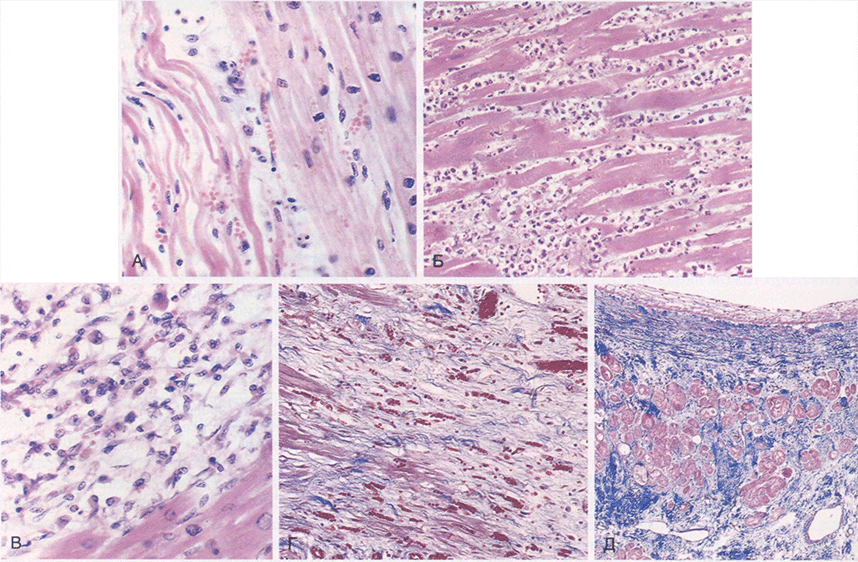
Рис. 11.11. Гистологические признаки инфаркта миокарда и его заживления: А — однодневный инфаркт: виден участок коагуляционного некроза и «волнистые» кардиомиоциты рядом с неизмененными кардиомиоцитами (справа). Некротизированные клетки разделены зонами отека; Б — выраженная нейтрофильная инфильтрация в очаге 2-3-дневного инфаркта; В — некротизированные кардиомиоциты отсутствуют благодаря фагоцитозу с участием макрофагов (возраст инфаркта — от 7 до 10 дней); Г — грануляционная ткань представлена рыхлой соединительной тканью и множеством капилляров; Д — заживление зоны инфаркта за счет образования плотного коллагенового рубца. Видны единичные сохранившиеся кардиомиоциты. Г и Д, окраска трихромом по Массону — коллаген окрашен в синий цвет
Гистологические изменения зоны инфаркта отличаются определенной последовательностью (табл. 11.2, рис. 11.11). Характерные признаки коагуляционного некроза (см. главу 2) можно видеть в зоне инфаркта через 4-12 ч. Кроме того, на периферии инфаркта появляются «волнистые» кардиомиоциты; они образуются при перерастяжении и деформации несократившихся погибших кардиомиоцитов. Сублетальная ишемия может также вызвать внутриклеточную вакуолизацию кардиомиоцитов. Такие клетки остаются жизнеспособными, но теряют способность сокращаться.
В некротизированном миокарде развивается острое воспаление (наиболее выражено на 1-3-й день инфаркта миокарда); воспаление сопровождается макрофагальной реакцией, благодаря которой удаляются погибшие кардиомиоциты и фрагменты нейтрофилов (наиболее выражена на 5-10-й день инфаркта миокарда). Зона инфаркта постепенно замещается грануляционной тканью (наиболее выражена через 1-2 нед инфаркта миокарда), которая формирует структурную основу для образования рубца. В большинстве случаев в конце 6-й недели образуется рубец, но степень заживления зависит от размера инфаркта. В заживлении участвуют клетки воспаления и образуются новые сосуды за счет пограничной с зоной инфаркта ткани. То есть заживление инфаркта миокарда происходит в направлении от периферии к центру, и в обширных инфарктах невозможно полное заживление в отличие от маленьких инфарктов. Более того, недоедание, слабая степень васкуляризации и экзогенные противовоспалительные стероиды препятствуют формированию рубцов при инфаркте (см. главу 3). После того как инфаркт зажил, определить возраст инфаркта невозможно: возник ли инфаркт 8 нед тому на-зад или 10 лет назад — независимо от возраста рубцы выглядят одинаково.
Вы читали отрывок из книги "Патологическая анатомия по Роббинсу: учебник"
Книга "Патологическая анатомия по Роббинсу: учебник"
Автор: Кумар В., Аббас А. К., Астер Д. С.

Настоящее издание отражает инновационные тенденции развития современной медицины и включает основы молекулярной патологии физиологических процессов и болезней. Материал дается интегративно на генетическом, молекулярном, субклеточном, клеточном и органном уровнях. Книга изобилует таблицами и иллюстрациями высочайшего качества, представленными как макро- и микропрепаратами, так и цветными схемами, выполненными в ЗБ-формате, что значительно облегчает обучение. Учебник рекомендован студентам медицинских вузов 2—3-го курса, ординаторам и врачам-патологоанатомам, а также медицинским работникам общего профиля.
Учебник патологии Роббинса является закономерным продолжением предыдущих изданий и раскрывает инновационные тенденции развития современной медицины. В то же время он имеет и свои особенности. Во-первых, в книге представлена «клеточная патология Вирхова» с учетом достижений последних лет в молекулярной, клеточной биологии и патологической анатомии.
Продемонстрировано строение и функционирование клеток в нормальных и патологических условиях. Во-вторых, обновлены и более глубоко представлены в разных главах книги данные, являющиеся предметом раздела «Молекулярная патология». Механизмы развития патологических процессов разбираются с учетом генетических, эпигенетических, молекулярных и метаболических перестроек. Таким образом, изложение патологических процессов и болезней дается интегративно на молекулярном, субклеточном, клеточном и органном уровнях. При этом в каждом разделе приводится клиника процесса. В-третьих, описываются недавно открытые органеллы клеток (инфламмасомы, микровезикулы, экзосомы и др.), типы клеточной гибели, механизмы повреждения клеток, воспаления, опухолевого роста, обсуждается молекулярный профиль и сигнатура наиболее значимых опухолей, лежащие в основе их таргетной терапии. В-четвертых, следует отметить обилие таблиц и высочайший уровень иллюстративного материала, представленного как макро- и микропрепаратами, так и цветными схемами, выполненными в 3D-формате. В то же время в учебнике относительно кратко раскрыты классическая морфология, для изучения которой авторы отсылают читателя к дополнительной литературе.
Десятое издание патологии Роббинса может быть рекомендовано для изучения патологической анатомии студентам-медикам, ординаторам и врачам, стремящимся знать и понимать материальный субстрат и молекулярные механизмы патологических процессов и болезней.
Содержание книги "Патологическая анатомия по Роббинсу: учебник"
Глава 1. Клетка как основа здоровья и болезни
Глава 2. Повреждение клетки, смерть клетки и адаптация
Глава 3. Воспаление и репарация
Глава 4. Нарушения кровообращения, тромбоз и шок
Глава 5. Болезни иммунной системы
Глава 6. Опухоли
Глава 7. Генетические и детские заболевания
Глава 8. Болезни, вызванные неблагоприятными факторами окружающей среды и нарушением питания
Глава 9. Патология инфекционных болезней, общие сведения
Глава 10. Кровеносные сосуды
Глава 11. Сердце
Глава 12. Гемопоэтическая и лимфоидная системы
Глава 13. Легкие
Глава 14. Почки и мочевыводящие пути
Глава 15. Полость рта и желудочно-кишечный тракт
Глава 16. Печень и желчный пузырь
Глава 17. Поджелудочная железа
Глава 18. Мужская половая система и нижние мочевые пути
Глава 19. Женская половая система и молочные железы
Глава 20. Эндокринная система
Глава 21. Болезни костей, суставов, опухоли мягких тканей
Глава 22. Периферическая нервная система и мышечная система
Глава 23. Центральная нервная система
Глава 24. Кожа











































































0 комментариев