Концепция комплексного УЗИ обследования брахиоцефальных сосудов (артерий и вен). Лекция для врачей
Дополнительный материал к лекции
Несмотря на достижения современной медицины за период 1998-2002 гг., заболеваемость системы кровообращения в России увеличилась на 22,9%. Показатель смертности от сосудистых заболеваний мозга в России остается одним из самых высоких в мире. К 2000 г. он увеличился с 279,3 (в 1998 г.) до 318,8, а в 2002 г. до 339,1 (+16,8%) случаев на 100 тыс. населения.
К сожалению, причины церебральных катастроф и соответственно все меры их профилактики основывают на доминирующей до настоящего времени эмболической и гемодинамической теориях нарушения мозгового кровообращения, учитывающих только артериальную патологию и в первую очередь стенозирующие поражения брахиоцефальных артерий, артериальную гипертонию, материальную и/или воздушную эмболию. При этом, по данным Н. В. Верещагина (1996 г.) 40% ишемических инсультов относят все же к неопределенному подтипу.
Естественное течение сосудистых заболеваний мозга происходит в двух основных направлениях: развитие инсультов и хроническое прогрессирующее течение с возможным исходом в сосудистую деменцию. По данным ВОЗ (1997 г.), цереброваскулярными болезнями в мире страдают 9 млн человек (0,15% населения), а деменцией - 29 млн (0,5% населения). Если социальные, экономические и медицинские последствия инсультов хорошо изучены, то масштабы этих последствий при сосудистой деменции точно не установлены. Есть основания полагать, что они весьма значительны, особенно если принять во внимание их влияние на интеллектуальный потенциал нации. Социальная значимость хронической сосудистой мозговой недостаточности (дисциркуляторной энцефалопатии) возрастает в связи с отчетливой тенденцией к старению населения. Из населения Земного шара 7% составляют лица 65 лет и старше (среди них 16% - старше 80 лет). Согласно прогнозам в ближайшие 25 лет ожидается увеличение этого контингента на 82%, при увеличении численности трудоспособного населения (20-64 года) всего лишь на 46%.
Как показал анализ исследований, проведенных в Центре сердечно-сосудистой хирургии им. А. Н. Бакулева РАМН, при оценке нарушений мозгового кровообращения необходимо оценивать не только артериальную, но и венозную сосудистую систему. Оценивать комплексно, поскольку раздельная оценка по полушариям, по бассейнам, по системам и вне связи с центральной гемодинамикой- нефизиологична.
Нарушения венозного оттока, а именно венозно-артериальный дисбаланс, вызывают повышение внутричерепного давления, «вазоспазм» интракраниальных артерий, повышение периферического сопротивления, вторичное снижение артериального притока по сонным и позвоночным артериям и нарушение перфузии мозга. При нарушениях венозного оттока может наблюдаться не только цефалгический синдром, но и ишемия мозга с развитием лейкоареоза, очагов как в каротидном, так и в вертебробазилярном бассейнах, расширение боковых желудочков и кортикальных борозд, церебральная атрофия. Длительно существующий дисбаланс венозного и артериального церебрального кровообращения вызывает развитие артериосклероза, а также вторичное снижение артериального притока по сонным и позвоночным артериям (рис. 5.1).
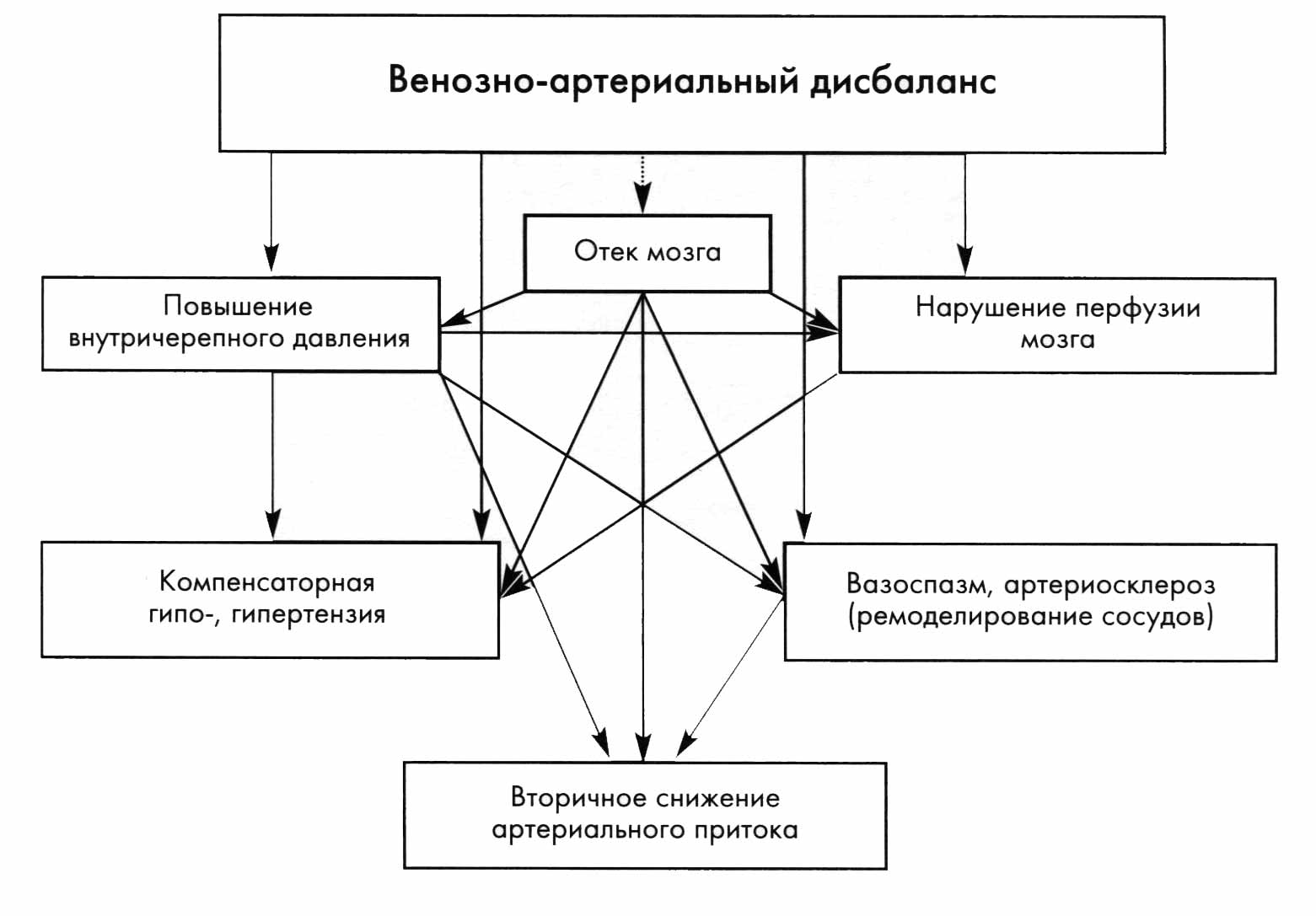
Рис. 5.1. Патологические последствия венозно-артериального дисбаланса.
Кровоток в сосудах головного мозга в норме определяется церебральным перфузионным давлением (ЦПД) и цереброваскулярной резистентностью, которая зависит от вязкости крови и размера внутричерепных артерий. ЦПД представляет собой разность между артериальным давлением, приносящим кровь к мозгу, и венозным давлением, благодаря которому кровь оттекает от мозга. Среднее значение ЦПД равно среднему значению системного артериального давления в сосудах основания мозга (в положении лежа), при котором оно примерно равно диастолическому давлению (около 80 мм рт. ст.) в сумме с одной третью пульсового давления минус значение внутричерепного венозного давления (в норме около 10 мм рт. ст.), то есть 80-85 мм рт. ст.
Перфузионное давление, а значит и перфузия мозга, могут снижаться не только при снижении артериального притока, но и при повышении венозного давления. Схема (рис. 5.2) помогает понять, что для нормальной перфузии головного мозга (то есть для поддержания перфузионного давления в 80-85 мм рт. ст.) при повышении венозного давления необходимо повышение артериального давления (так называемая компенсаторная артериальная гипертензия).
Под внутричерепным давлением понимают суммарную величину, в формировании которой участвуют вещество и оболочки мозга, ликвор, внутриклеточная и внеклеточная жидкость, артериальная и венозная системы крови. В основе повышения внутричерепного давления лежат следующие факторы: окклюзия ликворопроводящих путей и связанное с этим расширение желудочковой системы, увеличение продукции и ухудшение резорбции ликвора, изменение объема внутричерепного содержимого, отек мозга, нарушение церебральной гемодинамики, в частности нарушения венозного оттока.
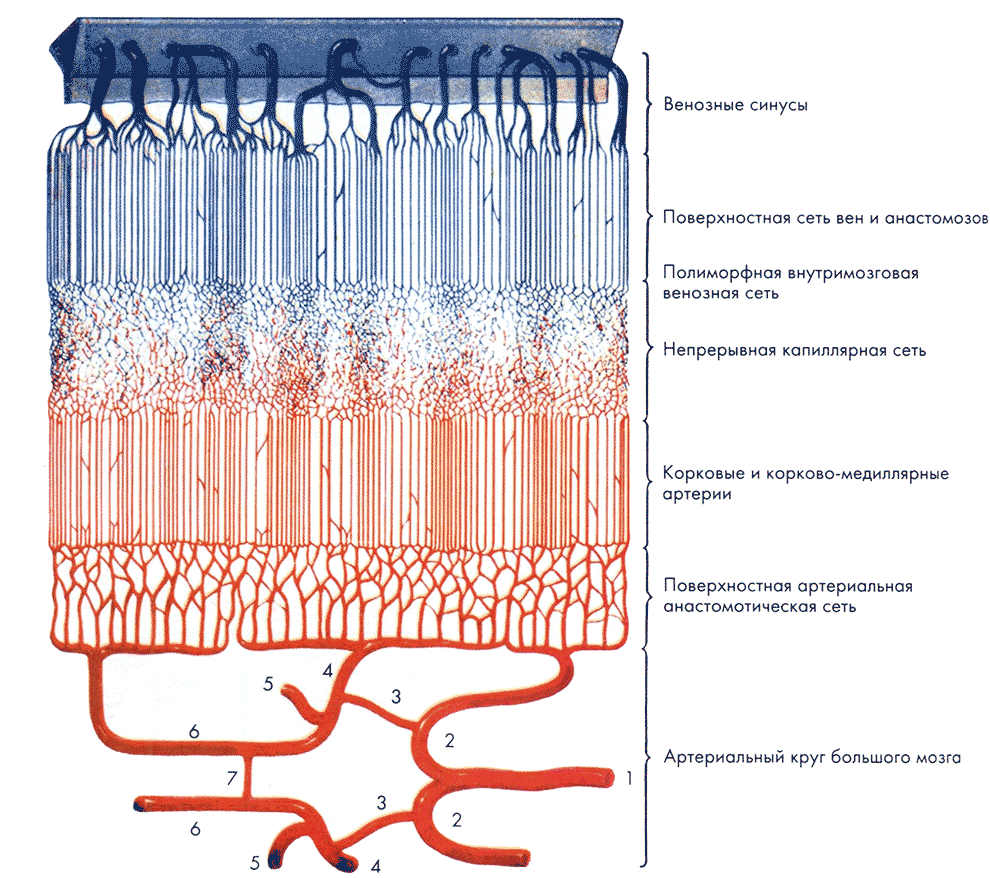
Рис. 5.2. Схема организации внутриорганного кровоснабжения полушарий большого мозга (Беков Д. Б., Михайлов С. С., 1979). 1 - базилярная артерия: 2 - задние мозговые артерии: 3 - задние соединительные артерии: 4 - средние мозговые артерии: 5 - внутренние сонные артерии; 6 - передние мозговые артерии; 7 - передняя соединительная артерия.
При снижении ЦПД включаются механизмы ауторегуляции, и прекапиллярные резистентные сосуды расширяются. Это приводит к увеличению церебрального объема крови, в то время как мозговой кровоток и скорость потребления кислорода мозгом остаются стабильными. Когда церебральные артериолы максимально расширены, достигается предел ауторегуляции, дальнейшее падение ЦПД приводит к снижению кровотока и скорости потребления кислорода мозговой тканью. Возможность возникновения нарушений мозгового кровообращения во многом зависит от состояния церебрального сосудистого резерва (ЦПР), который определяется способностью системы мозгового кровообращения компенсировать гемодинамические нарушения и зависит от сочетанного функционирования анатомических и функциональных источников компенсации. В понятие анатомических источников входят соединительные артерии виллизиева круга, лептоменингеальные и глазной анастомозы, магистральные артерии головы, а также вены головы и шеи. На величину ЦПР существенное влияние оказывает периферическое сопротивление, которое может быть обусловлено как повышением внутричерепного давления, включая венозное, так и наличием артериосклероза (рис. 5.3).
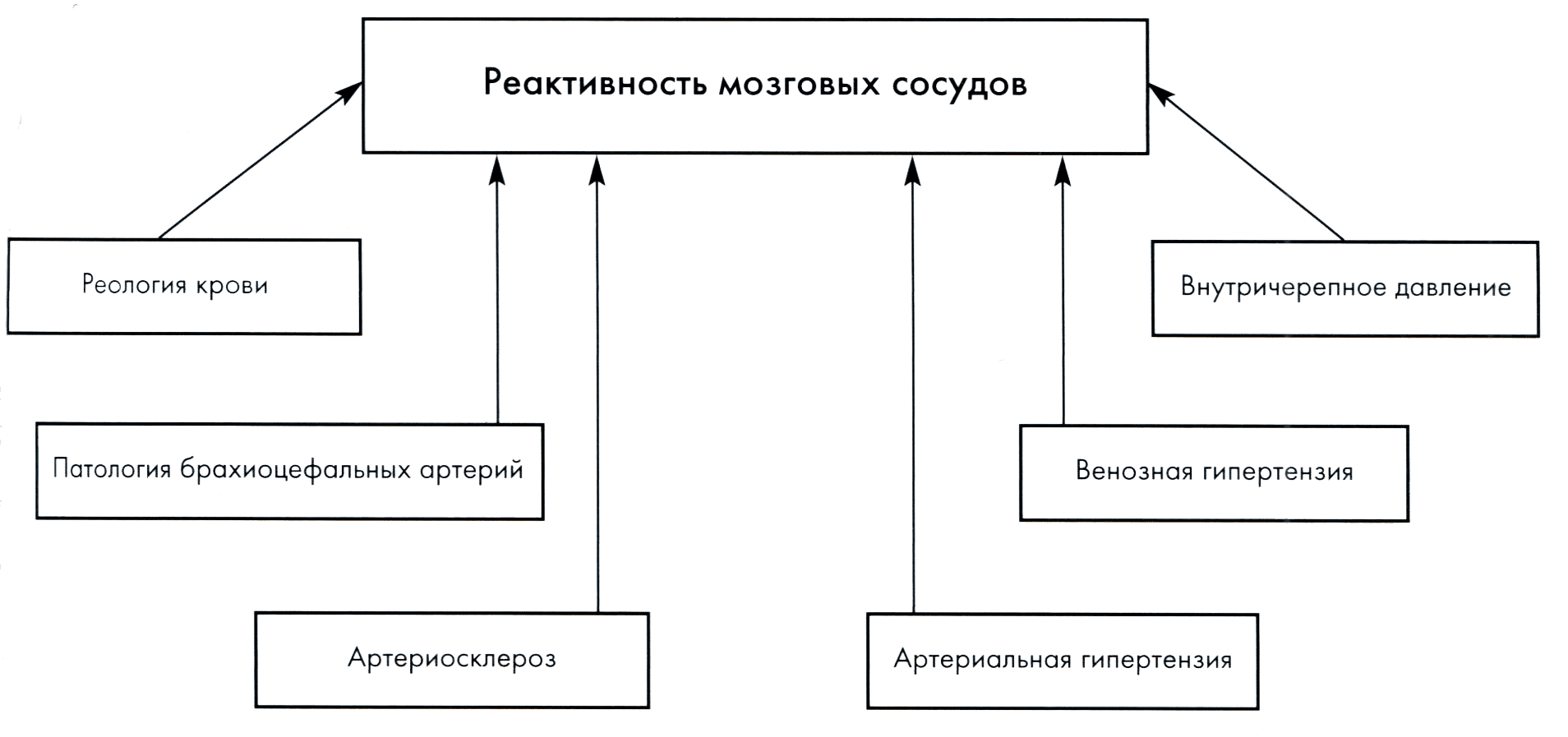
Рис. 5.3. Основные факторы, определяющие реактивность мозговых сосудов (межфакторные взаимодействия не рассматриваются).
При артериальной гипертензии (АГ) наиболее тяжело поражаются артерии диаметром 70-500 мкм и микроциркуляторное русло мозга, причем избирательно преобладают изменения в определенных сегментах и структурах мозга. Ауторегуляция мозгового кровообращения при АГ длительное время остается эффективной, защищая капиллярное русло от высокого АД и его резких перепадов. Методами радиоизотопного исследования были уточнены принципиальные особенности эффекта Остроумова-Бейлиса, который заключается в констрикции артериол мозга в ответ на повышение АД и в их дилатации вслед за его снижением. Однако этот эффект очень непродолжителен (от нескольких секунд до 2 мин), а затем угнетается при изменении метаболизма. При этом действенность миогенной регуляции во многом определяется исходным тонусом сосудов, изменениями газового равновесия крови, состоянием внутричерепного давления, регулярностью сердечного ритма и степенью выраженности артериосклероза. В мозговых артериях постепенно гипертрофируется мышечная оболочка, утолщается и фиброзируется интима, повреждается эндотелиальный слой - формируется липогиалиноз артерий. Структурная адаптация артериальной системы мозга к повышенному АД в виде гипертрофии и гиперплазии гладкой мускулатуры позволяет компенсировать растяжение артериального русла и дает возможность измененным сосудам сопротивляться повышенному сосудистому давлению, смещая таким образом параметры ауторегуляции вправо и предупреждая повреждение гематоэнцефалического барьера. Этот компенсаторный механизм, как правило, предотвращает развитие диапедезных кровоизлияний и массивных интрацеребральных геморрагий. Важно отметить, что величина объемного кровотока у пациентов с АГ варьирует достаточно широко и зависит от фракции выброса, от величины периферического сопротивления, которые изменяются при увеличении давности АГ и тяжести ее проявления. При длительном течении артериальной или венозной гипертензии, как правило более 5-6 лет, в стадии развития церебрального артериосклероза наблюдается вторичное уменьшение линейной и объемной скоростей кровотока. При осложнении АГ стенокардией, инфарктом, с развитием постинфарктного кардиосклероза за счет снижения фракции выброса, конечного систолического и конечного диастолического объемов отмечается изменение центральной гемодинамики и уменьшение артериального притока.
В физиологической и клинической литературе чаще освещаются процессы, связанные с притоком крови (насосная функция сердца, физиология и патология артериальной системы) и мало внимания уделяется венозному оттоку, а это 70-80% общего сосудистого объема крови. Еще в 50-х годах прошлого века было доказано, что повышение венозного давления (ВД) рефлекторно ограничивает поступление крови по сонным и позвоночным артериям. М. И. Холоденко, проведя несколько серий опытов, пришел к выводу, что механические или электрические раздражения яремных вен, твердой мозговой оболочки и стенок продольного синуса вызывают изменения артериального и венозного давления, а также дыхания. При этом изменения АД могут быть прессорного, прессорно-депрессорного или депрессорного типа. При повышении ВД в пещеристой пазухе происходило раздражение рецепторов ВСА, вследствие чего рефлекторно ограничивалось поступление артериальной крови в мозг. Такой же эффект наблюдал М. У. Струнжас и при повышении ВД в атланто-окципитальном синусе, через который проходит позвоночная артерия. М. И. Холоденко (1963 г.) выделил три стадии затруднения ВО. При первой происходит расширение вен мозга и его оболочек, сужение артерий мозга, понижение общего АД, ограничение поступление крови в череп и компенсация венозного застоя. При второй стадии - расширение всех мозговых сосудов, повышение общего АД, ускорение кровотока через мозг и полная или частичная компенсация венозного застоя. В третьей стадии при нарастающем, продолжительном венозном застое происходят значительные метаболические изменения в головном мозге. По мнению М. И. Холоденко, если причина венозного застоя не устраняется, появляются и все более возрастают необратимые морфологические изменения мозговой ткани. Сперва поражается кора мозга, затем подавляется деятельность более устойчивых вазомоторных аппаратов подкорковых структур и сетевидной формации ствола. Нарастание венозного застоя приводит к дальнейшему повышению внутричерепного давления. По мере развития застойной гипоксии в мозге и повышения внутричерепного давления все более нарушаются регулирующие влияния мозга на деятельность внутренних органов. Поэтому прогрессирующий венозный застой в головном мозге М. И. Холоденко считал тяжелым заболеванием не только мозга, но и всего организма в целом.
М. И. Холоденко (1957 г.) и Е. 3. Неймарк (1973 г.) выделяют семь различных клинических синдромов хронической венозной недостаточности (энцефалопатии). Это: астеновегетативный, псевдотуморозно-гипертензионный, полиморфный. беттолепсии, психопатологический, инсультообразный, терминальных и претерминальных судорог. М. М. Одинак с соавт. (1998 г.) считают, что клинические проявления могут быть систематизированы в виде следующих симптомов: 1) гипертензионного (псевдотуморозного); 2) рассеянной мелкоочаговой симптоматики: 3) астенического (астеновегетативного); 4) психопатологического: 5) беттолепсии.
Гипертензионный синдром характеризуется упорными головными болями, головокружением, оглушенностью, застойными дисками зрительных нервов, белково-клеточной диссоциацией в спинномозговой жидкости. В отличие от опухоли при псевдотуморозном синдроме очаговые симптомы представлены более скромно, менее выражены изменения в спинно-мозговой жидкости и на глазном дне, обнаруживаются симптомы внечерепного процесса (легочное сердце, зоб и др.). Для синдрома рассеянной мелкоочаговой симптоматики характерно сочетание органических микросимптомов с признаками венозного застоя. Астенический синдром проявляется эмоциональной лабильностью, быстрой истощаемостью и вялостью, нарушением сна, выраженными вегетативными реакциями и пароксизмами. Психопатологический синдром включает дисфорию, ипохондрические и депрессивные реакции, гипнагогические галлюцинации, иллюзорные зрительные восприятия. Беттолепсия возникает на высоте приступа кашля обычно у больных с хронической легочно-сердечной недостаточностью и характеризуется утратой сознания, иногда сочетающейся с общими или локальными судорогами. В качестве синонимов используются такие, как «гортанное головокружение», «гортанный криз», «кашлевой обморок», «кашлевая эпилепсия», «кашлево-мозговой» синдром («кашлево-обморочный»).
В. Д. Трошин и соавт. (1999 г.) выделяют следующие формы клинических расстройств венозной гемодинамики: 1) венозный застой; 2) венозная энцефалопатия; 3) венозные кровоизлияния; 4) тромбоз вен и венозных синусов; 5) тромбофлебиты; 6) образование каротидно-кавернозных соустий.
М. Я. Бердичевский (1989 г.) выделяет острый, подострый, хронический и ремиттирующий характер течения венозных интрацеребральных расстройств. Рабочая классификация венозной дисциркуляторной патологии включает три стадии формирования хронической мозговой недостаточности: 1 - латентная, 2 - церебральная венозная дистония, 3 - венозная энцефалопатия. В 1-й стадии типичные субъективные и объективные симптомы венозной дисциркуляции еще не определяются, но, как считают В. Д. Трошин и соавт. (2000 г.), по данным рео- энцефалографии они становятся достаточно отчетливыми. Во 2-й стадии проявляются типичная картина и характерные параклинические феномены прогрессирующей венозной дистонии, постепенно переходящие в венозную энцефалопатию со стойкой органической микросимптоматикой (3-я стадия). М. Я. Бердичевский (1989 г.) выделяет легкую, среднетяжелую и тяжелую формы. Поскольку нарушение венозного кровообращения пролонгировано во времени, оправдано также подразделение его на компенсированную, субкомпенсированную и декомпенсированную формы.
Общее состояние и неврологический статус у больных с венозным застоем и ВЭ характеризуются значительной вариабельностью. Пациенты обычно жалуются на постоянную или периодическую головную боль, чаще в утренние часы, ощущение тяжести, распирание, усиление боли в горизонтальном положении, при наклонах. Головная боль, как правило, не отличается большой интенсивностью, но бывает упорной, длительной, чаще диффузной, реже - локальной, в том числе и в форме гемикрании. Нередко беспокоят головокружения (системного или несистемного характера), шум в голове неопределенной локализации, снижение остроты зрения, появление пелены или «мушек» перед глазами. Типичны жалобы на нарушение сна и бодрствования.
По данным Н. В. Бабенкова и соавт. (1998 г.), у большинства больных с нарушениями венозного оттока наблюдались головокружение, оглушенность, нарушение памяти. Клиническое обследование неврологического статуса выявило только наличие астенического, гипертензионного, психоорганического синдромов. При УЗДГ и ДС в подавляющем большинстве случаев выявлены извитости, гипоплазия позвоночных артерий, их позднее вхождение в канал поперечных отростков. Обращает на себя внимание бледность лица в сочетании с цианозом губ, кончика носа, мочек ушей, усиливающимся при перемене температуры, отечность лица, особенно в утренние часы. Характерная триада выраженной венозной недостаточности - отечность и цианоз кожи лица, расширение подкожных вен на лице и шее. Некоторые больные жалуются на заложенность носа, что связано с расширением вен слизистой носа. Из объективной неврологической симптоматики следует отметить умеренную гиперрефлексию сухожильных и периостальных рефлексов, асимметрию иннервации ряда черепных нервов, неустойчивость в позе Ромберга, эмоциональную лабильность. Особенно часты у данной категории больных вегетативные нарушения в форме как локальных, так и общих вазомоторных пароксизмов, как симпатоадреналовых (с повышением АД, сильными головными болями и кардиалгиями), так и вагоинсулярными (со снижением АД, перепадами пульса, затруднением дыхания, гипергидрозом, головокружением). Нередки в клинике и смешанные варианты пароксизмов, а также синкопе.
Первоначально венозные дистонии проявляются рефлекторной вазодилатацией (реже - вазоконстрикцией), а затем - стойким вазопарезом, развивающимся за счет ареактивности вазомоторного центра. При длительном существовании венозной дистонии нарушается микроциркуляция, извращается работа клапанного аппарата, что проявляется гиперволемическим вариантом венозной гипертонии. Значительно изменяется мозговой метаболизм, в частности кислородный, углеводородный и водный баланс мозга, нарастают гипоксия и гиперкапния, способствующие дальнейшему повышению венозного и внутричерепного давления и отеку мозга. В процессе развития ишемии мозговой ткани важное повреждающее значение имеют токсическое воздействие на клетку избыточного накопления возбуждающих аминокислот (эксайтотоксичность), лавинообразное поступление в клетки ионов кальция, распад клеточных мембран, накопление свободных радикалов и продуктов перекисного окисления липидов.
При венозной гипертензии, наряду с повышением венозного давления, характерно депонирование крови в посткапиллярных венах, венулах, мелких венах. венозных синусах. При остром общем венозном полнокровии вследствие недостатка кислорода в венозной крови в тканях развиваются гипоксия и ацидоз, повышается сосудистая проницаемость, прежде всего в микроциркуляторном русле, что приводит к плазматическому пропитыванию и отеку, дистрофическим (а в тяжелых случаях и некротическим) изменениям, к диапедезным кровоизлияниям. При общей венозной гипертензии изменения в поражающихся прежде всего органах депонирования крови - легких, печени, коже с подкожной клетчаткой, почках, селезенке, вследствие структурно-функциональных особенностей отличаются в отдельных деталях. При хроническом венозном полнокровии, кроме перечисленных процессов, наблюдается атрофия паренхимы и склероз за счет активизации фибробластов и разрастания соединительной ткани, приводящей к уплотнению пораженных органов и тканей. Отмечается редукция капилляров, развивается склероз микрососудов, сужение их просвета (перекалибровка) вплоть до полной обтурации, атрофия эндотелиоцитов. Формируется централизация микродинамики за счет тока крови по магистральным сосудам микроциркуляторного русла. Это приводит к уменьшению объема транскапиллярного кровотока, увеличивает тканевую гипоксию, нарушает обмен веществ в сосудистой стенке и окружающих тканях, что обусловливает нарастающую дистрофию, атрофию клеток и склероз (рис. 5.4).
Современные представления о гемодинамических изменениях вследствие дефицита мозгового кровотока явились подтверждением и объяснением известного феномена - ишемические изменения выявляются преимущественно в зонах, снабжаемых конечными, корковыми ветвями мозговых артерий. Это в свою очередь приводит к развитию таких тяжелых форм церебральной патологии, как лакунарное состояние мозга, субкортикальная артериосклеротическая энцефалопатия с исходом в деменцию, обозначаемая как гипертоническая лейкоэнцефалопатия, сосудистый паркинсонизм и др.
Эндотелиальные клетки первыми воспринимают механическую деформацию сосудистой стенки, выступая при этом в роли «маэстро циркуляции». Как известно, эндотелий сосудов обладает способностью реагировать на физические, химические и гуморальные изменения окружающей среды продукцией сосудорасширяющих (эндотелиальный релаксирующий фактор, или оксид азота; простациклин; эндотелиальный гиперполяризующий фактор) и сосудосуживающих факторов (эндотелии-1, тромбоксан А2, простогландин Н2, ангиотензин-2), баланс которых определяет тонус сосудистых гладкомышечных клеток. В настоящее время уже доказаны такие позитивные эффекты оксида азота на сердечно-сосудистую систему, как релаксация гладкомышечных клеток, подавление агрегации тромбоцитов и клеточной пролиферации посредством угнетения синтеза гуанилмонофосфата. В начальной стадии заболевания наблюдается нарушение эндотелийзависимой вазодилатации.
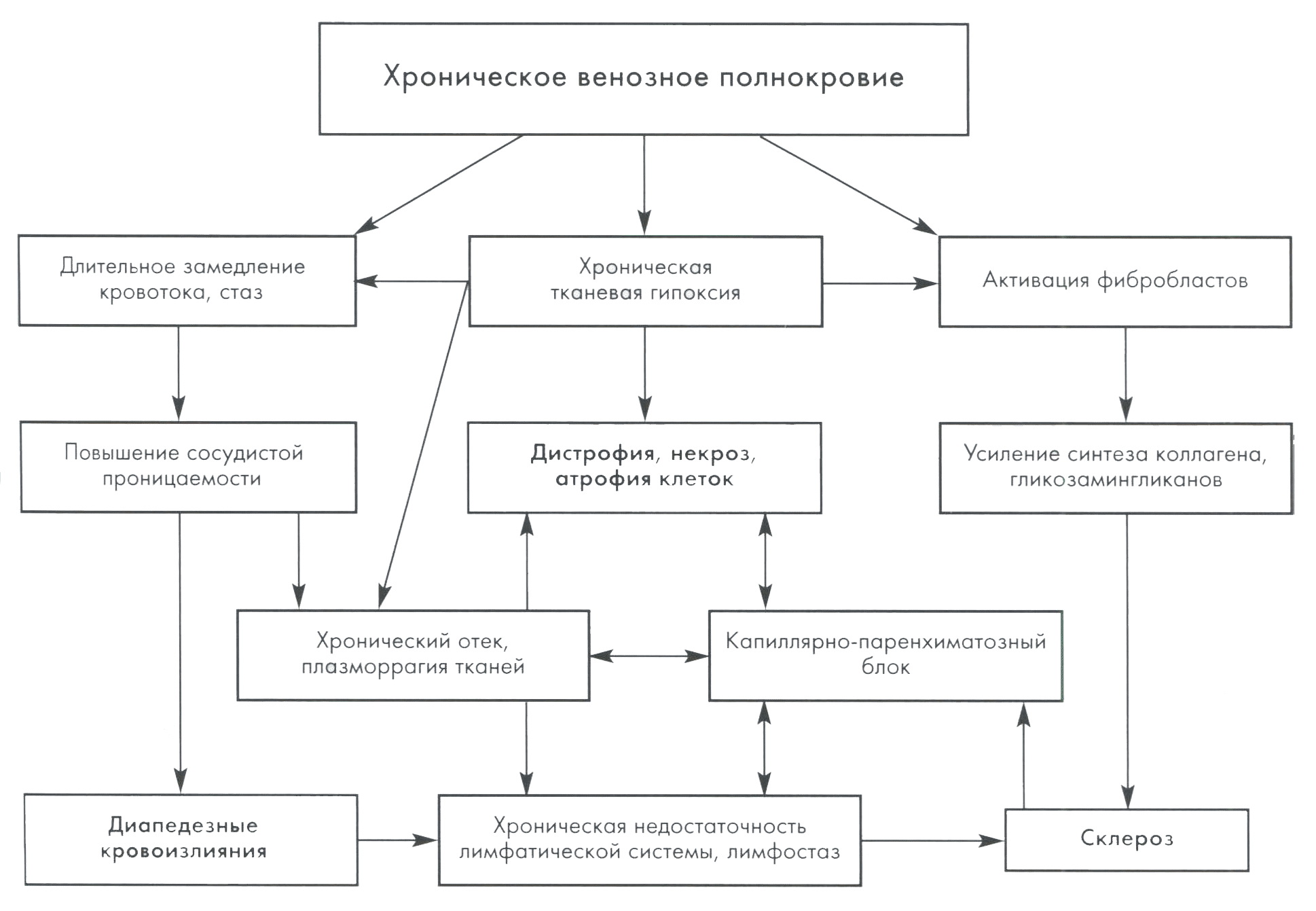
Рис. 5.4. Морфогенез изменений при хроническом венозном полнокровии (Салтыков Б. Б. и соавт., 2002).
Эндотелиальная дисфункция, приводя к снижению эндотелиального релаксирующего фактора, ухудшает растяжимость сосудов. По данным Е. Е. Гогина (1997 г.), в этих условиях надлежащий уровень тканевой перфузии достигается большей работой сердца. При нарушении церебрального венозного оттока длительностью более 5 лет нарушения функции эндотелия сопоставимы с таковыми при АГ. В связи с этим для уменьшения сокращения, пролиферации и гипертрофии гладкомышечных клеток как при артериальной, так и при венозной гипертензии, чрезвычайно актуальным является нормализация функции эндотелия.
Функционирование системы мозгового кровообращения тесно связано с ликвородинамикой, и реализация процессов регулирования мозгового кровообращения включает в себя взаимодействие объемов и давлений жидких сред крови и цереброспинальной жидкости как в полости черепа, так и между полостями черепа и позвоночника. Обратное всасывание ликвора происходит через арахноидальные ворсинки и пучки арахноидальных клеток, выдвинутых в просвет синусов твердой мозговой оболочки, особенно в верхний сагиттальный синус. Кроме того, имеются и некоторые другие пути резорбции ликвора: лимфатическая система, ворсинчатое сплетение, оболочки мозга, перивентрикулярная зона, адвентиция сосудов. Основной ток жидкости происходит под влиянием положительного градиента гидростатического давления между спинно-мозговой жидкостью и венозной кровью, причем арахноидальные ворсины действуют наподобие клапанов, позволяющих жидкости продвигаться из ликворного пространства в кровь, но не в обратном направлении. При давлении ликвора около 112 мм вод. ст. создается равновесие между его продуцированием и резорбцией. При медленном повышении внутричерепного давления вначале возможна неплохая компенсация нарушения ликвородинамики. Оно происходит за счет резервного внутричерепного пространства, а в дальнейшем - в результате стимуляции всасывания ликвора. По данным Я. А. Хананашвили (2001 г.) при повышении давления цереброспинальной жидкости наблюдаются снижение трансмурального давления и уменьшение растягивающей сосуды силы, что вызывает ауторегуляторную дилатацию мозговых артерий и усиление оттока венозной крови за счет повышения тонуса венозных сосудов мозга. В результате подъем давления спинно-мозговой жидкости не приводит к изменениям мозгового кровотока. При истощении компенсаторных механизмов у больных может развиться синдром внутричерепной гипертензии. Арахноидальные ворсины действуют наподобие клапанов, позволяющих жидкости продвигаться из ликворного пространства в кровь, но не в обратном направлении, поэтому при венозной гипертензии нарушается резорбция ликвора. При повышении венозного давления вследствие нарушения ВО в экстракраниальном отделе также нарушается поступление жидкости из ликворного пространства в кровь и возможно повышение давления спинно-мозговой жидкости. Эти факторы могут действовать совместно или раздельно. Длительное нарушение абсорбции цереброспинальной жидкости лежит в основе развития нормотензивной гидроцефалии с развитием деменции, тазовых расстройств, нарушений ходьбы и расширением желудочковой системы. При этом S. Khoromi и соавт. (1995 г.) и В. Kristensen и соавт. (1996 г.) заметили, что у пациентов с нормотензивной гидроцефалией достоверно чаще встречается артериальная гипертензия и инфаркты в глубинных отделах белого вещества. По данным И. Я. Раздольского (1954 г.), венозный застой приводит к повышению внутричерепного давления, главным образом, в тех случаях, когда в его основе лежит сдавление яремных вен, вены Галена.
Функциональная венозная гипертензия и нарушения микроциркуляции нередко сочетаются с обогащением красной крови, нарушениями ее реологических свойств. Повышение венозного давления, вызывающее ухудшение условий микроциркуляции, вносит дополнительный вклад в нарастание периферического сопротивления и может являться внутренним фактором риска развития гипертонической болезни. Между тем развитие гиперкинетического синдрома, величина сердечного выброса определяются главным образом преднагрузкой, конечным диастолическим объемом желудочков, обеспеченных венозным возвратом.
Таким образом, в патогенезе ишемии мозга имеют значение системные и локальные факторы, приводящие к нарушениям церебральной гемодинамики. Нарушения системной гемодинамики могут быть вызваны патологией, приводящей к снижению насосной функции миокарда, повышению или снижению системного АД, срыву ауторегуляции мозгового кровотока, нарушению коагуляционных и реологических свойств крови (рис. 5.5).
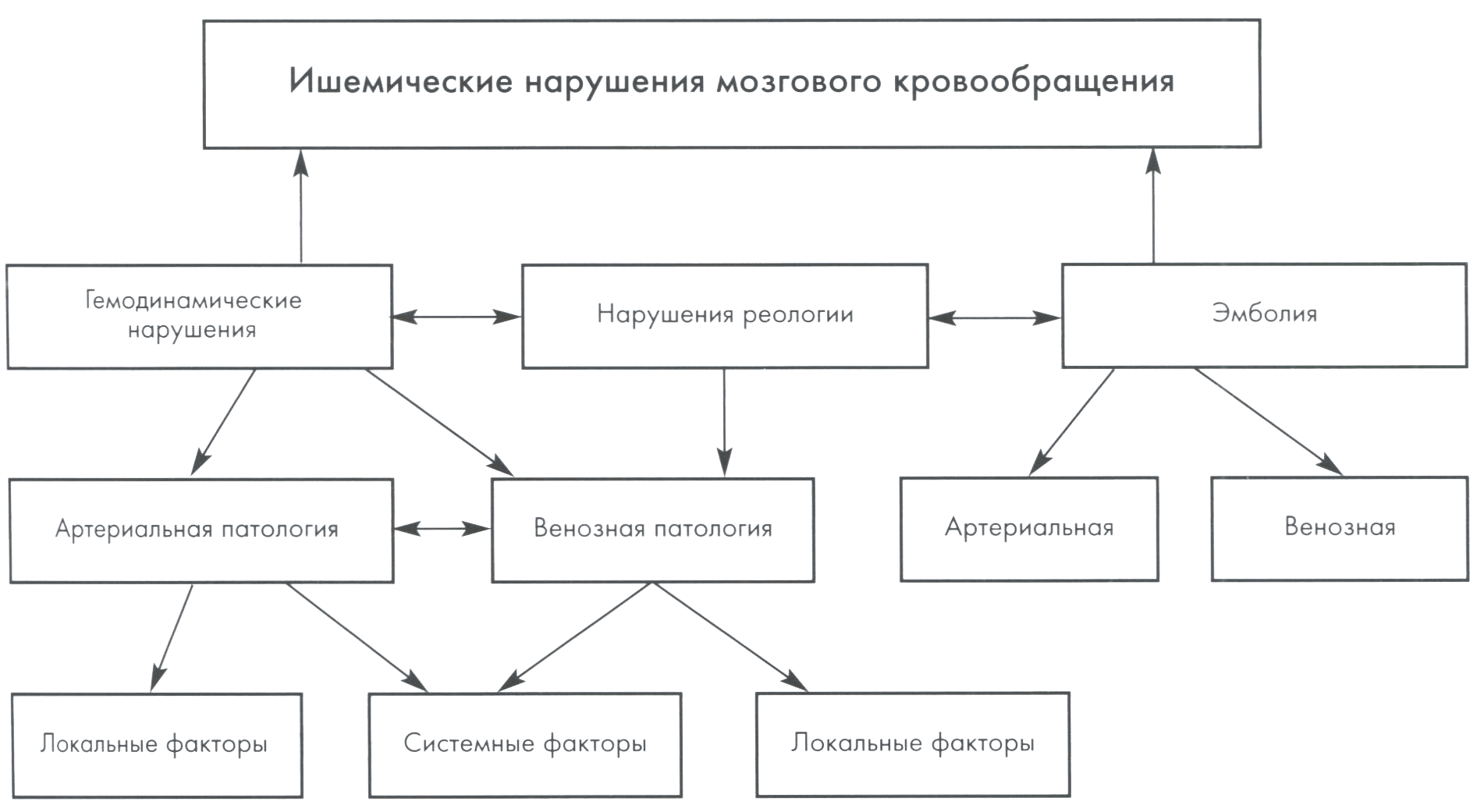
Рис. 5.5. Основные патогенетические звенья ишемических нарушений мозгового кровообращения.
Изменения центральной гемодинамики могут быть опосредованы изменениями активности гормональных систем, в частности, гипоталамо-гипофизарно- надпочечниковой оси, гормоны которой (АКТЕ кортизол, альдостерон, катехоламины) обладают выраженными вазопрессорными эффектами и являются универсальными факторами адаптации к стрессу, в том числе эндогенному, возникающему при любой соматической и неврологической патологии.
К системным факторам относится и венозная патология, в частности, венозная гипертония. В. А. Вальдман, углубленно изучавший венозное давление и тонус вен, разделил ее на две группы: физиологическую (конституционную, тоногенную) и патологическую (неврогенную, гормональную и застойную при сердечной недостаточности или механическом препятствии венозного оттока). К постоянно действующим факторам при венозной гипертонии относятся: 1) давление крови, определяемое работой сердца, пульсацией артериальных сосудов и тонусом артериол; 2) активная диастола сердца (присасывающий эффект), определяемая частично величиной остаточного давления в полостях сердца; 3) состояние транскапиллярного обмена, которое складывается из разницы между фильтрацией жидкой части плазмы и резорбцией тканевой жидкости (с учетом притока лимфы в венозную систему); 4) состояние внутритканевого давления; 5) давление в малом круге кровообращения. К периодически действующим факторам относятся: 1) неврогенный фактор с преимущественным влиянием на венозный тонус симпатической нервной системы; 2) действие биологически активных веществ на посткапилляры, венулы и продукты обмена; 3) влияние дыхания на ВД (оно достаточно сложно, так как при снижении давления в грудной клетке при вдохе повышается давление в брюшной полости); 4) состояние движения мышц, влияющих на венозный кровоток как при динамическом, так и статическом (тоническом) напряжении. Таким образом, периферическое венозное давление есть интегральная величина, которая в каждом конкретном периоде времени функционирует, подвергаясь влияниям конкретных, доминирующих на данный момент факторов.
Венозные дистонии могут возникать как следствие нарушения центральных регуляторных механизмов сосудистого тонуса, ведущего к функционально-динамическим расстройствам венозной гемоциркуляции. Застойные явления в малом круге могут быть вызваны тромбоэмболиями и тромбозами легочной артерии, острой или хронической правожелудочковой недостаточностью при заболеваниях сердца и аорты. К венозному застою приводит и хроническая легочно-сердечная недостаточность, вызванная обструктивными бронхолегочными заболеваниями (пневмосклероз, эмфизема легких, бронхиальная астма и др.), а также нарушениями внешнего дыхания из-за деформаций грудной клетки, плевральных спаек, резкого ожирения или метеоризма. Веногипотония (снижение тонуса венозной стенки) в виде резкого снижения венозного оттока наблюдается у больных при приеме нитроглицерина, биогенных аминов, интоксикациях, включая алкогольные, при снижениях атмосферного давления.
Сниженная реактивность мозговых сосудов и низкая перфузия у пациентов с ишемическими инсультами на фоне нарушенного венозного оттока при хронических неспецифических заболеваниях легких на практике обусловливает низкие компенсаторные возможности церебрального кровообращения, плохой регресс очаговых неврологических симптомов и, по мнению А. И. Исайкина и соавт. (1999 г.), высокую внутрибольничную летальность.
Наиболее частая причина локальных артериальных гемодинамических расстройств - окклюзирующие заболевания экстра- и интракраниальных артерий. Наличие атеросклеротических бляшек, тромбов, патологических извитостей, аневризм, расслоений, экстравазальных компрессий вызывает не только снижение притока крови с редукцией микрососудистого русла, но и смещение точек гемодинамического равновесия, образование зон стагнаций, нарушение ламинарности потока, а следовательно, усиливается склонность к тромбозу и эмболизации. Большое значение при этом имеет сочетанное воздействие системных факторов - снижение АД, падение сердечного выброса, изменения реологических свойств крови, причиной которых могут стать ятрогенные воздействия, связанные с назначением активных гипотензивных и мочегонных средств.
Купить книги по УЗИ сосудов в интернет-магазине shopdon.ru
Книга "Комплексная ультразвуковая диагностика патологии периферических сосудов"
Учебно-методическое руководство

Автор: Шумилина М. В.
ISBN: 978-5-7982-0298-0
В руководстве изложены принципы и методология комплексной ультразвуковой диагностики патологии экстра- и интракраниальных сосудов, сосудов верхних и нижних конечностей. Рассматриваются критерии гемодинамической значимости поражения брахиоцефальных сосудов и требования к их исследованию. Большое внимание уделено проблемам венозного давления, функциональной флебогипертензии.
Издание предназначено для специалистов по ультразвуковой (лучевой) и функциональной диагностике, а также врачей других специальностей, аспирантов, ординаторов, студентов медицинских вузов, интересующихся проблемами ангиологии.
Купить книги по УЗИ сосудов в интернет-магазине shopdon.ru
Содержание книги "Комплексная ультразвуковая диагностика патологии периферических сосудов" - Шумилина М. В.
Глава 1. Особенности допплеровского метода
Глава 2. Ультразвуковая допплерография и дуплексное сканирование артерий нижних конечностей
Глава 3. Особенности физиологии венозной системы
Глава 4. Ультразвуковая диагностика патологии вен нижних конечностей
Глава 5. Концепция комплексного обследования брахиоцефальных сосудов (артерий и вен)
Глава 6. Ультразвуковое обследование брахиоцефальных и церебральных артерий как один из подходов к решению проблемы мозговых инсультов
Глава 7. Комплексная ультразвуковая диагностика патологии брахиоцефальных артерий
Глава 8. Ультразвуковое обследование брахиоцефальных вен
Глава 9. Транскраниальная допплерография
Глава 10. Дисфункция эндотелия
Глава 11. Каротидные хемодектомы
Глава 12. Венозное давление
Глава 13. Что такое гемодинамически значимое поражение?
Глава 14. Требования к ультразвуковой диагностике брахиоцефальных сосудов
Глава 15. Дефект межпредсердной перегородки и краниальные синдромы






























0 комментариев