Название и адрес медицинского центра
_______________________________________________________
Ультразвуковое исследование
Контрон СИГМА 210, ирис. Электронные линейный датчик 7,5 МГц и конвексный - 3,5 МГц (название ультразвукового оборудования)
Врач ______________________________________
Пациент __________________________________
Исследование № ____________ от __.__.____
Исследуемый орган______________________
Протокол ультразвукового исследования матки с придатками
(образец протокола УЗИ ультразвукового описания патологии эхоструктуры матки с придатками)
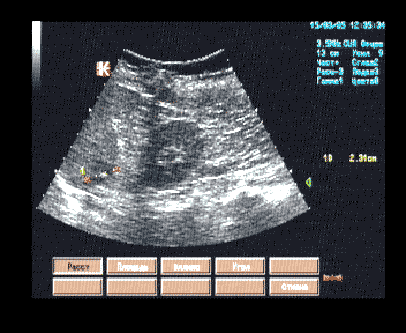
Матка 124 х 105 х 80 мм, anteflexio, неправильной овальной формы, типичного расположения, контуры деформированы, миометрий неоднородный за счёт не менее 8 — ми узловых образований, расположенных во всех отделах матки: в проекции шеечноперешеечного отдела гипоэхогенный узел размером 46 х 32 мм, имеющий четкие ровные границы, гипоэхогенную структуру; четыре узла л в задней стенке диаметрами до 30 мм, в дух из них гиперэхогенные включения диаметрами 7 мм и 10 мм, дающие акустические тени; в проекции передней стенки тела матки три гипоэхогенных узла диаметрами до 25 мм; на остальном протяжении миометрий повышенной эхогенности, полость щелевидная, в проекции просвета дополнительных эхоструктур не лоцировано, М-эхо толщиной 4 мм.
Яичники полностью прикрыты.
Заключение
Эхографические признаки многоузловой интрамуральной миомы матки.
Ультразвуковая диагностика не является основным методом и требует подтверждения диагноза другими методами обследования.
Подпись__________________________
Все протоколы УЗИ патология и норма
Купить профессиональную медицинскую литературу по УЗИ диагностике в интернет-магазине shopdon.ru
Купить профессиональную медицинскую литературу по УЗИ диагностике в интернет-магазине shopdon.ru
Книга "Практическое руководство по ультразвуковой диагностике. Общая ультразвуковая диагностика" - В. В. Митьков
Фундаментальное клиническое руководство подготовлено коллективом ведущих специалистов ультразвуковой диагностики. В книге представлены разделы, посвященные ультразвуковым диагностическим системам, физическим принципам ультразвуковой диагностики, ультразвуковой диагностике заболеваний печени, желчевыводящей системы, поджелудочной железы, пищевода, желудка, кишечника, селезенки, почек, мочевого пузыря, предстательной железы и семенных пузырьков, надпочечников, органов мошонки, лимфатической системы, молочных, щитовидной, околощитовидных и слюнных желез, органов грудной клетки.
Книга предназначена для врачей ультразвуковой диагностики, рентгенологов, радиологов, терапевтов, гастроэнтерологов, эндокринологов, хирургов, урологов, и всех заинтересованных специалистов.
Книга "Эхография в гинекологии" - Озерская И. А.

В 3 издании монографии «Эхография в гинекологии» рассмотрены все основные вопросы ультразвуковой диагностики в гинекологии, с которыми ежедневно сталкивается врач, обследующий органы малого таза у женщин в амбулаторной практике и гинекологическом стационаре. Внесены дополнения результатов собственных научных исследований, а также опыта работы ведущих лабораторий мира и нашей страны за последнее время. Особое внимание уделено вопросам стандартизации при обследовании миометрия, эндометрия и яичников, основанных на рекомендациях групп международных экспертов. Написаны новые главы, посвященные послеродовому периоду в норме и при осложнениях, ультразвуковому мониторингу при проведении аборта как медикаментозного, так и путем вакуум-аспирации, а также послеабортным и послеоперационным осложнениям, включая проблему рубца на матке.
Каждая глава состоит из небольшого этио-патогенетического раздела, подробно освещены вопросы эхографической диагностики, включая данные цветового картирования, допплерометрии, новых, недостаточно распространённых методик и дифференциально-диагностические критерии. Каждая глава иллюстрирована большим количеством эхограмм как типичного, так и нетипичного изображения рассматриваемой патологии. Определены диагностические возможности эхографии, цветового картирования и допплерометрии во всех рассматриваемых разделах гинекологии. Представлены новые направления диагностики и лечения, внедряемые в гинекологическую практику в течение последних лет. В приложение включены таблицы всех нормативных параметров, предложены протоколы ультразвукового исследования органов малого таза и проведения эхогистеросальпингоскопии.
Книга рассчитана на врачей ультразвуковой диагностики, гинекологов, акушеров, онкогинекологов, хирургов и врачей смежных специальностей.
Купить книгу "Эхография в гинекологии" - Озерская И. А.
Книга "Эхокардиография от Рыбаковой" - М. К. Рыбакова, В. В. Митьков

Данное издание представляет собой практическое руководство по эхокардиографии, в котором отражены все современные технологии, применяемые в настоящее время. Исключительный интерес для специалистов представляет CD-ROM с подборкой видеоклипов по всем основным разделам, включающих редкие случаи диагностики.
Особенность издания - попытка объединить и сравнить результаты эхокардиографического исследования сердца и паталогоанатомический материал по всем основным разделам.
Большой интерес представляют разделы, содержащие новые технологии исследования, такие как трех- и четырехмерная реконструкция сердца в реальном времени, тканевая допплерография. Большое внимание уделено также классическим разделам эхокардиографии – оценке легочной гипертензии, клапанных пороков сердца, ишемической болезни сердца и ее осложнений и т.д.
В книге представлены огромный иллюстративный материал, большое количество схем и рисунков, приведены алгоритмы тактики проведения исследования и диагностики по всем разделам эхоКГ.
Руководство помогает разрешить спорные и злободневные вопросы, позволяет ориентироваться в расчетах и измерениях, содержит необходимую справочную информацию.
Книга написана сотрудниками кафедры ультразвуковой диагностики ГБОУ ДПО «Российская медицинская академия последипломного образования'' Министерства здравоохранения Российской Федерации» (база – ГКБ им. С.П. Боткина, Москва).
Издание предназначено для специалистов эхокардиографии, врачей ультразвуковой и функциональной диагностики, кардиологов и терапевтов.
Купить книгу "Эхокардиография от Рыбаковой" - М. К. Рыбакова, В. В. Митьков
Книга "УЗИ в акушерстве и гинекологии. Том 1 Акушерство" - Мерц Эберхард
Данное издание является наиболее полным иллюстрированным руководством по ультразвуковой диагностике в акушерстве и гинекологии.
Авторы постарались охватить все известные на сегодняшний день режимы УЗИ, но тем не менее основной акцент делается на наиболее доступных методиках, технике, глубоком анализе результатов. Результаты ультразвуковых исследований приводятся в тесной корреляции с клиническими и лабораторными данными, что значительно повышает ценность диагностической информации и формирует у врача клиническое мышление. Первый том посвящен УЗИ в акушерстве.
Рассматриваются ультразвуковые параметры матери и плода на разных сроках гестации, различные варианты патологии беременности.
Отдельные главы посвящены ультразвуковой допплерографии и трехмерному УЗИ в режиме реального времени, ультразвуковой поддержке инвазивных диагностических и лечебных процедур. В приложении дается подробная справочная фетометрическая информация.
Книга предназначена для акушеров-гинекологов, специалистов по ультразвуковой диагностике женских консультаций и акушерских стационаров, студентов медицинских вузов и факультетов.
Купить книгу "УЗИ в акушерстве и гинекологии. Том 1 Акушерство" - Мерц Эберхард
Книга "Ультразвуковая диагностика в акушерстве и гинекологии: в 2 томах. Том 2. Гинекология" - Мерц Эберхард
Данное издание является наиболее полным иллюстрированным руководством по ультразвуковой диагностике в акушерстве и гинекологии. Авторы постарались охватить все известные на сегодняшний день режимы УЗИ, но тем не менее основной акцент делается на наиболее доступных методиках, технике, глубоком анализе результатов. Результаты ультразвуковых исследований приводятся в тесной корреляции с клиническими и лабораторными данными, что значительно повышает ценность диагностической информации и формирует у врача клиническое мышление.
Второй том посвящен проблемам ультразвуковых исследований в гинекологической практике: УЗ-анатомии здоровой женщины, порокам развития и заболеваниям женского полового тракта. Отдельные главы посвящены трансвагинальному и трансректальному методам исследования, а также УЗИ молочных желез.
Книга предназначена для акушеров-гинекологов, специалистов по ультразвуковой диагностике женских консультаций и акушерских стационаров, студентов медицинских вузов и факультетов.
Книга "Основы ультразвукового исследования сосудов" - В. П. Куликов

Руководство «Основы ультразвукового исследования сосудов» предназначено для тех, кто хотел бы получить по возможности краткую, но достаточно полную и главное практически полезную информацию по ультразвуковой диагностике сосудистой патологии. Автор, профессор Куликов Владимир Павлович, известен специалистам по первой в России книге, посвященной дуплексному сканированию сосудов, и руководству для врачей по ультразвуковой диагностике сосудистых заболеваний.
В Руководстве представлены важнейшие сведения о технике исследования, ультразвуковых критериях нормы и патологии кровеносных сосудов, основанные на международных согласительных документах и практическом опыте работы автора. Особое внимание уделено стандартизации техники, объема и терминологии описания ультразвукового исследования сосудов.
Книга предназначена для врачей ультразвуковой и функциональной диагностики, сосудистых хирургов, неврологов и кардиологов, а так же для студентов и врачей, обучающихся по программам ультразвукового исследования сосудов.
Купить книгу "Основы ультразвукового исследования сосудов" - В. П. Куликов